
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
9.4.2. Обмен пировиноградной кислоты
В зависимости от места и условий протекания гликолиза, наличия соответствующих ферментных систем, судьба ПВК может быть различна:
1. В анаэробных условиях происходит восстановление до молочной кислоты (молочнокислое брожение, окончание гликолиза):
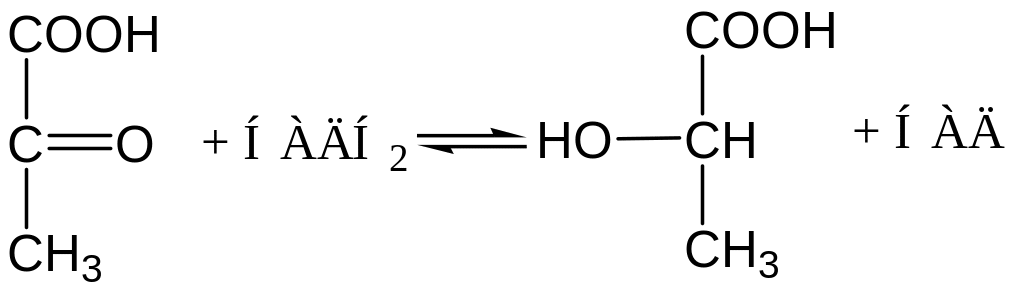
Фермент – лактатдегидрогеназа.
Молочная кислота накапливается при активной мышечной работе и вызывает утомление мышц. Освобождение мышц от нее достигается выведением ее в кровь, а затем – в печень, где в аэробных условиях молочная кислота превращается в глюкозу, которая затем вновь поступает в мышцы и включается в гликолиз. Часть молочной кислоты в аэробных условиях окисляется до СО2 и Н2О (1/5 – 1/6) или идет на ресинтез гликогена.
Изменение свободной энергии G310 при расщеплении глюкозы до молочной кислоты (С6Н12О6 → 2С3Н6О3) составляет около 210 кДж/моль. Из этого количества энергии около 126 кДж рассеивается в виде тепла, а 84 кДж накапливается в форме АТФ. Концевая макроэргическая связь АТФ соответствует примерно 33,6–42,0 кДж/моль. Таким образом, КПД гликолиза (до молочной кислоты) составляет около 0,4 (40%).
Молочнокислое брожение осуществляется молочнокислыми бактериями. Одни из них в процессе брожения углеводов образуют только молочную кислоту, а другие из каждой молекулы глюкозы «производят» по 1 молекуле молочной кислоты, этилового спирта и углекислого газа.
2. Спиртовое брожение осуществляется так называемыми дрожжеподобными организмами и некоторыми плесневыми грибами в анаэробных условиях: С6Н12О6 2СО2 + 2С2Н5ОН.
По своему механизму спиртовое брожение близко к гликолизу. При спиртовом брожении ПВК вначале подвергается декарбоксилированию под действием фермента пируватдекарбоксилазы, которая требует наличия ионов магния и кофермента тиаминпирофосфата (витамин В1):
СН3–СО–СООН СН3–СНО + СО2.
Затем уксусный альдегид восстанавливается в этанол при участии фермента алкогольдегидрогеназы:
СН3–СНО + НАДН2 СН3–СН2–ОН + НАД.
Существуют и другие виды брожения, отличающиеся конечными продуктами: пропионовокислое, ацетоноэтиловое, маслянокислое, янтарнокислое, уксуснокислое и др.
3. В аэробных условиях происходит окислительное декарбокислирование (дыхание) с образованием ацетил-КоА, который затем может окисляться до СО2 и Н2О. Реакция окислительного декарбоксилирования идет в соответствии с уравнением:
СН3–СО–СООН + НАД + НSКоА СО2 + СН3–СОSКоА + НАДН2
и ускоряется мультиэнзимным комплексом, называемым пируватдегидрогеназным.
Образовавшийся ацетил-КоА вступает в цикл три- и дикарбоновых кислот.
9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
Цикл три- и дикарбоновых кислот впервые был открыт английским биохимиком Х. А. Кребсом в 1937 г. В 1953 г. он удостоился Нобелевской премии по физиологии и медицине. Х.А. Кребс впервые постулировал значение данного цикла для полного «сгорания» ПВК, главным источником которой является гликолитическое превращение углеводов. В дальнейшем было показано, что цикл Кребса является «фокусом», в котором сходятся практически все метаболические пути.
Данный цикл состоит из 8-ми последовательных реакций. Ферменты цикла, ускоряющие единый метаболический многоступенчатый процесс окисления ацетильных групп, собраны в метаболон, локализованный между расположенными друг против друга поверхностями внутренней мембраны митохондрий (в кристах). В метаболоне осуществляется эстафетная передача промежуточных продуктов цикла от одного фермента к другому без их высвобождения в матрикс митохондрии. Поэтому процесс идет с большой скоростью. Рядом с метаболоном цикла Кребса располагаются пируватдегидрогеназный комплекс и, вероятно, метаболон -окисления жирных кислот, поставляющие ему ацетил-КоА.
Начинается цикл с конденсации ацетил-КоА со щавелевоуксусной кислотой (ЩУК) и образования лимонной кислоты. Затем лимонная кислота путем 4-х дегидрирований и 2-х декарбоксилирований теряет 2 атома углерода и снова в цикле Кребса появляется ЩУК, т. е. в результате полного оборота цикла молекула ацетил-КоА «сгорает» до СО2 и Н2О, а молекула ЩУК регенерируется.
Ниже приведены реакции цикла Кребса.
1. Конденсация ацетил-КоА со ЩУК, катализируемая ферментом цитратсинтазой.

G = –31,38 кДж/моль
2. Изомеризация лимонной кислоты (цитрата) в изолимонную (изоцитрат) под действием аконитатгидратазы, идет в две стадии:
2.1. Дегидратация лимонной кислоты:
 G
= 8,37 кДж/моль
G
= 8,37 кДж/моль
2.2. Гидратация цис-аконитовой кислоты:
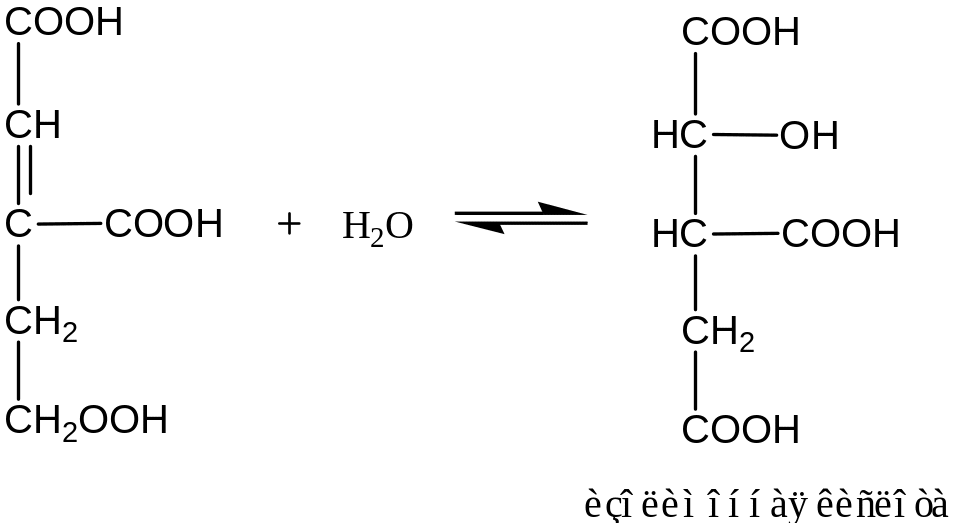 G
= –2,09 кДж/моль
G
= –2,09 кДж/моль
3. Окисление изолимонной кислоты, сопровождающееся декарбоксилированием. Катализируется ферментом изоцитратдегидрогеназой (кофермент – НАД):

G = –8,37 кДж/моль
4. Окислительное декарбоксилирование -кетоглутаровой кислоты, катализируемое -кетоглутаратдегидрогеназой и приводящее к образованию сукцинил-КоА:
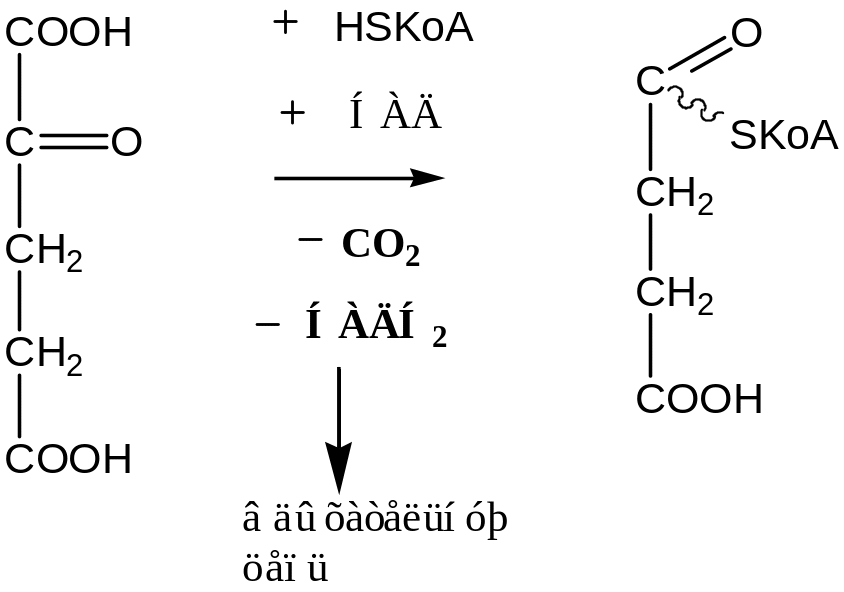 G
= –30,12 кДж/моль
G
= –30,12 кДж/моль
5. Субстратное фосфорилирование, катализируемое сукцинат: КоАлигазой:
 G
= –3,35 кДж/моль
G
= –3,35 кДж/моль
ГТФ + АДФ ⇄ ГДФ + АТФ.
6. Превращение янтарной кислоты в фумаровую (дегидрирование), катализируемое сукцинатдегидрогеназой (кофермент – ФАД):
 G
= 0
G
= 0
7. Гидратация фумаровой кислоты под действием фумаратгидратазы с образованием яблочной кислоты (малата):
 G
= –3,77 кДж/моль
G
= –3,77 кДж/моль
8. Окисление яблочной кислоты до кетоформы ЩУК, катализируемое малатдегирогеназой:
 G
= 29,71 кДж/моль
G
= 29,71 кДж/моль
Суммарное уравнение цикла Кребса:
СН3–СОSКоА + 3НАД + ФАД + АДФ + Н3РО4
НSКоА + 3НАДН2 + ФАДН2 + АТФ + 2СО2.
Как видно, за 1 оборот цикла Кребса происходит полное окисление 1 молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД и ФАД), перешедшие в восстановленное состояние, должны снова и снова окисляться. Это окисление происходит в дыхательной цепи, локализованной в митохондриях.
Освобождающаяся в результате окисления ацетил-КоА энергия в значительной мере сосредоточивается в макроэргических связях АТФ. Из 4-х пар атомов Н три пары переносятся на систему транспорта электронов через НАД, при этом синтезируется по 3 молекулы АТФ, а всего – 9 молекул АТФ. Одна пара атомов Н попадает в дыхательную цепь через ФАД, в результате образуется 2 молекулы АТФ. Одна молекула АТФ синтезируется в ходе реакций цикла Кребса. Таким образом, при окислении 1 молекулы ацетил-КоА в цикле Кребса образуется 12 молекул АТФ.
