
- •Химическое отделение вятский государственный гуманитарный университет
- •М. А. Зайцев основы биохимии
- •Часть 2
- •6. Нуклеиновые кислоты
- •6.1. Химический состав нуклеиновых кислот
- •6.2. Молекулярная масса нуклеиновых кислот
- •6.3. Локализация в клетке днк и рнк. Виды днк и рнк
- •6.4. Строение структурных элементов нуклеиновых кислот
- •6.5.1. Первичная структура днк
- •Генетический код
- •6.5.2. Вторичная структура днк
- •6.5.3. Третичная структура днк
- •6.5.4. Свойства днк
- •6.5.4.1. Репликация (редупликация, самоудвоение) днк
- •6.5.4.2. Транскрипция (синтез рнк)
- •6.6.1. Первичная структура рнк
- •6.6.2. Вторичная структура рнк
- •6.6.3. Третичная структура рнк
- •6.6.4. Классы рнк
- •6.6.5. Синтез белка (трансляция)
- •7. Общие понятия об обмене веществ и энергии в организме
- •7.1. Основные этапы обмена веществ
- •1 Этап. Подготовительный
- •2 Этап. Превращение строительных блоков (мономеров) в более простые соединения
- •3 Этап. Цикл Кребса (цикл ди- и трикарбоновых кислот, цтк)
- •4 Этап. Окислительная цепь ферментов (дыхательная цепь)
- •7.2. Обмен энергии. Макроэргические соединения
- •8. Биологическое окисление
- •8.1. Функции биологического окисления
- •8.2. Типы биологического окисления
- •II. Окисление, сопряженное с фосфорилированием адф
- •6 Железосерных белков
- •9. Обмен углеводов
- •9.1. Переваривание и всасывание углеводов
- •9.2. Синтез гликогена
- •9.3. Распад гликогена и освобождение глюкозы (глюкогенез)
- •9.4. Превращения моносахаридов
- •9.4.1. Дихотомический путь распада глюкозы. Гликолиз
- •1. Фосфорилирование:
- •9.4.2. Обмен пировиноградной кислоты
- •9.4.3. Цикл три- и дикарбоновых кислот (цикл Кребса)
- •9.4.4. Энергетический эффект гликолитического расщепления 1 молекулы глюкозы и последующего окисления пвк до со2 и н2о
- •9.4.5. Апотомический путь распада глюкозо-6-фосфата (пентозный, или пентозофосфатный цикл окисления углеводов)
- •9.5. Общая схема распада углеводов
- •9.6. Синтез углеводов
- •10. Обмен белков
- •10.1. Переваривание белков
- •10.2. Превращения аминокислот в организме
- •10.2.1. Процессы гниения белков в кишечнике
- •10.2.2. Судьба всосавшихся аминокислот
- •10.2.3. Конечные продукты распада аминокислот
- •10.3. Новообразование аминокислот
- •11. Обмен липидов
- •11.1. Переваривание и всасывание липидов
- •11.2. Окисление жирных кислот
- •11.3. Распад глицерина
- •11.4. Биосинтез липидов
- •11.4.1. Синтез высших жирных кислот
- •11.4.2. Биосинтез триглицеридов
- •12. Взаимосвязь процессов обмена веществ
- •12.1. Взаимосвязь обменов нуклеиновых кислот и белков
- •12.2. Взаимосвязь обменов нуклеиновых кислот и углеводов
- •12.3. Взаимосвязь обмена белков и углеводов
- •12.4. Взаимосвязь обмена белков и липидов
- •12.5. Взаимосвязь обмена углеводов и липидов
- •13. Регуляция обмена веществ
- •I. Метаболитный уровень регуляции
- •II. Оперонный уровень регуляции
- •III. Клеточный уровень регуляции
- •IV. Организменный уровень регуляции
- •V. Уровень регуляции метаболизма в экосистемах (популяционный)
9.4. Превращения моносахаридов
Обмен моносахаридов, образовавшихся при распаде олиго- и полисахаридов, идет такими путями, что используются только фосфорные эфиры моносахаридов, свободные же монозы фосфорилируются. Фосфорилирование моносахаридов – обязательная реакция на пути их использования для нужд организма. Оно приводит к возникновению более реакционных, чем свободные моносахариды, фосфорных эфиров моносахаридов и поэтому часто рассматривается как реакция активирования. Фосфорилирование моносахаридов осуществляется при взаимодействии их с АТФ и ускоряется ферментами фосфотрансферазами (киназами).
Важнейшей особенностью фосфорных эфиров моносахаридов является их способность к изомеризации, что дает возможность перехода от одной гексозы или пентозы к другой, изомерной ей.
9.4.1. Дихотомический путь распада глюкозы. Гликолиз
Гликолиз – сложный ферментативный процесс превращения глюкозы, протекающий в тканях человека и животных без потребления кислорода.
Гликолиз является первым, а в анаэробных условиях основным этапом на пути использования глюкозы и других углеводов для обеспечения биоэнергетических потребностей живых организмов. Кроме того, на промежуточных стадиях гликолиза образуются трехуглеродные фрагменты, используемые для биосинтеза ряда веществ.
У ряда микроорганизмов процессами, аналогичными гликолизу, являются различные виды брожения.
Процесс гликолиза катализируется 11-ю ферментами и протекает в гиалоплазме клеток. Ниже приведены реакции гликолиза.
1. Фосфорилирование:
 G
= –16,74 кДж/моль
G
= –16,74 кДж/моль
глюкоза Г-6-Ф
Эта реакция связана с освобождением значительного количества свободной энергии системы, может считаться практически необратимым процессом и называется первой пусковой реакцией распада глюкозы.
2. Изомеризация Г-6-Ф во фруктозо-6-фосфат (Ф-6-Ф) при участии фермента гексозофосфатизомеразы (Г-6-Ф-изомеразы):
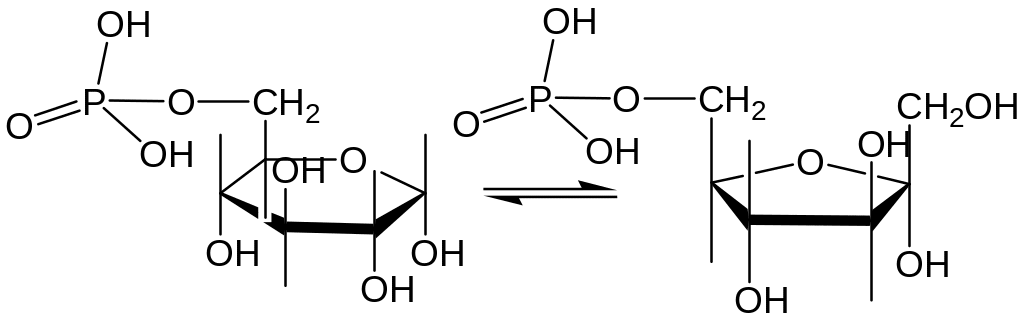 G
= 1,67 кДж/моль
G
= 1,67 кДж/моль
3. Фосфорилирование Ф-6-Ф во фруктозо-1,6-дифосфат (Ф-1,6-дФ) при участии фермента 6-фосфофруктокиназы:
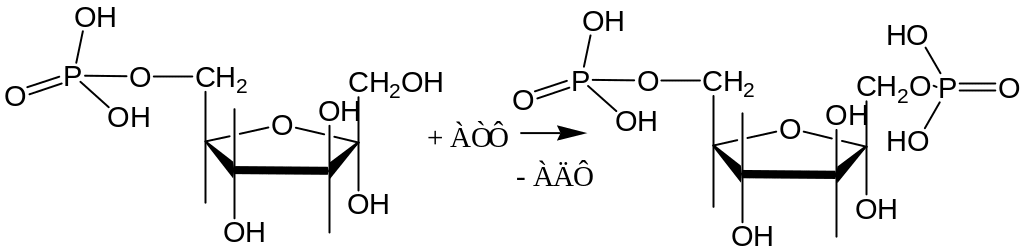 G
= –14,23 кДж/моль
G
= –14,23 кДж/моль
Данная реакция, также как и первая, практически необратима, протекает в присутствии ионов магния и называется второй пусковой реакцией гликолиза.
Фосфофруктокиназа ингибируется АТФ и стимулируется АДФ и АМФ. Так, в неработающей мышце концентрация АТФ высокая, а активность фосфофруктокиназы низкая. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению гликолиза.
4. Распад Ф-1,6-дФ на 2 фосфотриозы:
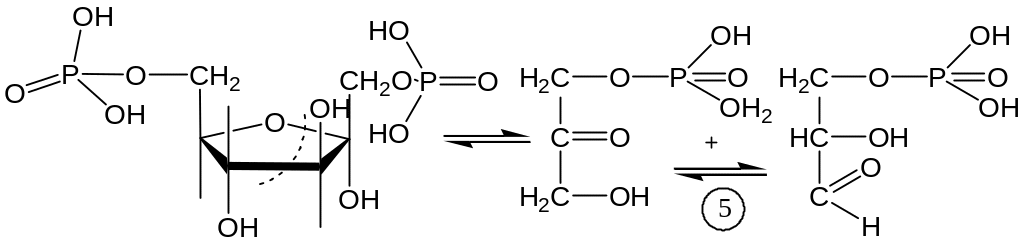
диоксиацетонфосфат 3-фосфоглицерино-
(ДОАФ) вый альдегид (3-ФГА)
G = 23,85 кДж/моль
Эту стадию катализирует фермент альдолаза.
5. Изомеризация триозофосфатов. Катализируется ферментом триозофосфатизомеразой. G = 7,53 кДж/моль. Равновесие данной реакции сдвинуто в сторону ДОАФ: 95% ДОАФ и около 5% 3-ФГА.
Однако в последующие реакции гликолиза может включаться только 3-ФГА. Вследствие этого по мере потребления 3-ФГА ДОАФ превращается в 3-ФГА.
Образованием 3-ФГА завершается первая стадия гликолиза. Вторая стадия включает окислительно-восстановительную реакцию, сопряженную с субстратным фосфорилированием, и является наиболее сложной и важной частью гликолиза.
6. Окисление 3-ФГА до 1,3-дифосфоглицериновой кислоты (1,3-дФГК):
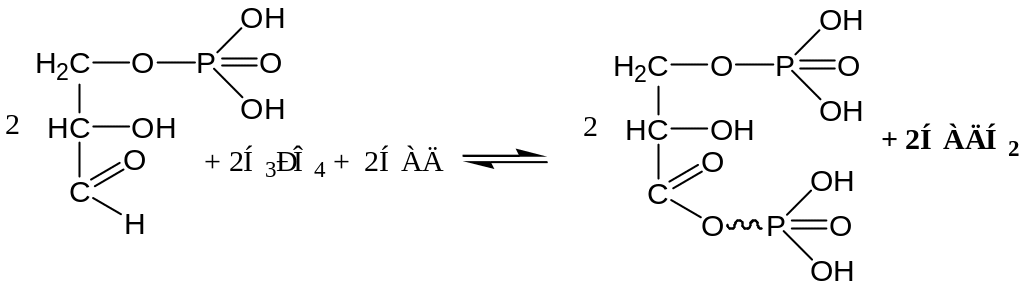
G = 6,28 кДж/моль
Фермент: глицеральдегид-3-фосфатдегидрогеназа (кофермент – НАД). 1,3-дФГК – макроэргическое соединение
7. Субстратное фосфорилирование – передача остатка фосфорной кислоты с 1,3-дФГК на АДФ с образованием АТФ:
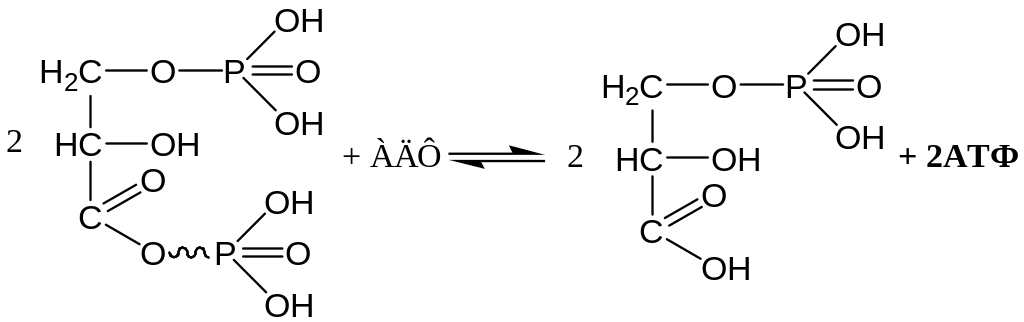
3-фосфоглицериновая кислота (3-ФГК)
G = –18,83 к/Дж моль
Фермент: фосфоглицераткиназа. Таким образом, энергия, высвобождающаяся при окислении альдегидной группы 3-ФГА до карбоксильной, запасается в форме энергии АТФ,
8. Изомеризация 3-ФГК в 2-фосфоглицериновую кислоту (2-ФГК) – внутримолекулярный перенос остатка фосфорной кислоты:
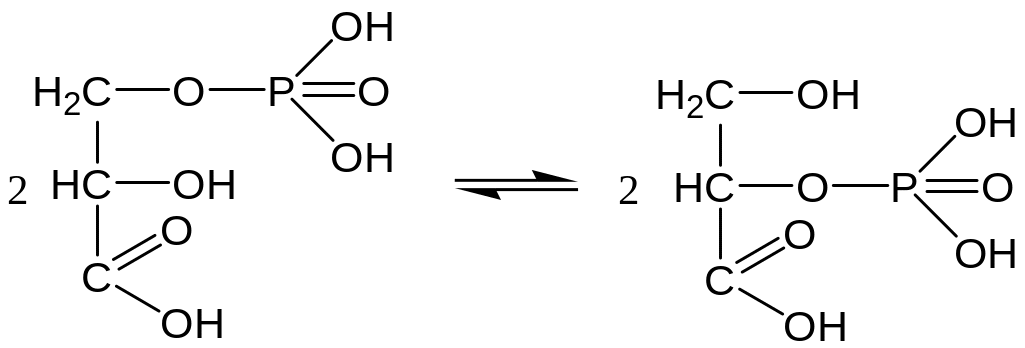 G
= 4,6 кДж/моль
G
= 4,6 кДж/моль
Фермент: фосфоглицерат-фосфомутаза. Реакция легко обратима, протекает в присутствии ионов магния.
9. Дегидратация 2-ФГК с образованием фосфоенолпировиноградной кислоты – макроэргического соединения:
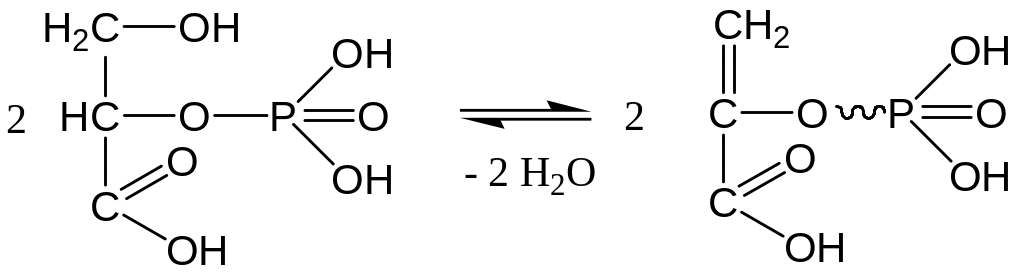 G
= 1,67 кДж/моль
G
= 1,67 кДж/моль
Фермент: енолаза, активируемая ионами Mg2+ или Mn2+ и ингибируемая F–.
10. Субстратное фосфорилирование – перенос остатка фосфорной кислоты с ФЕП на АДФ:
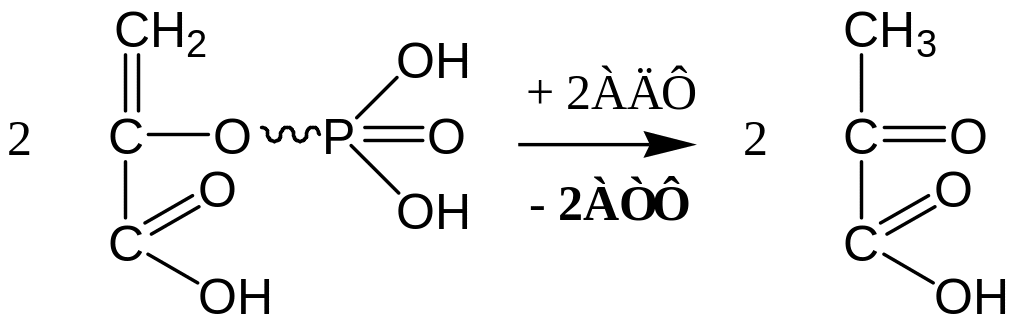 G
= –31,38 кДж/моль
G
= –31,38 кДж/моль
пировиноградная кислота (ПВК)
Фермент: пируваткиназа. Для ее действия необходимы ионы Mg2+ и Mn2+, а также ионы щелочных металлов (К+ или др.)
Суммарное уравнение гликолиза:
С6Н12О6 + 2НАД + 2АДФ + 2Н3РО4 2СН3–СО–СООН + 2НАДН2 + 2АТФ
6 АТФ (в дых. цепи)
8 АТФ
Биологическое значение процесса гликолиза заключается прежде всего в образовании макроэргических соединений. В первой стадии гликолиза затрачиваются 2 молекулы АТФ; во второй стадии образуются 4 молекулы АТФ. Таким образом, энергетическая эффективность гликолиза составляет 2 молекулы АТФ на 1 молекулу глюкозы.
