- •Федеральное агентство по образованию
- •Кафедра аналитической химии
- •Рентгенофазовый анализ Учебно-методическое пособие
- •Оглавление
- •6.1.2. Рфа смеси фаз известного состава. Картотека astm–jcpds-pdf 33
- •6.1.3. Рентгенометрические картотеки 34
- •Введение
- •Некоторые положения кристаллографии
- •1.1. Симметрия и ее элементы
- •1.2. Классы симметрии, решетки Браве
- •1.3. Пространственные группы
- •1.4. Символические обозначения плоскостей и направлений в кристалле. Индексы Миллера
- •2. Рентгеновские спектры и выбор излучения
- •2.1. Уравнение Вульфа – Брэгга
- •3. Интенсивность рентгеновских отражений
- •3.1. Шкалы интенсивности
- •3.2. Факторы, влияющие на интенсивность линий
- •3.3. Погрешности в определении интенсивности
- •3.4. Чувствительность метода рфа
- •4. Получение рентгенограмм
- •5. Промер рентгенограмм порошка
- •6. Рентгенофазовый анализ
- •6.1. Качественное определение состава смеси
- •6.1.1. Рфа при недоступности рентгенометрических характеристик анализируемых соединений
- •6.1.4. Рфа с помощью «указателей»
- •Рентгенометрические характеристики NaCl
- •Рентгенометрические характеристики uo2, GaP, CaF2
- •6.1.5. Пример качественного рфа
- •Рентгенометрические характеристики неизвестной смеси
- •Пример использования «ключа» для фазовой идентификации
- •Сопоставление рентгенометрических данных исследуемого образца, CaWo4 и wo3
- •6.1.6. Применение компьютерной техники для идентификации фаз
- •6.2. Количественный фазовый анализ
- •6.2.1. Метод подмешивания
- •6.2.2. Метод «гомологических» пар
- •6.2.3. Безэталонный метод
- •6.2.4. Метод с использованием т.Н. «корундового числа»
- •6.3. Идентификация соединений
- •7. Использование компЬЮтерной базы данных pdf
- •Литература
1.2. Классы симметрии, решетки Браве
Для кристалла, как уже упоминалось, характерна периодическая повторяемость расположения атомов, причем периоды повторяемости различны для разных направлений.
В кристаллической решетке параллельные переносы (трансляции) могут комбинироваться с макроскопическими элементами симметрии. Если, например, кристалл обладает какой-либо осью симметрии или плоскостью симметрии, то путем параллельного переноса их на период решетки возникает бесконечное множество таких параллельных между собой осей и соответственно плоскостей симметрии.
Сочетание трансляции и поворота около оси, совпадающей с направлением этой трансляции, приводит к новому элементу симметрии, который называется винтовой осью.
Аналогично, если точка решетки может быть совмещена с другой путем сочетания трансляции этой точки и отражения ее от плоскости, параллельной направлению трансляции, то возникает соответствующий элемент симметрии, называемый плоскостью зеркального скольжения.
Различные кристаллы могут обладать несколькими элементами симметрии. Элементы симметрии могу комбинироваться в кристаллах. Однако, как было показано А.В. Гадолиным в 1867 г., существует всего 32 возможные комбинации элементов симметрии. Каждая из комбинаций элементов симметрии образует класс симметрии.
Все кристаллы могут относиться только к одному из 32 классов симметрии. Так, например, кристаллы, с одной осью симметрии, образуют пять классов симметрии, соответствующих пяти порядкам этих осей, включая и ось первого порядка, когда симметрия отсутствует. Четыре класса образуют кристаллы, содержащие кроме одной оси симметрии и перпендикулярные к ней оси второго порядка. При этом отдельный класс симметрии образуют кристаллы, обладающие только центром симметрии.
В кристаллографии принято объединять указанные 32 класса симметрии в 7 систем симметрии (или сингоний), которые носят следующие названия в порядке возрастания симметрии [1,2]:
триклинная система, объединяющая 2 класса симметрии;
моноклинная система, куда входят 3 класса;
ромбическая система; также с 3 классами симметрии;
тригональная система, объединяет 7 классов;
гексагональная система — 5;
тетрагональная система с 7 классами;
кубическая система, наиболее симметричная, объединяет 5 классов.
Совокупность, эквивалентных узлов решетки, которые могут быть совмещены друг с другом только путем трансляции, образует так называемую трансляционную решетку, или решетку Браве кристалла, принимаемую в качестве элементарной.
|
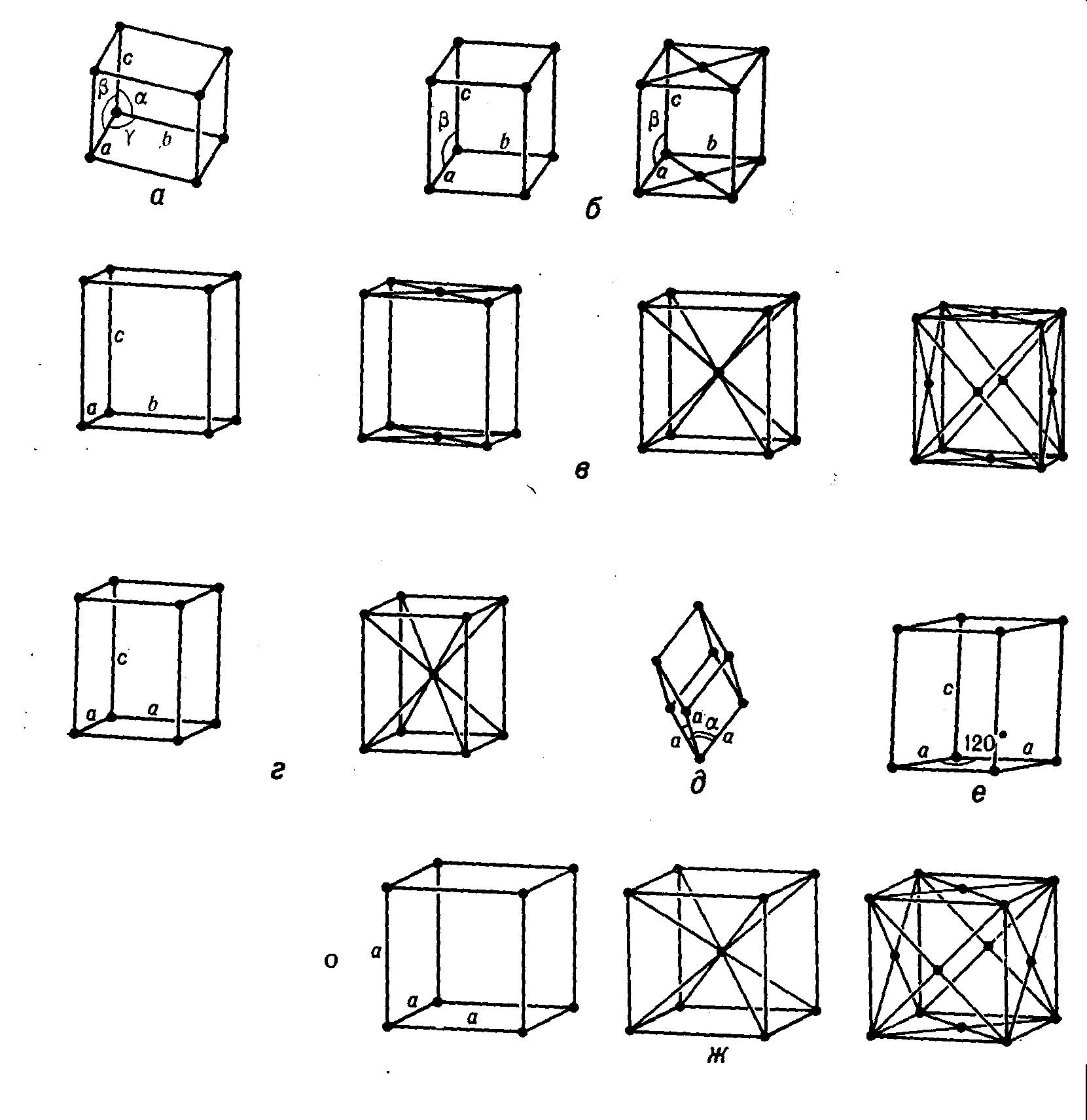
|
Рис.4. Решетки Браве. а триклинная, б моноклинная (примитивная и базоцентрированная), в ромбическая (примитивная, базоцентрированная, объемноцентрированная, гранецентрированная), г тетрагональная (примитивная, объемноцентрированная, д ромбоэдрическая, е гексагональная, жкубическая (примитивная, объемноцентрированная и гранецентрированная). |
|
Параметры элементарной ячейки обозначаются символами a, b, c, а углы , , . В табл. 1 представлены все такие решетки.
Из рис.4 следует, что решетка Браве представляет собой параллелепипед, построенный путем параллельного переноса какого-нибудь из узлов решетки по трем направлениям. В качестве координатных осей выбирают направления, параллельные осям симметрии кристалла или перпендикулярные к его плоскостям симметрии (такие направления обычно называют кристаллографическими осями). В параллелепипедах повторяемости эквивалентные узлы (атомы) могут располагаться не только в вершинах, но и в центре граней, ив центре диагональной плоскости. В первом случае решетка Браве называется гранецентрированной, во втором - объемноцентрированной.
Таблица 1.
Решетки Браве
Система |
Соотношение параметров элементарной ячейки |
Тип центрирования |
Триклинная |
a ≠ b ≠ c, ≠ ≠ ≠90 |
Примитивная |
Моноклинная |
a ≠ b ≠ c, = =90, ≠90 |
Примитивная |
Базоцентрированная |
||
Ромбическая |
a ≠ b ≠ c, = = =90 |
Примитивная |
Объемноцентрированная |
||
Базоцентрированная |
||
Гранецентрированная |
||
Ромбоэдрическая |
a = b= c, ≠90, = |
Примитивная |
Гексагональная |
a = b ≠ c, = =90, =120 |
Примитивная |
Тетрагональная |
a = b ≠ c, = = =90 |
Примитивная |
Объемноцентрированная |
||
Кубическая |
a = b = c, = = =90 |
Примитивная |
Объемноцентрированная |
||
Гранеценрированная |
|
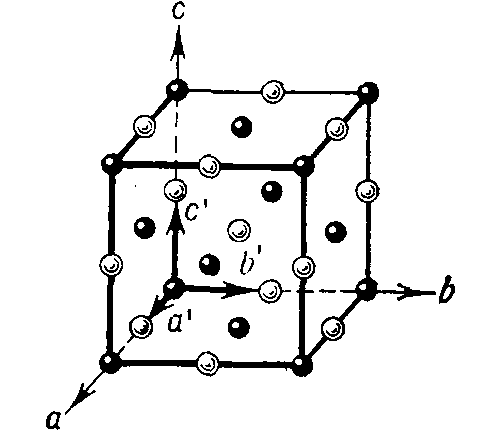
|
Рис.5. Структура типа NaCl |
Решетка Браве строится для определенного узла кристаллической решетки путем параллельного переноса его по трем кристаллографическим осям. Если выбрать в качестве исходного другой какой-нибудь узел (атом), получим другую решетку. Отсюда следует, что кристаллические решетки могут быть представлены системой из нескольких вложенных друг в друга решеток. Так, например, кристаллическая решетка поваренной соли NaCl состоит из двух подрешеток (рис. 5) соответственно тому, что ионы Na (черные кружки) и ионы Сl (белые кружки) каждый по отдельности образуют кубическую решетку. Обе эти решетки смещены относительно друг друга на половину ребра куба.