- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
3.1.2 Математическое описание избыточной свободной энергии лабильной
системы23
Свободная энергия любой системы в окрестности точки (Т,р), в которой свободная энергия есть G0, записывается при использовании разложения в ряд Тейлора при ограничении только квадратичными членами следующим образом:
G = G0 + Gpδp + GT δT + Gξδξ + ½(Gppδp2 + 2GTp δpδT + GTTδT2 + Gξξδξ2 + 2Gξpδξδp + 2GξTδξδT).
Все изменения «δ» могут быть сколь угодно малыми.
Из принятых определений следует, что во всех точках этой области, кроме точки (Tgpg)
ΔG = Gdξ=0 – GA=0 ˃ 0.
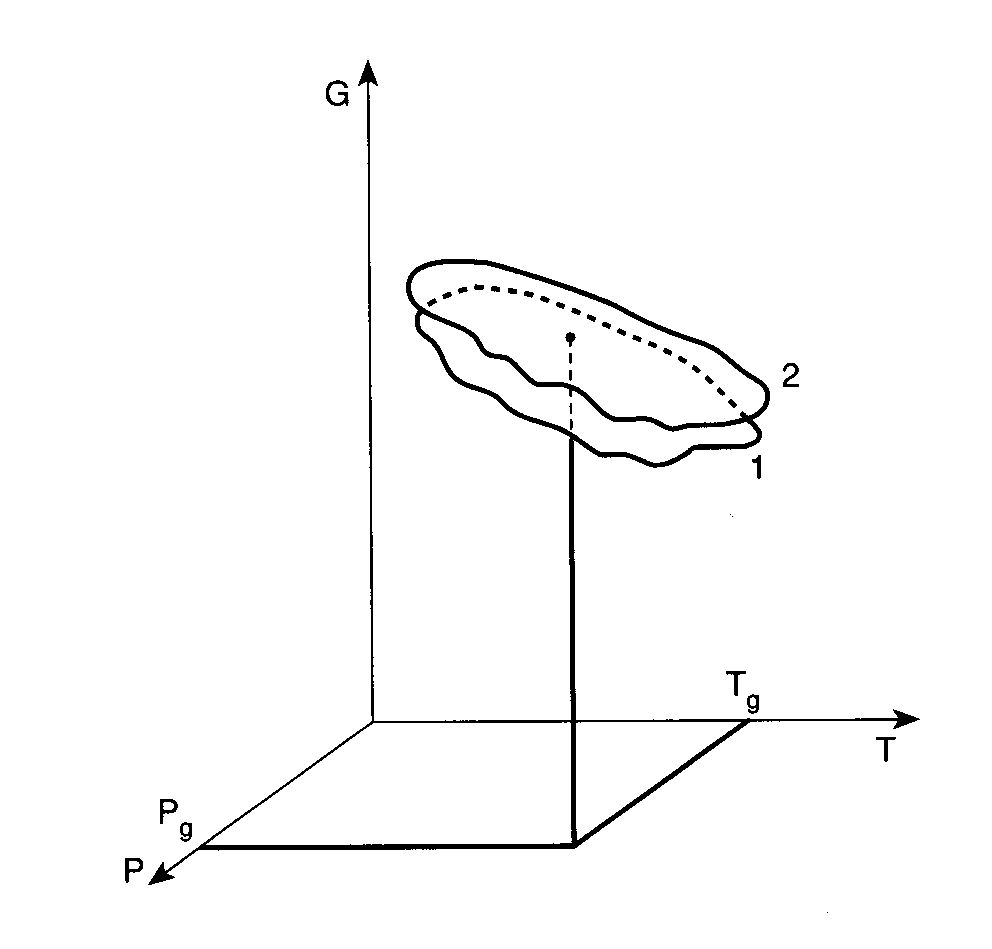
Это соответствует тому, что поверхность свободной энергии, соответствующая состоянию с постоянной структурой (т.е стеклу, dξ=0), касается по крайней мере в одной точке поверхности свободной энергии равновесного состояния, то есть метастабильной жидкости (A=0) . Поверхность «стекла» находится выше поверхности равновесного состояния. Этот случай показан на рис. 33.
|
Рис. 33 Соприкосновение поверхностей свободной энергии стеклообразующей жидкости (1) и стекла(2) в точке стеклования. |
При температуре стеклования, рассматриваемой как точка, энтропия, свободная энергия и энтальпия обоих состояний совпадают. Только в окрестности этой точки, в которой возникает состояние стекла, они становятся различными. Причиной этого различия (в частности, причина возникновения «зазора», показанного на рис. 33) становится различие вторых производных термодинамического потенциала для стекла и для жидкости.
Таким образом, величина зазора между этими поверхностями (избыток свободной энергии стекла по сравнению с метастабильной жидкостью при той же температуре) функционально определена только слагаемыми в записи свободной энергии, в которые входят вторые производные свободной энергии стекла и жидкости.
3.1.3 Математическое условие стеклования, налагаемое на изменения
вторых производных термодинамического потенциала в точке
стеклования
Опуская математические детали рассмотрения, приведем первый вывод, касающийся того, как влияет структура жидкости на температуру стеклования.
Оказывается, что изменение давления стеклования при изменении температуры стеклования зависит только от свойств равновесной жидкости в точке стекловании. Это обозначает, что стеклование не является фазовым переходом ни I, ни II рода, это чисто кинетический процесс. Поверхность свободной энергии, соответствующая стеклу, «рождается» из хотя бы одной точки соприкосновения её с поверхностью свободной энергии жидкости за счёт различия вторых производных. Эта точка принадлежит жидкости.
Второй важнейший вывод определяет знаки изменения термодинамических коэффициентов при стекловании. Поскольку обе поверхности касаются друг друга по крайней мере в одной точке (Tg,pg), математическое условие такого случая сформулировано в теории детерминантов. Это условие состоит в обязательной положительности диагональных членов определителя (матрицы или якобиана), построенной на вторых производных анализируемой функции в точке стеклования, когда А =0. В нашем случае эта матрица выглядит так:

∂2(δ(ΔG))/∂T2 ∂2(δ(ΔG))/∂T∂p ∂2(δ(ΔG))/∂T∂ξ
J = ∂2(δ(ΔG))/∂p∂T ∂2(δ(ΔG))/∂p2 ∂2(δ(ΔG))/∂p∂ξ ˃ 0, или
∂2(δ(ΔG))/∂ξ∂T ∂2(δ(ΔG))/∂ξ∂p ∂2(δ(ΔG))/∂ξ 2


-GξT (∂ξ/∂T)p,A=0 -GξT(∂ξ/∂p)T,A=0 -GξT
J = -Gξp (∂ξ/∂T)T,A=0 -Gξp(∂ξ/∂p)T,A=0 -Gξp ˃ 0.
-GξT -Gξp -Gξξ
Раскрывая смысл вторых производных, получаем
-GξT (∂ξ/∂T)p, A=0 = ΔСp/T ˃ 0,
- Gξp(∂ξ/∂p)T, A=0 = V·ΔκT, ˃ 0.
Знаки определены здесь тем, что состояние стекла, возникающее в результате несогласованной с давлением и температурой фиксацией ξ (в окрестности точки (Tg,pg)) неустойчиво, лабильно. Но знак -GξT(∂ξ/∂p)Т,A=0 = Δα может быть любым, поскольку этот коэффициент не является диагональным коэффициентом матрицы. Стеклование возможно как при уменьшении, так и при увеличении коэффициента объемного термического расширения24. Положительность коэффициента - Gξξ соответствует тому, что стеклование возможно только в вязких жидкостях (см. выше).