- •Специальные разделы оптического материаловедения
- •Термодинамика фазовых равновесий
- •1.1 Общие сведения о термодинамике
- •1 Предмет термодинамики1
- •1.1.2 Термодинамическая система, виды систем
- •Изолированные системы – те, которые не имеют возможности обмениваться веществом и энергией с окружением и имеющие постоянный объем.
- •1.1.3 Параметры состояния, параметры процессов
- •1.1.4 Функции состояния
- •1.1.5 Виды процессов
- •1.1.6 Внутренняя энергия, теплота и работа
- •1.1.7 Максимальная работа при изобарических, изотермических, адиабатических и изохорных процессах
- •1.2 Законы термодинамики
- •1.2.2 II закон термодинамики и энтропия как термодинамическая функция
- •1.2.3 Энтропия и термодинамическая вероятность. III закон термодинамики
- •Следствия Законов
- •1.2.5 Термодинамические функции, важные для материаловедения.
- •1.2.6 Применение термодинамических понятий в других областях науки
- •1.3 Производные термодинамических потенциалов и фазовые переходы
- •1.3.1 Первые производные термодинамических потенциалов, их физический
- •1.3.2 Вторые производные термодинамических потенциалов (соотношения
- •1.3.3 Фазовые переходы I и II рода.
- •1.3.4 Фазовые переходы I рода. Барическая зависимость фазовых переходов I рода:
- •1.4 Теория фазовых равновесий
- •1.4.1 Понятия «фазовые равновесия», «компонент», «диаграмма состояний»,
- •1.4.2 Понятие химического потенциала. Условия равновесия фаз. Правило фаз
- •1.4.3 Диаграмма состояний однокомпонентной системы
- •1.4.5 Эвтектики (двухкомпонентные системы). Линии ликвидуса и солидуса.
- •1.4.6 Твердые растворы (двухкомпонентные системы). Значение твердых
- •1.4.7 Ограниченные твердые растворы
- •1.4.8 Упорядочение твердых растворов
- •1.4.9 Полная несмешиваемость в жидком и в твердом состояниях
- •1.4.10 Системы с расслаиванием в жидком состоянии. Стабильное и
- •1.4.11 Системы с образованием химических соединений (двухкомпонентные
- •1.4.12 Системы с образованием химических соединений (двухкомпонентные
- •1.4.13 Трёхкомпонентные системы (принципы изображения,
- •1.4.14 Комбинация элементов диаграмм состояний. Физико-химический анализ.
- •2. Фазовые переходы и кинетическая теория стеклования
- •2.1 Стеклование
- •2.1.1 Принципиальная особенность фазовых переходов I и II рода в общей
- •2.1.2 Природа взаимодействия в конденсированных системах (общие
- •Ионное взаимодействие
- •Взаимодействие в металлах
- •Ковалентное взаимодействие
- •Водородные связи
- •Взаимодействие Ван-дер-Ваальса
- •Энергия химических связей
- •2.1.3 Основные особенности строения жидкостей и принцип их обобщенного
- •2.1.4 Общие сведения о релаксационных процессах как о процессах перехода от
- •2.1.5 Равновесные и мгновенные свойства жидкостей
- •2.1.6 Переохлажденные жидкости как частный случай метастабильного
- •2.1.7 Проявление стеклования на свойствах жидкостей
- •2.1.8 Определение стеклообразного состояния как лабильного (абсолютно
- •2.1.9 Математическое описание стеклования в кинетической теории. Твердо- и
- •2.1.10 Время релаксации структуры и его зависимость от температуры.
- •2.1.11 Соотношение температур стеклования и плавления (правило «2/3»
- •2.2 Кристаллизация расплавов стекол
- •2.2.1 Термодинамические особенности метастабильной жидкости
- •2.2.2 Работа образования зародыша кристаллизации20
- •2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
- •Б) скорость роста и кривая роста.
- •2.2.4 Методы изучения кристаллизационной способности и её
- •А) политермический метод и диаграммы кристаллизационной способности
- •Б) фазовый состав и морфология кристаллов.
- •В) дифференциальный термический анализ.
- •Г) скорость кристаллизации
- •2.2.5 Типы кристаллизации
- •2.2.6 Катализированная кристаллизация; ситаллы
- •2.2.7 Связь кристаллизационной способности с диаграммой состояния
- •3.Термодинамика стеклообразного состояния
- •3.1.1 Термодинамические переменные, используемые при математическом
- •3.1.2 Математическое описание избыточной свободной энергии лабильной
- •3.1.3 Математическое условие стеклования, налагаемое на изменения
- •3.1.4 Соотношение Пригожина-Дефея и его экспериментальная проверка
- •3.1.5 Термодинамический инвариант стеклообразного состояния
- •3.1.6 Следствия, вытекающие из соотношений термодинамики
2.2.2 Работа образования зародыша кристаллизации20
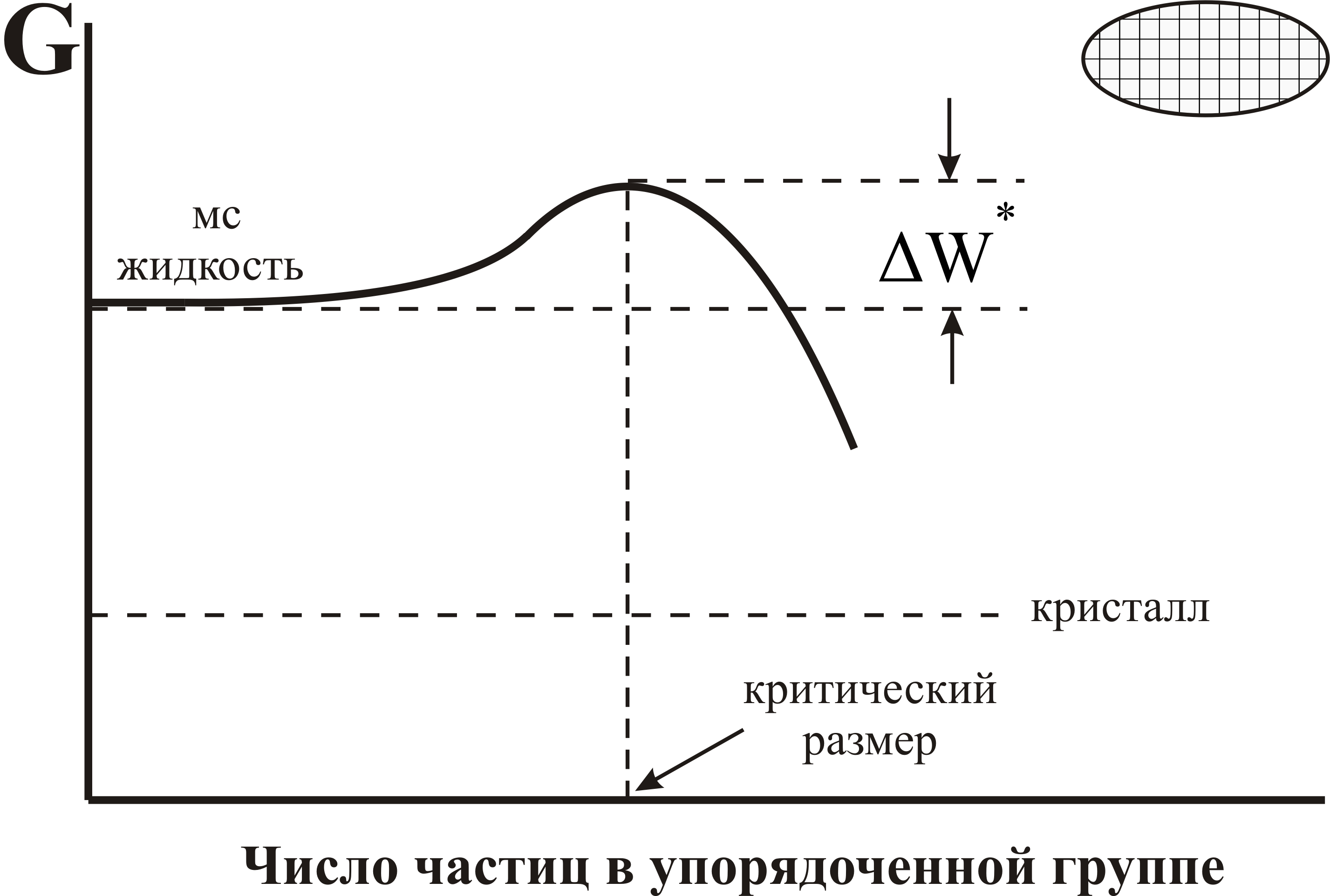
Пусть температура постоянна и жидкость переохлаждена. В структуре жидкости при случайных флуктуационных процессах может происходить кристаллоподобное упорядочение. При этом могут образовываться малые области, внутри которых атомы (молекулы) расположены так же как в кристалле (справа наверху на рис. 30).
|
Рис. 30. Изменение свободной энергии системы при образовании и росте зародыша кристаллизации. Пояснения см. в тексте. |
Вокруг этой области - жидкость и, поскольку структура жидкости и кристалла несовместимы, на границе между «зародышем» и жидкостью существует поверхностное натяжение. Работа по созданию этой поверхности растет по мере увеличения размера зародыша. При малых размерах она ничтожно мала и уровень энергии такой системы очень мало отличается от величины свободной энергии жидкости, не содержащей зародыша (рис. 30). Однако развитие поверхности приводит к увеличению свободной энергии (затрата работы на создание поверхности). Затем выигрыш свободной энергии внутри зародыша (упорядоченное расположение выгоднее энергетически) снижает затраты энергии на образование поверхности раздела и при дальнейшем росте числа частиц в зародыше свободная энергия начинает снижаться и этот процесс прогрессирует. Далее зародыш спонтанно растет и превращается в равновесный кристалл. Работа ∆W*, соответствующая достижению зародышем критического размера (рис. 30), называется термодинамическим барьером образования зародыша (нуклеации). Теория позволяет дать приближенный расчет величины ∆W* по формуле:
∆W*
=
 .
.
Здесь К – фактор формы зародыша. В случае
сферической формы К =
![]() .
V здесь объем г-атома
(моля) кристалла. ∆G =
∆G(мсж-к) тоже относится
к молю частиц. σ – коэффициент
поверхностного натяжения (граница
«кристалл-жидкость»). Зародыши критического
размера при дальнейшем росте вырастают
в стабильный кристалл. Зародыши размером
менее критического могут либо расти до
критического размера, либо рассасываться,
исчезать. Таким образом, рост кристаллов
возможен только из зародышей критического
размера.
.
V здесь объем г-атома
(моля) кристалла. ∆G =
∆G(мсж-к) тоже относится
к молю частиц. σ – коэффициент
поверхностного натяжения (граница
«кристалл-жидкость»). Зародыши критического
размера при дальнейшем росте вырастают
в стабильный кристалл. Зародыши размером
менее критического могут либо расти до
критического размера, либо рассасываться,
исчезать. Таким образом, рост кристаллов
возможен только из зародышей критического
размера.
2.2.3 Кривые Таммана а) скорость зарождения и кривая зарождения.
Скорость зарождения I
соответствует числу зародышей, достигших
критического размера, в единице объема
за единицу времени. Она определена
произведением числа частиц в единице
объема n и частоты
термических колебаний ν: чем более
плотно расположены частицы в расплаве,
тем более вероятно их «слипание» в
некотором сочетании друг с другом, само
«слипание» происходит в моменты сближения
частиц при их естественных (термических)
движениях. Но эти случаи только вероятны:
«слипание» приведет к образованию
зародыша критических размеров, если
в расчет ввести вероятность такого
события [exp(-NA∆W*/RT)].
Частицы подойдут друг к другу, если
учесть вероятность их смещения. Смещение
лимитируется вязким течением, поэтому
появляется вероятность [exp(-![]() ].
В окончательном виде эта формула для
I содержит много
сомножителей и две экспоненты:
].
В окончательном виде эта формула для
I содержит много
сомножителей и две экспоненты:
I =
n∙ν∙exp(-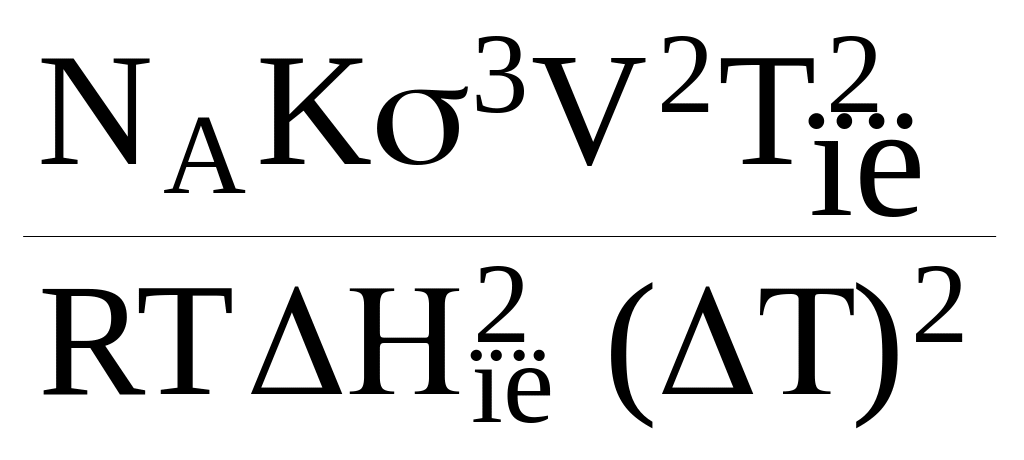 )∙exp(-
)∙exp(-
![]() )
.
)
.
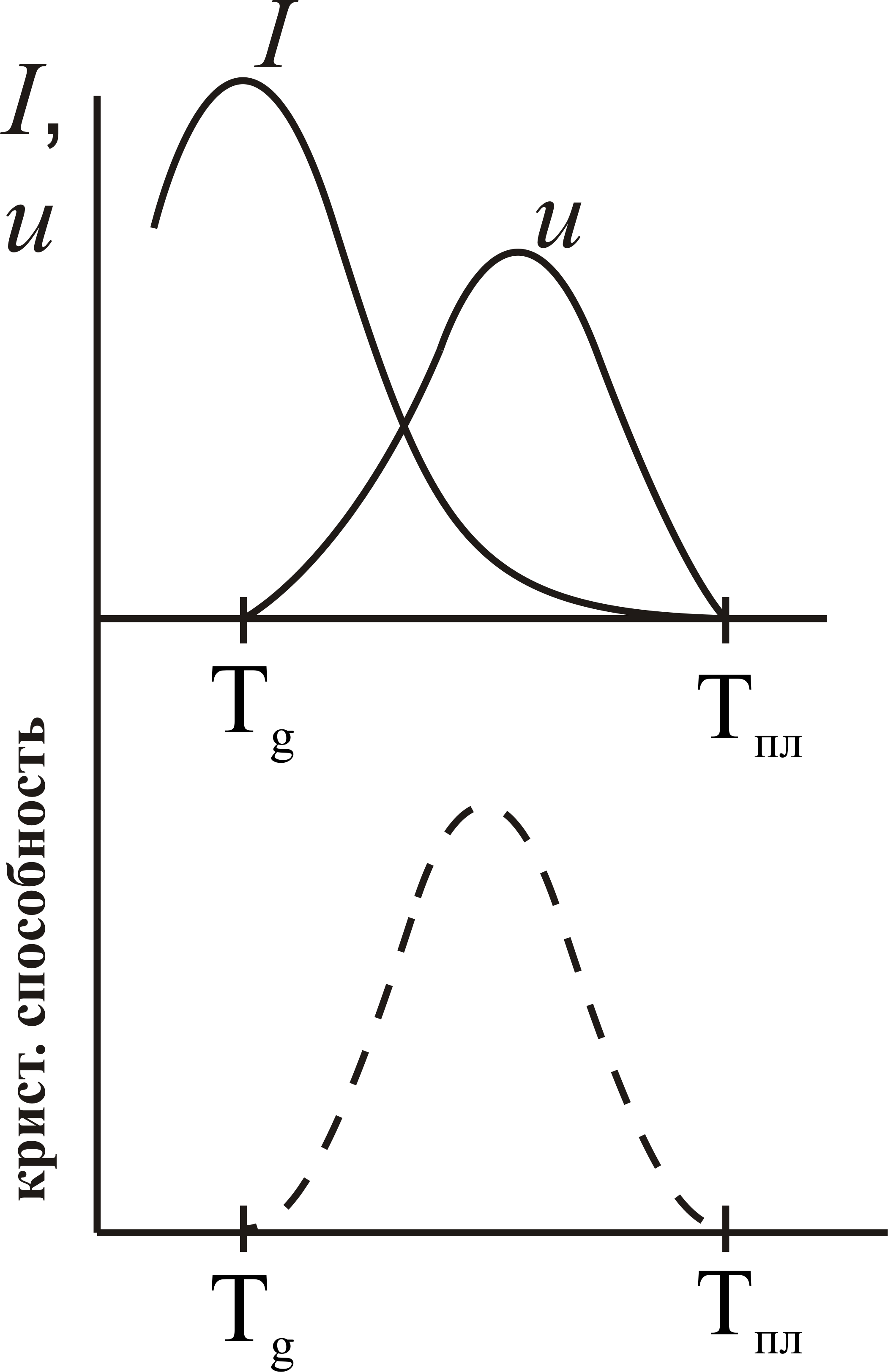
Сложное влияние каждого сомножителя приводит к возрастанию I с переохлаждением. В области Tg скорость зародышеобразования достигает максимума и затем падает (рис.31, кривая I). При Т≥Тпл зародыши не образуются.
|
Рис. 31. Кривые Таммана (наверху) и суммарная характеристика кристаллизационной способности (внизу). Пояснения см. в тексте. |
Экспериментально скорость образования зародышей исследуют методом «проявления». Образец выдерживают некоторое время при заданной температуре, затем быстро переводят к более высокой температуре, когда все образовавшиеся зародыши начинают быстро расти (появление). Образец закаляют и под микроскопом подсчитывают число кристаллов. Потом производят пересчет их числа на единицу объема, полагая, что число кристалликов соответствует числу зародышей, образовавшихся за время низкотемпературной экспозиции расплава.