
- •Биохимия
- •Химический состав живых организмов.
- •Химические вещества в живых организмах.
- •Неорганические вещества клетки
- •Функции воды
- •Неорганические соли
- •Роль солей в организме.
- •Органические вещества клетки.
- •Углеводы.
- •Химические свойства моносахаридов. Реакции по карбонильной группе
- •2. Восстановление.
- •Реакции по гидроксильным группам
- •Реакции брожения.
- •Олигосахариды. Полисахариды.
- •Строение дисахаридов.
- •Полисахариды.
- •Крахмал.
- •Амилаза и Амилопектин – две фракции крахмала.
- •Химические свойства полисахаридов:
- •Целлюлоза.
- •Химические свойства целлюлозы:
- •Липиды.
- •Простагландины.
- •Физические свойства липидов.
- •Функции жиров в организме:
- •Нуклеиновые кислоты
- •Биологически важные гетероциклические соединения
- •Кислотно-основные свойства гетероциклов
- •Строение мононуклеотидов
- •Название нуклеозидов и мононуклеотидов
- •Первичная структура днк
- •Вторичная структура днк
- •Структура рнк
- •Белки аминокислотный состав белков
- •Структуры белков первичная
- •Вторичная
- •Третичная
- •Свойства белков электрические
- •Денатурация белка
- •Функции белков в клетке
- •Физические и химические свойства
- •Химические свойства
- •Качественные реакции на белки
- •Биокатализ
- •2 Класс: Трансферазы
- •3 Класс (Гидролазы)
- •4 Класс: Лиазы
- •5 Класс: Изомеразы
- •6 Класс: Лигазы (синтетазы)
- •Номенклатура ферментов
- •Кофакторы
- •Водорастворимые
- •Жирорастворимые
- •I. Коферменты, входящие в состав оксиредуктаз (коферменты дегидрогеназ)
- •I.2.Флавиновые дегидрогеназы
- •I.4. Группа гемма
- •II. Коферменты переноса групп (трансферазы)
- •II.1. Аминотрансферазы.
- •Ацилтрансферазы
- •Основы кинетики ферментативных реакций Зависимость скорости ферментативной реакции от концентрации реагентов
- •Влияние температуры на скорость ферментативных реакций
- •Влияние рН на скорость ферментативной реакции
- •Ингибиторы ферментов
- •Динамическая биохимия
- •Катаболизм Специфические и общие пути катаболизма.
- •Катаболизм углеводов
- •Катаболизм липидов
- •Катаболизм белков
- •Катаболизм аминокислот.
- •Общий путь катаболизма.
- •Цпэ. Тканевое дыхание. Окислительное фосфорилирование.
- •Биосинтезы Биосинтез днк. Репликация.
- •Биосинтез рнк
- •Информационные рнк
- •Рибосомные рнк
- •Трансляция (биосинтез белка)
- •Биосинтез углеводов
- •Биосинтез гликогена
- •Биосинтез жиров
- •Биосинтез жирных кислот.
- •Биосинтез триацилглицеридов
- •Оглавление
Общий путь катаболизма.
Специфические катаболические пути углеводов, жиров, белков в дальнейшем объединяются в цикле трикарбоновых кислот.
Общим метаболитом является пировиноградная кислота, дальнейшее окисление которой приводит к выделению углекислого газа и воды. Если бы пировиноградная кислота сгорала в колориметрической бомбе, то
![]()
В живой клетке эта энергия извлекается в результате окисления путем дегидрирования и первая стадия на общем пути катаболизма является окислительное декарбоксилирование пирувата. В результате этого процесса пировиноградная кислота превращается в ацетил КоА. В этом сложном превращении участвуют НАД+ и кофермент А:
![]()
![]()
Цикл Кребса (цикл трикарбоновых кислот).
Цикл Кребса представляет собой систему из замкнутых реакций, в результате которых образуются углекислый газ и вода, запасается небольшое количество энергии и образуется большое количество восстановленных коферментов, которые затем, с помощью переносчиков, попадают в дыхательную цепь и обуславливают там синтез АТФ в процессе окислительного фосфорилирования.
Таким образом, основной задачей цикла трикарбоновых кислот является окончательное окисление органических веществ и регенерация восстановленных коферментов. Кроме того, в цикле Кребса образуется ряд промежуточных продуктов, которые используются в качестве субстратов для биосинтеза важных соединений: аминокислот, парфиринов, глюкозы. Поэтому цикл трикарбоновых кислот является центральным типом метаболизма.
Цикл включает в себя девять реакций, в результате каждого цикла образуется две молекулы углекислого газа. Цикл действует в аэробных условиях.

Цпэ. Тканевое дыхание. Окислительное фосфорилирование.
После завершения цикла Кребса водород, отобранный от окисленных субстратов, находится в форме НАДН+Н+, то есть связан с коферментами дегидрогеназ. На следующем этапе происходит окисление восстановленных коферментов путем дегидрирования до воды, одновременно с этим за счет энергии окисления образуется АТФ. Эти окислительные процессы можно представить следующим образом:
S*Н2 + ½ О2 → S + H2О
Очевидно, что этот процесс по конечному результату сходен с реакцией горения водорода в кислороде:
Н 2
+ ½ О2
Н2О
ΔG0
= -100 кДж/моль
2
+ ½ О2
Н2О
ΔG0
= -100 кДж/моль
2 Н – 2е 2Н+
О 0 + 2е О-2
За счет этой энергии происходит синтез АТФ. Известно, что максимально полезная работа получается при полностью обратимом процессе, реальные же процессы всегда не обратимы, поэтому величина полезной работы будет тем больше, чем в большей степени процесс приближается к равновесному. Организм превращает в полезную работу приблизительно 40% той энергии, которая выделяется при окислении субстратов и достигается это постепенным переносом протонов и электронов от субстратов к молекулярному кислороду. Увеличение числа промежуточных стадий способствует приближению реального процесса к равновесному, весь процесс тканевого дыхания протекает в митохондриях клетки. Митохондрия имеет форму цилиндра с закругленными краями, количество митохондрий в клетках различно : от 100-2 тысяч, они имеют внутреннюю и наружную мембраны, разделенные межмембранным пространством. Внутренние мембраны образуют складки – это так называемые кристы, содержимое пространство, которое ограничено внутренней мембраной, называется матриксом. Внутренние и внешние мембраны отличаются по составу и функциям, так, внешние мембраны проницаемы для молекул с молекулярной массой до 5 тысяч, а проницаемость внутренних мембран ограничена, следовательно, состав матрикса и состав межмембранного пространства отличается. Матрикс на 50 % состоит из белков, а во внутренней мембране митохондрий встроен ферментный ансамбль дыхательной цепи, который называется цепью передачи электронов – ЦПЭ. Ансамбль состоит из трех жесткозакрепленных ферментных комплексов , первый ферментный комплекс состоит из дегидрогеназ с коферментом ФМН, который переносит водород с НАДН на ФМН и далее на кофермент Q (убихинон).
Н АДН
+ Н+
+ ФМН ФМН*Н2
+ НАД+
АДН
+ Н+
+ ФМН ФМН*Н2
+ НАД+
Ф МН*Н2 + Q ФМН + Q* Н2
Перенос водорода включает в себя много этапов, участвует ряд промежуточных переносчиков, разделяющих отдельно перенос электронов и протонов, в этом переносе участвуют цитохромы, представляющие собой гемопротеины. Атом железа в геммах цитохрома может менять валентность :
F
 e3+
+ e Fe2+
e3+
+ e Fe2+
Рис.: Сопряжение дыхания и синтеза АТР (окислительного фосфорилирования).
I – NADH – дегидрогеназа; II – сукцинатдегидрогеназа; III – OH2 – дегидрогеназа; IV - цитохромоксидаза; V – АТР – синтаза.
Н аружная
мембрана митохондрий
аружная
мембрана митохондрий
М

 ежмембранное
пространство
ежмембранное
пространство
 nH+ nH+ nH+
nH+ nH+ nH+





 +
+ ++ + +
+
+ ++ + +
В



 нутренняя 2e- Q
2e-
нутренняя 2e- Q
2e-
М ембрана 2e-
2e-
2e-
ембрана 2e-
2e-
2e-
Митохондрий








 NADH NAD+ Фумарат 1/2О2 Н2О
NADH NAD+ Фумарат 1/2О2 Н2О

 Сукцинат
V
Сукцинат
V
О

 ксалоацетат Малат
ADP
+ H3PO4
ксалоацетат Малат
ADP
+ H3PO4


 H+
H+
ATP


 АТР
АТР
Матрикс
АDP
П рисоединение электрона в такой структуре и его отдача вызывают изменение лишь электронной конфигурации атома металла, не затрагивая структуру белков. Цитохромы дыхательных путей обозначаются как: b, c1, с, a a3 и располагаются в цепи между убихиноном и кислородом: b c1 с a a3
К роме
железа, входящего в состав цитохромов,
в митохондриях имеются белки, содержащие
негемовое железо, их называют железосерными
белками. В них атомы железа связаны с
атомами серы боковых цистеиновых
остатков аминокислот:
роме
железа, входящего в состав цитохромов,
в митохондриях имеются белки, содержащие
негемовое железо, их называют железосерными
белками. В них атомы железа связаны с
атомами серы боковых цистеиновых
остатков аминокислот:
Fe


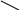
 цис
- S S – цис
цис
- S S – цис
 цис
- S S – цис
цис
- S S – цис
Железосерные белки входят в комплекс дыхательной цепи, выполняя роль простетической группы в процессе переноса электронов. Комплекс III, цитохромов b, c1 действует как QH2 - дегидрогеназа:
 QH2
+ 2с (Fe3+)
Q
+ 2Н+
+ 2с (Fe2+)
QH2
+ 2с (Fe3+)
Q
+ 2Н+
+ 2с (Fe2+)
Электроны последовательно проходят через атомы железа цитохромов b, c1 функционируют как Q∙H2 - дегидрогеназа, а протоны высвобождаются в раствор. Стехиометрический коэффициент 2 перед цитохромом с означает, что с QH2 передается 2 электрона, а цитохромы за один цикл могут передать только 1 электрон. Комплекс IV, действует как цитохромоксидаза, он помимо гемма содержит ионы меди, которые тоже участвуют в переносе электронов с цитохрома с на кислород, при этом электроны соединяются последовательно к ионам железа а1, а3, затем к меди, затем к кислороду. Кислород, поступающий в митохондрии из крови, связывается с атомом железа в цитохроме а3 в форме молекулы кислорода в молекулярном виде. Затем каждый из атомов молекулы кислорода последовательно присоединяет по два электрона и по два протона, превращаясь в молекулу воды. В дыхательной цепи имеется комплекс II, где осуществляется перенос электронов от сукцината, образующегося в цикле Кребса, направление потока электронов в дыхательной цепи при сопряжении одной окислительно-восстановительной системы с другой определяется их стандартными окислительно-восстановительными Red/Ox потенциалами. Эти величины для компонентов цепи и субстратов приведены в таблице, их величины:
КОМПОНЕНТ |
СИСТЕМА |
Е0, В |
|
НАД+/НАДН+Н+ |
-0,32 |
|
ФМН/ ФМН* Н2 |
-0,12 |
|
ФАД/ ФАД* Н2 |
-0,05 |
|
Q/ QH2 |
0,0 |
|
Цитохром b (Fe3+, Fe2+) |
0,07 |
|
Цитохром с1 (Fe3+, Fe2+) |
0,22 |
|
Цитохром с (Fe3+, Fe2+) |
0,26 |
|
Цитохром а (Fe3+, Fe2+) |
0,29 |
|
Цитохром а3 (Fe3+, Fe2+) |
0,55 |
|
½ О2/ Н2О |
0,82 |
|
Фумарат/ Сукцинат |
0,03 |
|
ЩУК/ Малеиновая кислота |
-0,17 |
|
Пируват/ Лактат |
-0,19 |
В связи с тем, что Red/Ox потенциалы определяют сродство к электрону, то для любых двух пар система с более положительным потенциалом будет стремиться принимать электроны и, как видно, в дыхательной цепи Red/Ox потенциалы переносчика электронов становятся более положительными. Поэтому, электроны передаются в дыхательной цепи внутри мембраны, а протоны высвобождаются в межмембранное пространство. Протоны необходимы для восстановления той ФМН, которая поступает из матрикса.
Таким образом, ЦПЭ работает как протонный насос, перекачивая ионы водорода из матрикса на наружную сторону мембраны, в результате , по разные стороны от внутренней мембраны возникает разность концентраций ионов водорода и одновременно разность потенциалов на поверхности. Следовательно, разность окислительно-восстановительных потенциалов трансформируется в энергию ΔµН+. Электрохимический потенциал заставляет протоны двигаться с наружной поверхности во внутреннюю, однако, мембраны в обратном направлении не проницаема для них, за исключением протонных каналов (V комплекс). В области этих каналов на внутренней поверхности внутренней мембраны располагается фермент Н+ АТФ-синтетаза, катализирующая синтез АТФ. Образующиеся молекулы, которые транспортируются из матрикса на наружную сторону мембраны и попадают в цитозоль. На синтез 1-ой молекулы АТФ, Δ Е0>0,2 В, требуется энергия не менее 31 кДж/моль, то есть в дыхательной цепи имеются 3 участка (I, III, IV), где высвобождение энергии достаточно для синтеза АТФ, следовательно, перенос пары электронов от НАДН в итоге дает нам образование 3-х молекул АТФ, а ФАД – 2-х молекул АТФ. Известно, что человек за сутки из воздуха потребляет приблизительно 67 литров (27 молей) кислорода, подавляющая его часть (90%) восстанавливается до воды при участии дыхательной цепи, за это же время в митохондриях синтезируется 62 кг АТФ, однако, содержание АТФ в организме составляет около 50 грамм, вследствие того, что каждая молекула АТФ расщепляется и регенерируется 2,5 тыс. раз в сутки, средняя продолжительность ее жизни меньше 1-ой минуты.
