
- •Биохимия
- •Химический состав живых организмов.
- •Химические вещества в живых организмах.
- •Неорганические вещества клетки
- •Функции воды
- •Неорганические соли
- •Роль солей в организме.
- •Органические вещества клетки.
- •Углеводы.
- •Химические свойства моносахаридов. Реакции по карбонильной группе
- •2. Восстановление.
- •Реакции по гидроксильным группам
- •Реакции брожения.
- •Олигосахариды. Полисахариды.
- •Строение дисахаридов.
- •Полисахариды.
- •Крахмал.
- •Амилаза и Амилопектин – две фракции крахмала.
- •Химические свойства полисахаридов:
- •Целлюлоза.
- •Химические свойства целлюлозы:
- •Липиды.
- •Простагландины.
- •Физические свойства липидов.
- •Функции жиров в организме:
- •Нуклеиновые кислоты
- •Биологически важные гетероциклические соединения
- •Кислотно-основные свойства гетероциклов
- •Строение мононуклеотидов
- •Название нуклеозидов и мононуклеотидов
- •Первичная структура днк
- •Вторичная структура днк
- •Структура рнк
- •Белки аминокислотный состав белков
- •Структуры белков первичная
- •Вторичная
- •Третичная
- •Свойства белков электрические
- •Денатурация белка
- •Функции белков в клетке
- •Физические и химические свойства
- •Химические свойства
- •Качественные реакции на белки
- •Биокатализ
- •2 Класс: Трансферазы
- •3 Класс (Гидролазы)
- •4 Класс: Лиазы
- •5 Класс: Изомеразы
- •6 Класс: Лигазы (синтетазы)
- •Номенклатура ферментов
- •Кофакторы
- •Водорастворимые
- •Жирорастворимые
- •I. Коферменты, входящие в состав оксиредуктаз (коферменты дегидрогеназ)
- •I.2.Флавиновые дегидрогеназы
- •I.4. Группа гемма
- •II. Коферменты переноса групп (трансферазы)
- •II.1. Аминотрансферазы.
- •Ацилтрансферазы
- •Основы кинетики ферментативных реакций Зависимость скорости ферментативной реакции от концентрации реагентов
- •Влияние температуры на скорость ферментативных реакций
- •Влияние рН на скорость ферментативной реакции
- •Ингибиторы ферментов
- •Динамическая биохимия
- •Катаболизм Специфические и общие пути катаболизма.
- •Катаболизм углеводов
- •Катаболизм липидов
- •Катаболизм белков
- •Катаболизм аминокислот.
- •Общий путь катаболизма.
- •Цпэ. Тканевое дыхание. Окислительное фосфорилирование.
- •Биосинтезы Биосинтез днк. Репликация.
- •Биосинтез рнк
- •Информационные рнк
- •Рибосомные рнк
- •Трансляция (биосинтез белка)
- •Биосинтез углеводов
- •Биосинтез гликогена
- •Биосинтез жиров
- •Биосинтез жирных кислот.
- •Биосинтез триацилглицеридов
- •Оглавление
Кофакторы
Различают две группы кофакторов – неорганические и органические. К первым относятся ионы металлов (Mg+2, Mn+2, Ca+2), а также некоторые неорганические анилоны (Cl-). Ионы двухвалентных металлов могут быть очень прочно связаны с белковой молекулой, выполняя роль простетической группы.
Органические кофакторы называются коферментами. Они, как правило, представляют собой небелковые вещества. Большинство коферментов не синтезируются в организме млекопитающих, и должны поступать с растительной пищей. Однако в организм поступают не сами коферменты, а их предшественники – витамины, являющиеся незаменимыми пищевыми факторами, которые в клетке модифицируются.
Витамины представляют собой очень разную в химическом отношении группу органических соединений, поэтому с точки зрения химической структуры им нельзя дать общего определения. Единственная классификация витаминов основана на их отношению к воде
Известно 13 витаминов:
Водорастворимые
ВИТАМИНЫ |
КОФЕРМЕНТЫ |
Тиамин (В1) |
Тиаминпирофосфат |
Рибофлавин (В2) |
Флавинмононуклеотид (флавиндинуклеотид) |
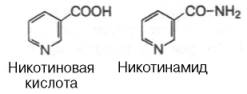
Никотиновая кислота (В5) |
Никотинамидадениннуклеотид |
Пантотеновая кислота (В3) |
Коэнзим (кофермент А) |
Пиридоксин (В6) |
Пиридоксальфосфат |
Биотин Н |
Биоцитин |
Аскорбиновая кислота |
Не известно |
Жирорастворимые
ВИТАМИНЫ |
КОФЕРМЕНТЫ |
Витамин А |
Ретинол |
Витамин Д |
Не известно |
Витамин Е |
Не известно |
Витамин К |
Не известно |
Общим для всех витаминов является их абсолютная необходимость для организмов в качестве составной части пищи дополнительно к белкам, жирам, углеводам и минеральным веществам. Поскольку они не синтезируются гетеротрофными организмами, то их недостаток сопровождается возникновением патологических явлений. В количественном отношении потребность в витаминах ничтожна: к 66 граммам сухих питательных веществ нужно 0,1-0,2 грамма витаминов. Отсюда ясно, что витамины в организме выполняют каталитические функции. Во многих случаях они являются составными частями ферментов, необходимыми для их функционирования.
К числу реакций, требующих участия коферментов, относятся окислительно-восстановительные реакции, реакции переноса групп, изомеризации, а также реакции, катализируемые лигазами (лигазозависимые). Без участия коферментов протекают реакции расщепления, например гидролитические реакции, катализируемые пищеварительными ферментами.
Ниже приведены важнейшие органические коферменты, их активные группы, тип реакции, в которой участвует кофермент, а также витамины, входящие в их состав.
I. Коферменты, входящие в состав оксиредуктаз (коферменты дегидрогеназ)
I.1. Дегидрогеназы, содержащие соединения никотинамида (НА), -
НАД (никотинамидадениндинуклеотид) и НАДФ никотинамидадениндинуклеотидфосфат). Это НАД- и НАДФ-зависимые дегидрогеназы. Они могут синтезироваться в организме человека из никотиновой кислоты и никотинамида, но в крайне ограниченном количестве.
Н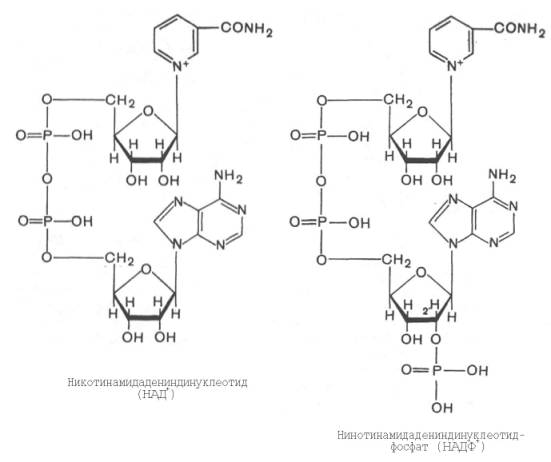 А
и никотиновую кислоту относят к витамину
РР. Ниже представлена общая схема
строения НАДФ и НАД :
А
и никотиновую кислоту относят к витамину
РР. Ниже представлена общая схема
строения НАДФ и НАД :
НАД и НАДФ являются коферментами ферментов в реакции дегидрирования.
НАДФ – является акцептором окисляемого вещества.
H H
H
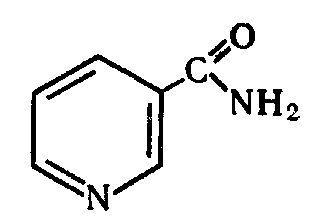



S H2 + S + + H+

R
R
Как видно из схемы присоединение водорода происходит таким образом, что один атом водорода субстрата присоединяется к атому водорода пиридинового кольца, а другой отдаёт свой электрон атому азота пиридинового кольца, а сам уже в виде иона переходит в раствор. При этом он может присоединяться к остатку фосфорной кислоты в молекуле кофермента НАДФ, который обычно в растворе ионизирован. Поэтому в уравнениях реакции Окисленный и восстановленный НАД изображают следующим образом:
SH2 + НАД+ S + НАДH + H+
НАД находится в цитозоле клетки в свободном состоянии и взаимодействует с ферментом только в момент реакции. В этом отношении он сходен с субстратами.
Дегидрогеназа с НАД катализирует следующие реакции:
а) дегидрирование гидроксильных групп, например реакцию окисления молочной кислоты лактатдегидрогеназой, в результате которой спиртовая группа окисляется до кето- группы
O
O
лактат
C
OH
OH
дегид.


лактат
пируват
б
O
O
H

C + НАД+ + HOPO3H2 1C-O-PO3H2
CH-OH 2CH-OH
C
1,3
дифосфорглицериновая кислота
В этом случае в молекулу вводится вторая фосфатная группа.
в) дегидрирование аминогрупп например, дегидрирование глутаминовой кислоты
O
O
OH
OH
иминная
связь
C
 C
C
C H-NH2 + НАД+ C=NH + НАДH + H+
CH2 CH2
C
глутамат
П
O
C-N- эта -C=N-
│
H OH
Такого же типа реакции катализируют дегидрогеназы, использующие в качестве коферментов НАДФ.
