
Литература от Абакумова ч2 / Осмотический массоперенос
.pdf
электрическим весам, которые позволяют непрерывно записывать изменение массы m на ленте самописца. Работа весов основана на компенсации измерения веса силой взаимодействия магнитного поля соленоида (L) и ферромагнитного сердечника (М). Магнитное поле соленоида регулируется фотоэлектрическим усилителем.
Рис. 1.15. Схема калориметрической установки: образец (1); калориметрический стакан (2); оболочка (3); водяная рубашка (4); поглотитель (5); датчик (6); усилители (7); блоки регулировки (8); самописцы (9)
Вопыте определяется величина тока в калориметрическом стакане J
искорость убыли влаги dm/dt. Теплота испарения на различных этапах
обезвоживания материала рассчитывается по формуле: Q =J2 R/(dm/dt), Дж/кг, где R — сопротивление нагревателя.
В течение опыта относительная влажность воздуха измеряется с помощью электрического датчика 6. В другой модифицированной установке применяется фронтальный газохроматографический метод с видоизмененной системой определения количества поглощенной влаги.
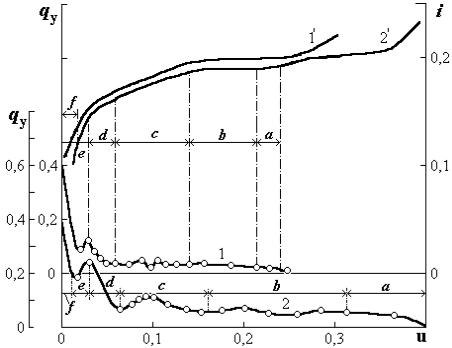
На рис. 1.16 приведены значения теплоты десорбции влаги из отмытого и очищенного от примесей кварцевого песка фракции меньше 170 мкм (кривая 1) и порошка кварцевого стекла с размерами зерен 50–63 мкм (кривая 2). Кривые 1 и 2 подобны, но порошок имеет большее влагосодержание, удельную поверхность и меньший размер макропор. В связи с этим, теплота испарения капиллярно-пленочной влаги у кварцевого порошка выше, чем у песка.
Под влагой в широких капиллярах понимается вода, заполняющая все пространство между зернами песка и кварца. Влага в узких капиллярах
— это вода, которая остается после испарения влаги из макропор между
31
контактирующими частицами. Она удерживается менисками. Пленочная влага образуется на поверхности зерен после удаления основной части поглощенной воды из пор. Она контактирует с менисками узких капилляров.
Удаление влаги из пористых тел происходит в строгой последовательности. Вначале она испаряется в широких капиллярах [15]. Затем испарение происходит из пленок и узких капилляров. Эта последовательность обусловлена тем, что для испарения влаги из меньших по размеру капилляров требуются большие удельные расходы тепла на испарение.
При избыточном насыщении влагой пор между твердыми частицами чистая теплота испарения равна нулю, так как испарение происходит со свободной поверхности воды.
По мере испарения влаги между частицами поверхностного слоя материала образуются мениски. Это вызывает увеличение чистой теплоты испарения (участок а кривых 1 и 2). По мере дальнейшего испарения влаги происходит обезвоживание крупных капилляров (участок b). При этом значения теплоты испарения остаются постоянными до тех пор, пока полностью не обезвоживались макропоры между твердыми частицами в тонком слое песка и кварца 1–2 мм.
Последующее испарение влаги из зазоров между частицами кварца сопровождается ростом значений qу (участок с). После обезвоживания мелких пор испарение происходит из толстых пленок жидкости и манжет-
|
ных |
менисков |
|
|
(участок d). Ис- |
||
|
парение влаги из |
||
|
пленок приводит |
||
|
при |
влажности |
|
|
около |
3% |
к |
|
уменьшению их |
||
|
толщины и |
раз- |
|
|
рыву. |
Остатки |
|
|
пленочной влаги |
||
|
стекают в |
ман- |
|
|
жеты |
между |
|
|
частицами. |
Это |
|
|
вызывает |
вре- |
|
|
менное увеличе- |
||
|
ние радиусов их |
||
Рис. 1.16. Зависимость чистой удельной теплоты де- |
менисков и |
со- |
|
ответственно |
|||
сорбции qу (МДж/кг) (1, 2) и интенсивности испарения |
снижение тепло- |
||
i 10–5 (кг/(м2 с) (1′, 2′) от влагосодержания u: кварцевый |
ты |
испарения |
|
песок фракции менее 170 мкм (1); молотый кварц с раз- |
(участок е |
кри- |
|
мерами зерен 50–63 мкм (2) |
вых 1 и 2). |
|
|
32 |
|
|
|
Значительный рост значений теплоты фазового перехода связан с удалением остатков манжетной и затем адсорбированной влаги (участок f). Кривые интенсивности сушки i (1′, 2′) также имеют сингулярные точки. Они соответствуют испарению влаги, имеющей различную энергию связи
сматериалом.
Вобразцах асбестоцементных изделий после 7 дней с момента изготовления имеется капиллярно-пленочная влага. Пленки воды находятся на поверхности нерастворившихся частиц цемента и асбестных волокон. Имеется также манжетная влага между частицами. Этапы удаления этой влаги подобны ее испарению из кварцевого порошка (рис. 1.16).
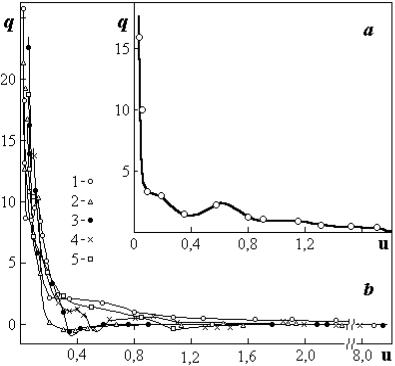
Зависимость теплоты десорбции из силикагеля КСК-3 с удельной поверхностью 340 м2/г приведена на рисунке 1.17а. При влагосодержании
u >0,6 происходит удаление пленок влаги на поверхности зерен силикагеля и связанными с ними манжетными менисками.
При влагосодержании u =0,6 имеется максимум. Он возникает из-за разрыва пленок и стекания их в манжеты. В диапазоне влагосодержаний 0,4–0,6 происходит испарение с менисков оставшейся манжетной влаги между зернами и затем из пор зерен силикагеля. При u <0,1 имеет место десорбция молекул воды, находящихся на активных центрах внутри микропор.
На рис. 1.17b и 1.18 приведены удельные теплоты испарения поглощенной влаги из торфа и других материалов. Большая часть кривых пред-
|
ставляет |
собой моно- |
||||
|
тонно |
|
убывающие |
|||
|
функции, |
стремящиеся |
||||
|
при |
больших |
влагосо- |
|||
|
держаниях |
к |
теплоте |
|||
|
испарения |
|
свободной |
|||
|
воды. Процесс испаре- |
|||||
|
ния влаги сопровожда- |
|||||
|
ется |
структурными |
и |
|||
|
физико-химическими |
|||||
|
превращениями |
систе- |
||||
|
мы сорбат–сорбент с |
|||||
|
выделением |
или |
по- |
|||
|
глощением |
тепла. |
В |
|||
|
случае лавсана, поли- |
|||||
|
стирола (рис. 1.18b) |
|||||
|
удаление воды способ- |
|||||
Рис. 1.17. Чистые теплоты десорбции влаги q, |
ствует, по-видимому, |
|||||
дальнейшей |
полимери- |
|||||
кДж/моль из a) силикагеля КСК-3, b) пяти об- |
зации имеющихся в ма- |
|||||
разцов торфа |
териале |
|
мономеров. |
|||
33 |
|
|
|
|
|
|
|
Эти процессы |
со- |
|||
|
провождаются |
по- |
|||
|
глощением тепла. |
||||
|
В |
|
цементе |
||
|
(рис. 1.18b, кривая |
||||
|
5) сразу после за- |
||||
|
меса |
по |
|
|
мере |
|
уменьшения |
коли- |
|||
|
чества |
влаги |
про- |
||
|
цессы растворения, |
||||
|
гидратации и обра- |
||||
|
зования |
из |
раство- |
||
|
ра новой |
кристал- |
|||
|
лической |
|
фазы |
||
|
проходят как с вы- |
||||
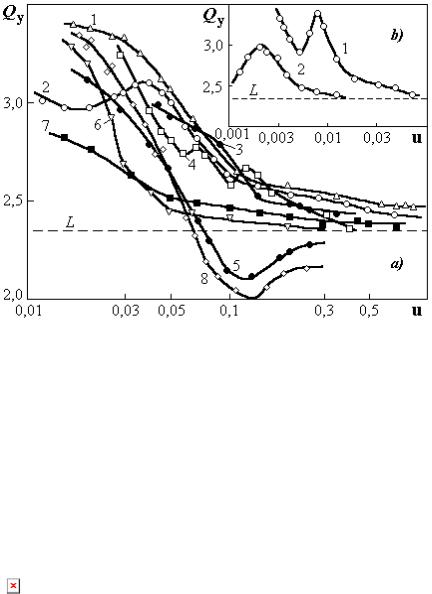
Рис. 1.18. Удельные теплоты испарения Qу (МДж/кг) при по- |
делением, так и по- |
||||
стоянной температуре 383 К из материалов различного влаго- |
глощением |
|
тепла. |
||
содержания u: а) биомасса «Биошрот» (1), целлюлоза (2), ио- |
При этом на опре- |
||||
нит ЭДЭ-10П (3), аминопласт (4), портландцемент марки 500 |
деленных |
|
этапах |
||
сразу после замеса (5), хлоркаучук (6), асбест марки П-6-65 |
десорбции |
|
инте- |
||
(7), нитрофоска (8); b) лавсан (1), полистирол (2) |
гральная |
теплота, |
|||
|
|||||
отнесенная к единице массы испаряемой воды, оказывается ниже скрытой теплоты парообразования чистой воды L. В образцах этого же цемента одного- и семисуточного «возраста» теплота испарения Qу >L во всем диапазоне влагосодержаний. Кривая 8 для нитрофоски подобна зависимости
Qу =ƒ(u) для цемента. |
Следует |
|
отме- |
||
|
|
|
|||
|
|
|
|||
|
|
тить, что теплоты де- |
|||
|
|
сорбции |
для |
биологи- |
|
|
|
ческой массы «Био- |
|||
|
|
шрот», |
целлюлозы и |
||
|
|
ионита за исключением |
|||
|
|
низких |
влагосодержа- |
||
|
|
ний близки. Это свиде- |
|||
|
|
тельствует о том, что |
|||
|
|
механизмы десорбции |
|||
|
|
осмотической |
и |
час- |
|
|
|
тично |
сорбированной |
||
|
|
влаги в них подобны. |
|||
Рис. 1.19. Чистая удельная теплота десорбции влаги qу, |
На рис. 1.19 при- |
||||
(МДж/кг) (1–3) и интенсивность испарения j 10–10 (кг/м2с) |
ведены |
зависимости |
|||
(1′–3′) из образцов асбестоцемента (1, 1′), 28 (2, 2′) и 37 |
чистой |
удельной |
теп- |
||
(3, 3′) суток выдержки |
лоты испарения |
влаги |
|||
34 |
|
|
|
|
|

qу из образцов асбестоцемента и скорости сушки через 7 (1), 28 (2) и 37 (3) дней после изготовления. В таких материалах волокна асбеста служат «арматурой», а цемент — связующим.
При замесе частицы цемента частично растворяются и появляются кристаллические новообразования. По мере их роста образуются фазовые контакты между частицами в виде системы «нитей», приводящие к увеличению прочности изделия.
С «возрастом» асбестоцементного изделия число фазовых контактов возрастает и создается пространственная сетчатая микропористая структура. Увеличивается также общая поверхность нитей и соответственно количество центров сорбции.
В области малых влагосодержаний (рис. 1.19, кривые 1–3) значения qу, больше величины Qу−L для цемента, приведенной на рис. 1.18 (кривая 5), а при u >0,05 близки к чистой теплоте десорбции для асбеста (кривая 7). При малом влагосодержании молекулы воды десорбцируются из микропористой структуры твердеющего связующего, а при большем влагосодержании — преимущественно из пористой структуры асбестных волокон.
В образцах асбестоцементных изделий (особенно после 7 дней с момента изготовления) имеется капиллярно-пленочная влага. Этапы удаления этой влаги подобны ее испарению с частиц кварца (рис. 1.16).
На рис. 1.20 приведены чистые калориметрические q (кривая 1) и изостерические q′ (кривая 2) теплоты испарения. Увеличение значений q и снижение энтропии Sa (кривая 5) при u =0,038 является результатом кон-
тракции системы целлюлоза—вода.
Образуются «водяные мостики» между функциональными группами соседних макромолекул. Энергия их связи с сорбентом более высокая, чем при других влагосодержаниях. Этот вывод подтверждается наличием минимума
t на кривой 6 спинспиновой релаксации t сорбированной влаги, приведенной на рис. 1.20.
Рис. 1.20. Чистые калориметрическая q (1) и изостерическая q′ (2) теплоты и значения дифференциальной работы Аа (3) (кДж/моль), калориметрической Sa (4) и изостерической
ΔS′а энтропии (5) (Дж/(моль К) десорбции влаги из целлюлозы; кривая спин-спиновой релаксации t (c) (6)
35
Изостерические и калориметрические кривые теплоты испарения несколько различаются особенно в области больших величин

влагосодержаний. Это различие вызвано тем, что изостеры отражают процессы десорбции при равновесных условиях. В калориметрических экспериментах фиксируются также неравновесные процессы, связанные с изменением структуры матрицы, кластеров воды и сопутствующих физикохимических процессов в органических материалах.
Таким образом, объемная сорбция (десорбция) в гидрофильных органических набухающих сорбентах существенно отличается от адсорбции на твердых сплошных телах. Это необходимо учитывать при механической, термической и химической обработке пищевых, текстильных и различных других природных и синтетических материалов.
1.8.Кинетика набухания и деформации материалов
Поглощение жидкостей или растворов при набухании происходит в течение определенного времени t. Уравнение кинетики набухания имеет вид [16]:
dβ dt = к(βm −β), |
(1.8.1) |
где к — константа, βm и β предельная и соответствующая времени t степень набухания, которая рассчитывается по формуле: β=(m –
m0)/m0 = umс/m0.
Здесь m0 и m — навески материала до и после набухания, u =u – u0 — количество поглощенной влаги при набухании; mс — масса абсолютно сухого материала; u0 — начальное влагосодержание материала.
Интегрируя уравнение (1.8.1), получим: |
|
βm (βm −β)= exp(kτ). |
(1.8.2) |
Уравнение (1.8.2) можно переписать в виде: |
|
−ln(1− u um )= kτ, |
(1.8.3) |
где um =um −u0; um — влагосодержание предельно набухшего материала. |
|
Изменения влагосодержания можно заменить на разности их объемов: |
|
−ln(1− V Vm )= kτ. |
(1.8.4) |
На рис. 1.21 приведены графики кинетики набухания для зерна смолы СДВ-3 [16]. Смола поглощала децинормальный раствор хлорида натрия (график 1). При этом происходил ионный обмен. Водород функциональных групп –SO3H замещался ионами натрия. Второй график соответствует восстановлению Naна Н-форму катионита. Время набухания зерен в Na- и Н-формах различно. Коэффициенты k, соответствующие графикам 1 и 2, равны 6,7 10–4 и 2,3 10–3 с–1. Изменения объемов V, отнесенных к
36
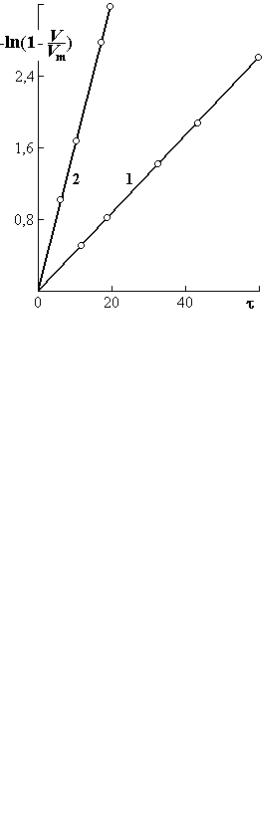
начальному объему V0 =0,858 мм3 зерна катионита в Н-форме при обмене ионов водорода на одно- и двухвалентные ионы показаны на рис. 1.22. При поглощении катионов (за исключением иона лития) в зависимости от энергии гидратации Е относительный объем уменьшается.
При сушке, массопереносе в почвах, грунтах, химических и строительных материалах и изделиях, пищевых продуктах и других средах переносятся растворы различных неорганических соединений. Перенос растворов вызывает изменение структуры ограниченно набухающих материалов, что, в свою очередь, влечет изменение интенсивности внутреннего массопереноса. Это обстоятельство следует учитывать при
анализе процессов переноса влаги в таких средах (см. раздел 1.9). Зависимость давления набухания π от содержания абсолютно сухого
полимера в набухшем студне с имеет вид [12]:
|
|
π=Асβ, |
|
(1.8.5) |
|
|
где А, β — эмпирические постоянные. |
||
|
|
Концентрацию с в уравнении (1.8.5) |
||
|
|
можно заменить |
на величину γ0 =γ/(1 + u). |
|
|
|
После логарифмирования получим соотно- |
||
|
Е |
|||
|
|
шение: |
|
|
|
|
|
|
|
|
|
lgπ=В– β lg(1 + u), |
(1.8.6) |
|
|
|
где В=lg (Аγβ). |
|
|
|
|
Зависимости |
давления набухания при |
|
|
|
сорбции и десорбции (рис. 1.10, кривые 7, 7′) в |
||
|
|
зерне пшеницы в координатах уравнения |
||
|
|
(1.8.6) представлены на рис. 1.23. Увеличение |
||
|
|
давления набухания возможно в том случае, |
||
|
|
если объем тела мало деформируется или ос- |
||
|
|
тается постоянным (γ=const). При |
наличии |
|
Рис. 1.22. Изменение относи- |
жесткой внешней оболочки объем зерна пше- |
|||
тельного объема V/V0 (%) при |
ницы при набухании изменяется незначитель- |
|||
обмене ионов водорода на одно- |
но. |
|
|
|
и двухвалентные ионы (указаны |
Согласно уравнений (1.5.4) и (3.3.5) |
|||
на графиках) |
обратные величины влагосодержаний u–1 и |
|||
|
|
37 |
|
|

|
давления π пропорциональны ло- |
|||
|
гарифму |
ps/p =ϕ–1. Поэтому зна- |
||
|
чения π также пропорциональны |
|||
|
u–1 (рис. 1.23, графики 2, 2′). Эти |
|||
|
графики линейные для u > 0,18 (u– |
|||
|
1 < 5,5). |
При значениях |
u < 0,18 |
|
|
имеет место контракция материа- |
|||
|
ла (рис. 1.10, кривые 4, 4′). |
|
||
|
Контракция материала опи- |
|||
|
сывается |
эмпирическим |
уравне- |
|
|
нием: |
|
|
|
Рис. 1.23. Зависимость логарифма давления π |
|
Vк =au/(b +u), |
(1.8.7) |
|
(МПа) от логарифма 1 +u (1, 1′) и π от u–1 (2, |
где а, b — постоянные. |
|
||
2′) в зерне пшеницы при сорбции (1, 2) и де- |
Изменение объема |
Vк < 0. |
||
сорбции (1′, 2′) влаги |
||||
В уравнении (1.8.7) подставляется |
||||
|
||||
абсолютное значение Vк. В координатах W/ Vк =f(W) (W — влажность, %) на рис. 1.24 приведены результаты опытов контракции желатина, целлюлозы и крахмала, полученные гелевым пикнометром.
Согласно левых ветвей кривых 1, 2, 3 рис. 1.3 происходит уменьшение объема биополимеров. Эта часть объема становится недоступной для атомов гелия.
Как отмечалось, контракция происходит за счет образования при сорбции молекул воды дополнительных связей через «водяные мостики» между функциональными полярными группами контактирующих макромолекул. Вероятность их образования возрастает по мере заполнения первичных центров сорбции молекулами воды.
По мере дальнейшего поглощения влаги при набухании эти «мостики» разрушаются. Поэтому после достижения определенного значения влагосодержания объем биополимеров начинает возрастать.
Таким образом, при увлажнении или сушки набухающие материалы существенно изменяют свою структуру. Это осложняет механизмы внутреннего тепломассопереноса в них по отношению к малодеформируемым пористым телам. В процессе набухания или усадки изменяются энергия связи влаги с материалом, его реологические и прочностные характеристики, а также коэффициенты пере-
Рис. 1.24. Контракция жела- носа тепла и влаги.
тина (1), целлюлозы (2), крахмала (3)
38
1.9. Ионный обмен
Ионный обмен происходит в почвах, глинах, торфе, синтетических ионитах и других материалах. Внутренние поры пространственной структуры (матрицы) зерна ионита заполнены раствором. На матрице находятся ионогенные группы (ИГ). Под воздействием полярного растворителя они диссоциируют. Часть ионов переходят во внутриматричный раствор.
Если в результате диссоциации ИГ во внутриматричный раствор поступают положительные или отрицательные ионы, то такие ионообменные материалы называют соответственно катионитами или анионитами. В некоторых природных материалах при диссоциации ИГ в раствор переходят как положительные, так и отрицательные ионы. При этом обычно преобладает одна группа ионов. Поэтому такой ионит можно отнести либо к катионитам, либо к анионитам. Механизм ионного обмена для катионитов и анионитов аналогичен.
Рассмотрим ионообменный процесс на катионитах [17]. При переходе катионов А во внутриматричный раствор на матрице остаются диссоциированные ИГ — связанные анионы, имеющие средний заряд Z0. Катионы А с зарядом ZА совершают броуновское движение во внутриматричном растворе. Периодически они подходят к диссоциированным ИГ и находятся определенное время в «оседлом состоянии», а затем вновь переходят в раствор.
При постоянных внешних условиях (давлении, температуре) система ионит-раствор находится в динамическом равновесии. При этом одна часть (α0) ИГ находится в диссоциированном состоянии, а другая (1 −α0) взаимодействует с катионами. Величина α0 — степень диссоциации ИГ. Вероятность полной рекомбинации связанного аниона с катионом и образование ионной связи мала, так как они имеют гидратные оболочки. В период «оседлого состояния» катион находится в потенциальной яме связанного аниона. Если несколько связанных анионов находятся вблизи катиона, то он взаимодействует со всеми этими диссоциированными функциональными группами. Между ними возникают по закону Кулона силы притяжения.
Система связанных анионов и подвижных катионов, находящихся во внутриматричном растворе, электронейтральная. По мере увеличения концентрации внешнего раствора свободные катионы и анионы поступают из внешнего во внутриматричный раствор. Их суммарный заряд равен нулю. Поэтому электронейтральность системы ионит – раствор сохраняется.
Поступающие новые катионы В поливалентных металлов одновременно взаимодействуют с диссоциированными ИГ, а также со свободными анионами, находящимися во внутриматричном растворе.
При взаимодействии со свободными анионами возникают ионные ассоциаты и нейтральные молекулы. Например, ионы железа Fe3+ образу-
39

ют соединения [FeOH]2+, [Fe(OH)2]1+, Fe(OH)3 и другие ионные ассоциаты. Молекула Fe(OH)3 выпадает в осадок. Заряд такого «иона» равен нулю. Вероятность образования ионных ассоциатов возрастает по мере уменьшения порового пространства и соответственно объема внутриматричного раствора. При отсутствии пористости ионный обмен возможен только на поверхности зерен ионита.
Таким образом, во внутриматричном растворе ионные ассоциаты с катионом В валентности ZВ имеют заряды j в пределах от нуля до ZB и соответствующие им концентрации CBj.
Средний заряд ZВ* ионных ассоциатов равен:
Z |
|
Z |
|
|
ZB* = ∑B |
j CBj |
∑B |
CBj . |
(1.9.1) |
j=0 |
|
j=0 |
|
|
По мере увеличения концентрации ассоциатов с катионом В во внутриматричном растворе снижается вероятность сорбции на диссоциированных ИГ первичных катионов А. Их концентрация во внутриматричном растворе возрастает. Они мигрируют во внешний раствор, из которого в эквивалентном по заряду количестве дополнительно поступают во внутрь матрицы ионные ассоциаты с катионом В. При этом во всех локальных объемах системы ионит–раствор соблюдается электронейтральность. Внутри матрицы устанавливается не равная начальной α0 степень диссоциации α.
Уравнение ионного обмена имеет вид
|
|
|
1 ZB* |
|
|
|
1 Z *А |
|
|
||
|
|
|
|
||||||||
|
CB |
|
|
CА |
|
, |
(1.9.2) |
||||
|
|
||||||||||
|
|
|
|
= K0 |
|
|
|
||||
CB |
CА |
|
|
||||||||
где K0 — константа обмена.
Соотношение (1.9.2) отличается от уравнения Б. П. Никольского [18]. Вместо активностей в нем учитываются концентрации поглощенных CA и CB и находящиеся во внешнем растворе СА, СВ ионов, а вместо ва-
лентностей ZА, ZВ — средние заряды ионных ассоциатов Z A* и ZB* .
Из соотношения (1.9.2) при малых, средних и больших концентрациях поглощаемого катиона В можно получить уравнения Генри, Ленгмю- ра-Вагелера и Фрейндлиха [17].
Логарифмируя уравнение (1.9.2) получим
Z* |
|
X ′ |
|
1 |
− X ′ |
|
|
|||
A |
lg |
|
|
= lg K +lg |
|
|
|
|
, |
(1.9.3) |
ZB* |
|
|
|
|
||||||
|
X |
|
|
1− X |
|
|
||||
где K = K0Z *A — постоянная обмена; X = CB/CBm, CBm — начальная (макси-
мальная) концентрация ионов В во внешнем растворе; X ′ = CB /CBm , СBm
— максимальное поглощение катионов В и их ассоциатов ионитом. 40
