
Литература от Абакумова ч2 / Осмотический массоперенос
.pdf
зец торфа — вспомогательные камеры всегда имеются низкой концентрации катионы и анионы.
Опыты по электроосмосу проводили следующим образом. Вспомогательные камеры 2 (рис. 3.28) заполняли дистиллированной водой и подключали к электродам 5 источник тока 6. В этом случае наиболее вероятным процессом, позволяющим получить ток во внешней цепи, является электролиз воды. На катоде и аноде происходило разложение молекул во-
ды соответственно по схемам: 4Н2О+ 4е– = 4ОН– + 2Н2↑, 2Н2О– 4е– = |
|
= 4Н+ + О2↑ ([9], т. 2, С. |
582). |
Согласно первой |
реакции на катоде выделяется газ — водород, а |
гидроксилы поступают в раствор. Он становится щелочным. На аноде выделялся газообразный кислород, а за счет ионов водорода раствор в прианодной зоне становится кислым. Согласно экспериментам рН в прианодной зоне достигают значений 3–4, а в прикатодной — 11–12. На аноде и катоде соответственно адсорбируются молекулы кислорода и водорода. Из приведенных реакций следует, что убыль электронов на катоде компенсируется равным их поступлением на аноде. Это позволяет получить постоянный ток во внешние цепи.
По мере увеличения концентрации ионов Н+ и ОН– возрастает их перенос через образец соответственно к катоду и аноду. В связи с этим растет число переносчиков зарядов. В каждом опыте ток поддерживался по-
|
стоянным. |
|
Увеличение |
|||
|
числа ионов обоих знаков |
|||||
|
вызывало |
снижение на- |
||||
|
пряжения между электро- |
|||||
|
дами (рис. 3.34 кривая 5). |
|||||
|
|
К катоду ион водо- |
||||
|
рода (протон) перемеща- |
|||||
|
ется |
путем |
туннельных |
|||
|
переходов (скачков) по |
|||||
|
пространственной |
сети |
||||
|
контактирующих молекул |
|||||
|
воды (см. раздел 1.4). При |
|||||
|
этом |
последовательно |
||||
|
возникает |
ион |
гидроксо- |
|||
|
ния Н3О+. Поступая на |
|||||
Рис. 3.34. Изменение во времени τ (мин) суммарного |
катод |
протон |
получает |
|||
электрон и образует атом |
||||||
Qм+э 104 (см3/с) потока воды под воздействием гидро- |
водорода, |
а |
затем |
моле- |
||
статического давления Qм и электроосмоса Qэ при зна- |
кулу |
Н2 |
|
по |
|
схеме: |
чениях постоянного тока J (мА): 1 (1), 1,5 (2), 2,5 (3), 5 |
|
|
||||
(4); напряжения U (В) (5) после включения тока J =1,5 |
4Н+ + 4е– =2Н2. |
|
|
|||
мА и остаточного потенциала ϕ (В) (6) после его вы- |
|
Гидроксилы |
также |
|||
ключения (А — включение, В — выключение тока) |
переносятся |
эстафетным |
||||
101 |
|
|
|
|
|
|

способом: Н2О+OH– → →OH– +Н2О. И в этом случае протон перемещается к катоду, а возникающий при его переходе отрицательный заряд (ион гидроксила) – к аноду. На аноде происходит реакция: 4OH– =2Н2О+O2 +4e–. Поступившие на анод электроны переносятся по внешней цепи к катоду.
Всвязи с переносом гидроксилов к аноду, у катода возникает избыток ионов водорода. Последние рекомбинируют с гидроксилами прикатодной зоны и образуют молекулы воды. Возможна рекомбинация этих ионов в процессе их переноса через образец.
Образующиеся в результате приведенных реакций молекулы Н2 и О2 дополнительно адсорбируются на электродах, а также растворяются в жидкости.
Внабухшей матрице ионообменного материала (в частности, торфа) поглощенные катионы могут перемещаться под воздействием вектора напряженности внешнего электрического поля. Во внутриматричном растворе они находятся в диссоциированном, подвижном состоянии. Катионы удерживаются в этом растворе равным суммарным зарядом связанных анионов (см. раздел 1.9). Для сохранения электронейтральности убыль из образца в правую камеру поглощенных катионов должна быть компенси-
рована равным по заряду притоком свободных катионов (преимущественно Н+-ионов) из левой камеры.
Свободные катионы вступают в ионный обмен с имеющимися во внутриматричном растворе катионами. При обмене водородных ионов на поливалентные происходит дробление ассоциатов макромолекул (пептизация). Это вызывает в месте обмена ионов дополнительное набухание матрицы ионообменного материала. Поступившие из образца катионы
Рис. 3.35. Распределение концентраций катионов С (мг-экв/г сух. вещества) по длине образца l (см) верхового торфа в процессе электроосмоса кальция (1), магния (2),железа (3); 4, 5, 6 — соответственно их начальные концентрации
вступают в катодной зоне во взаимодействие с гидроксилами и другими свободными анионами.
С увеличением подаваемого на электроды напряжения (и соответственно тока во внешней цепи) возрастает вынос катионов в прикатодную зону. Мигрируя в эту зону, катионы не могут вызвать ток во внешней цепи из-за отсутствия равного по заряду поступления анионов к аноду. Связанные анионы не перемещаются, поэтому электроны от них на анод не поступают.
О выносе поглощенных катионов из образцов торфа свидетельствуют их распределения по длине образца (рис. 3.35), полученные до и после завершения опытов с электроосмотическим переносом. Поступление катионов в тече-
102
ние опыта фиксировалось путем отбора проб в правой камере и определения концентраций в них ионов. В первую очередь выносятся одновалентные катионы, затем двухвалентные ионы Са2+ и Mg2+. Ионы железа, соединяясь со свободными анионами, образуют ионные ассоциаты (см. раздел 1.9). Поэтому вынос ионов Fe3+ в прикатодную зону незначителен.
По мере выноса катионов возрастает их концентрация в прикатодной зоне. Это вызывает увеличение осмотического давления и переноса (всасывания) молекул воды из левой в правую камеру как при солевом ос-
мосе (рис. 3.32).
Вначале процесса переноса графики зависимости Qм+э от времени
—линейные (рис. 3.34). Осмотический перенос Qэ возрастает с увеличением тока J. Отношение Qэ/J — приблизительно постоянная величина. Со-
гласно экспериментам при токах 0.5, 2, 3, 4, 6, 9, 10 мА значения Qэ соот-
ветственно были равны (0,2; 0,8; 1,25; 1,6; 2,3; 3,3; 3,5)·10–3 см3/с.
Для токов J < 1,5 мА (графики 1, 2) после линейного участка электроосмотический поток становится постоянным. При J > 1,5 мА после ли-
нейного участка (графики 3, 4) значения Qм+э уменьшаются, а затем поток стабилизируется. Его снижение вызывается обратным переносом катионов в образец из-за разности концентраций катионов металлов в прикатодной зоне и образце. Возникает солевой осмос. Об этом свидетельствует значительное увеличение концентраций катионов в конце опыта вблизи правого торца образца (рис. 3.35) В связи с уменьшением концентрации катионов в прикатодной зоне снижается осмотический перенос воды в правую камеру установки.
После достижения равенства количества выносимых катионов в прикатодную зону и обратном направлении наблюдается установившийся электроосмотический поток.
Для больших значений тока доля фильтрационного переноса Qм по отношению к электроосмотическому потоку мала, а при низких она существенна из-за снижения интенсивности обратной диффузии катионов в образец. Времени стабилизации электроосмотического потока соответствует время установления постоянного, но неоднозначного для различных токов J, напряжения на электродах.
При выключении тока (рис. 3.34, точка В) происходит постепенное
снижение совместного потока Qм+э до фильтрационного Qм. Для малых значений тока J (графики 1, 2) установившийся поток наблюдается в течение 30–40 минут после отключения тока вследствие выноса катионов в прикатодную зону фильтрационным потоком и остаточной разности потенциалов φ. При изменении тока от 0,5 до 10 мА значения φ равны 0,3–0,8 В.
На спиральных платиновых электродах, которые омываются потоком жидкости, количество адсорбированных молекул водорода и кислорода мало. При десорбции молекул водорода и кислорода с электродов и перехода
их в раствор происходят реакции: 2Н2 – 4e– =4H+ и 2Н2О+O2 +4e– =4OH–. 103
Эти реакции обратные тем, которые имеют место при разряде ионов водорода и гидроксилов на электродах. В результате рекомбинаций этих ионов образуются молекулы воды. Они синтезируются из молекул водорода и кислорода. Эти реакции сопровождаются, как и горение водорода в атмосфере кислорода, выделением энергии (тепла). Часть ее может быть использована для совершения работы. Благодаря этому возникает вторичный источник тока.
Миграция избытка Н+ и ОН– ионов и их разряд на электродах вызывает дополнительную адсорбцию молекул Н2 и О2 соответственно на катоде и аноде. Этот процесс происходит до полной рекомбинации водородных ионов и гидроксилов во вспомогательных камерах и превращения их в молекулы воды. Он способствует продлению работы вторичного источника тока в течение продолжительного времени после выключения основного источника тока.
Воздействие внешнего электрического (или другого) поля приводит ограниченную в пространстве систему в неравновесное состояние. При определенных параметрах поля в ней достигаются не равновесные, а установившиеся процессы. В этом случае в системе наблюдается постоянство потоков энергии, вещества, зарядов.
Если внешние поля прекращают воздействия, то неравновесная система в течение определенного времени релаксации стремится к исходному равновесию. В этом случае в любом локальном ее объеме вновь наблюдается постоянство физических величин. Для такого состояния системы применима термодинамика равновесных процессов (термостатика). Достигается также неизменность (постоянство) информации, свидетельствующая о равновесии системы. Она поступает от комплекса датчиков и устройств контроля процессов внутри ограниченной системы.
Установление равновесия и соответственно значений φ=0 при токах 0,5–10 мА происходит в течение 16–36 ч. За это время возникает обратный отток катионов металлов из прикатодной зоны и равномерное их распределение по длине образца. Этот процесс сопровождается ионным обменом. Ионы водорода замещаются на ионы металлов. При этом вновь происходит изменение структуры торфа.
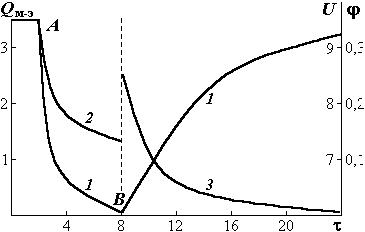
Если электроосмотический поток Qэ направлен противоположно фильтрационному Qм, то общий поток Qм–э (рис. 3.36, кривая 1) и напряжения на электродах (кривая 2) постепенно во времени снижаются. После выключения тока (точка B) после 16 ч опыта результирующий поток Qм–э не достигал фильтрационного Qм, а остаточное напряжение φ (кривая 3) не снижалось до нуля. Механизм переноса ионов подобен приведенному выше, но имеется и отличие.
При встречных потоках Qм–э массоперенос, вызванный градиентом гидростатического давления Qм =3,5·10–4 см3/с, существенно осложнял миграцию катионов в левую камеру, в которой находился катод. Из-за
104
уменьшения притока катионов снижались значения электроосмотического потока по отношению к их величинам при параллельном совместном электроосмотическом и фильтрационном переносе Qм+э.
Вся совокупность подвижных ионов во внешнем постоянном электрическом поле способствует разрушению структуры воды. Само электрическое поле ориентирует функциональные полярные группы ВМС и молекулы воды, создает макродиполи за счет локального переноса протонов вдоль направления вектора напряженности поля (см. раздел 1.4). Это влечет искажение и разрыв водородных связей в ассоциатах молекул воды. Количество несвязанных молекул возрастает, а средняя энергия связи U между ними уменьшается.
Рис. 3.36. Изменения суммарного Qм–э 104 (см3/с) (1) потока воды под воздействием гидростатического давления Qм и обратного электроосмотического потока Qэ, напряжения U (В) (2) после включения тока и остаточного потенциала ϕ (В) (3) после его выключения с увеличением времени τ (ч) (А — включение, В — выключение тока J =1 мА)
Чем большая разность потенциалов (и соответственно ток J) приложена к электродам, тем более интенсивное разрушение структуры воды. Об этом свидетельствуют экспериментальные графики lgQэ =f1(Т–1) и lgQм+э =f2(Т–1), которые в диапазоне температур 273–313 К — линейные. Полученные из этих графиков значения энергии активации Е, необходимые для скачков молекул воды при электроосмосе, равны 9,6; 7,1; 6,7; 6,3 кДж/моль. Этим величинам Е соответствуют токи 0,5; 1; 1,5; 3 мА. Энергия фильтрационного массопереноса при i =3, как отмечалось ранее, равна 18 кДж/моль. Для совместного параллельного фильтрационно-электро- осмотического потока Qм+э при тех же значениях токов значения энергии активации Е соответственно равны 13,4; 11,3; 10,5; 8,4 кДж/моль.
Как показали опыты, применение электроосмотического обезвоживания набухших материалов целесообразно при низкой их водопроницаемости.
105

4.МАССОПЕРЕНОС ПРИ СУШКЕ
ИУСАДКЕ МАТЕРИАЛОВ
4.1.Механизм влагопереноса в ненабухающих материалах
Исследования механизма внутреннего влагопереноса при конвективной сушке различных материалов с применением радиоактивных индикаторов [22, 40, 41] проводили на установке, изображенной на рис. 4.1. Внутри гигротермостата с помощью растворов солей, находящихся в сосудах, устанавливали необходимую для опытов постоянную температуру и относительную влажность воздуха. Установка имела устройства для измерения массы и объемной усадки материала в процессе сушки. Измерение объема образцов определяли ртутным волюминометром. В различные периоды времени от начала сушки образец закрывали сверху камерой, которая плотно контактировала с дном гигротермостата. Отрывая кран, ртуть заполняла камеру. Объем образца определяли по перемещению мениска в капилляре. После измерения ртуть сливали в емкость, помещенную в термостате. В гигротермостате и термостате температуру поддерживали постоянной.
Предварительно исследуемые материалы насыщали водным раствором радиоактивной соли Na2S*O4. В процессе сушки радиоактивный индикатор поступал на поверхность образца. Величину потока β-частиц определяли с помощью счетчика 20.
Критерий фазового превращения рассчитывали по формуле
ε=1− |
u−uк |
|
N N0 |
, |
(4.1.1) |
1−N N |
u |
||||
0 |
|
|
|
|
|
где N – интенсивность излучения при влагосодержании u, соответствующем времени t; N0 – максимальная радиоактивная в конце сушки; N/N0 – относительное изменение радиоактивности при уменьшении влагосодержания на u.
Объектами исследования были гидрофильные сферические образцы пористого кварца диаметром 15 мм, диски толщиной 3 – 4 мм и диаметром 26 мм из пористого стекла с размерами пор 5, 40, 100, 160 мкм и керамические сферические образцы диаметром 15 мм.
110
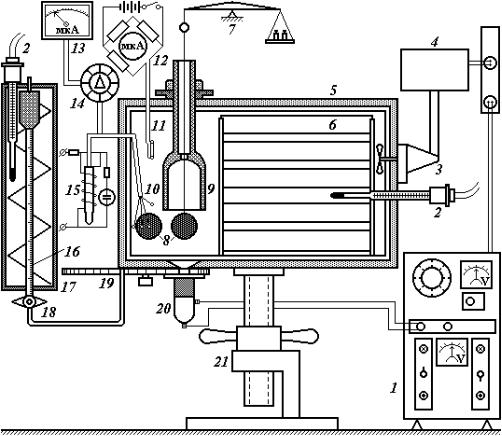
Рис. 4.1. Установка для конвективной сушки дисперсных материалов: радиометр (1); контактный термометр (2); вентилятор (3); выпрямитель (4); гигротермостат (5); сосуды с растворами солей (6); весы (7); образцы (8); камера (9); термопары (10); термистор (11); мостовая схема (12); гальванометр (13); переключатель (14); микротермостат (15); измерительный капилляр (16); термостат (17); кран (18); поворотный диск (19); детектор (20); подставка (21)
Образцы пористого кварца получали методом спекания кварцевого порошка с близкими по размеру зернами. В результате спекания образцы имели размеры пор 3 – 5 мкм и удельную поверхность S =100 м2/кг. Гидрофобные образцы получали тем же способом, но затем пропитывали двухпроцентным раствором триметилхлорсилана ((CH3)3SiCl) в бензоле с последующей промывкой чистым бензолом и сушкой. В результате, гидрофильные группы на поверхности зерен кварца замещались на метильные CH3 группы. Для насыщения радиоактивным раствором образцы подвергали вначале вакуумированию при давлении 13 Па. Затем под давлением 1 МПа раствор впрессовывался в поры материала до предельного влагонасыщения Wп =20,7%. Такая же предельная абсолютная влажность была у гидрофильных кварцевых образцов. Изотермическую сушку образцов проводили при относительной влажности воздуха ϕ=0,1 и 0,76, температуре среды Тс =323 К и постоянной скорости воздушного потока 2 м/с.
111

|
|
Температурные |
|
кривые |
||||
|
(рис. 4.2, графики 3 – 5 и 6 – 8) |
|||||||
|
имеют несколько |
характерных |
||||||
|
точек перегиба. После неболь- |
|||||||
|
шого времени прогрева наблю- |
|||||||
|
дается период постоянной тем- |
|||||||
|
пературы во всех слоях материа- |
|||||||
|
ла. Влага в этом периоде испаря- |
|||||||
|
ется |
при |
температуре мокрого |
|||||
|
термометра. Затем она повыша- |
|||||||
|
ется. Влага испаряется с постоян- |
|||||||
|
ной скоростью q=100·du/dτ (%/ч) в |
|||||||
|
течение всего времени сушки за |
|||||||
|
исключением низких |
влагосодер- |
||||||
|
жаний (рис. 4.3, графики 1, 2). Пе- |
|||||||
|
реход от постоянного к периоду |
|||||||
|
роста температуры для данного ма- |
|||||||
|
териала |
имеет |
|
место |
при |
|||
|
W≈5 – 7%. |
|
|
|
|
|
||
|
|
Подобные |
графики |
полу- |
||||
|
чены |
при |
сушке |
сферического |
||||
Рис. 4.2. Зависимости от времени τ (ч) при |
образца при том же значении ϕ и |
|||||||
Тс =323 К изменения влагосодержания u (1, 2); |
более |
высокой |
|
температуре |
||||
относительной радиоактивности N/N0 (1′, 2′); |
343 К. При этом время сушки со- |
|||||||
температуры Т (К) на поверхности (3, 6), в се- |
кратилось |
почти |
в |
два раза |
||||
редине радиуса (4, 7) и в центре (5, 8) порис- |
(рис. 4.2, графики 2 – 8). |
|
||||||
того сферического образца кварца при ϕ=0,76 |
|
Согласно |
калориметриче- |
|||||
(1, 1′, 3, 4, 5) и 0,1 (2, 2′, 6, 7, 8) |
|
|||||||
ским опытам (см. рис. 1.18), до |
||||||||
|
||||||||
влажности 5% теплоты испарения из кварцевого песка и молотого кварца малы. В этом случае влага испаряется из макропор. При W <5% наблюдается существенный рост теплоты испарения, так как удаляются манжетная влага, а затем пленки воды.
Подтверждением предложенного механизма массопереноса служат графики выноса радиоактивности (рис. 4.2, кривые 1′, 2′), скорости поступления метки B =100·d(N/N0)/dτ (%/ч) на поверхность образца (рис. 4.3, кривые 1′, 2′), а также значение ε (рис. 4.3, кривые 1′′, 2″).
Зона испарения в начале сушки отступает внутрь образца, и ε становится меньше единицы. Вся влага испаряется с менисков и пленок влаги. Значительный рост температуры и радиоактивности наблюдается при влажности меньше 5%. Увеличение температуры вызвано тем, что подводимое к образцу тепло неполностью затрачивается на парообразование. Имеет место постепенный нагрев материала до температуры сухого термометра.
112
Рост радиоактивности при W <5% связен не только осушением поверхностных слоев, но и жидкостным переносом влаги с высокой концентрацией метки в эти слои образца. При этом поступление излучения из больших по толщине поверхностных слоев из-за малых размеров пор мало вероятно. Перенос пара в них затруднен, поэтому основным механизмом влагопереноса в этом случае является пленочный, а также жидкостный массоперенос в узких щелях между контактирующими частицами кварца.
В связи с этим значение критерия ε постепенно уменьшается (рис. 4.3, кривые 1′′, 2′′).
С увеличением относительной влажности внешней парогазовой среды скорость пленочного переноса и диффузии пара из образца снижаются. Это следует из анализа кривых скорости накопления метки B на поверхности образца (рис. 4.3, графики 1′, 2′). Величина B в конце сушки при относительной влажности воздуха ϕ=0,1 приблизительно в два раза больше, чем при ϕ=0,76. В опытах при более высокой температуре 343 К наблюдается увеличение радиоактивности на поверхности образца из-за более интенсивного пленочного переноса.
|
По |
мере |
дальнейшей |
|||
|
сушки пленки влаги у поверх- |
|||||
|
ности |
образца |
постепенно |
|||
|
становятся тоньше и на от- |
|||||
|
дельных |
участках поверхно- |
||||
|
сти и внутри тела разрывают- |
|||||
|
ся. Оставшаяся влага в водо- |
|||||
|
проводящей пленке стекает в |
|||||
|
манжеты, что приводит к |
|||||
|
снижению жидкостного пере- |
|||||
|
носа влаги. Она испаряется с |
|||||
|
отдельных менисков и поли- |
|||||
|
молекулярных |
слоев жидко- |
||||
|
сти и переносится в окру- |
|||||
|
жающую газовую среду в па- |
|||||
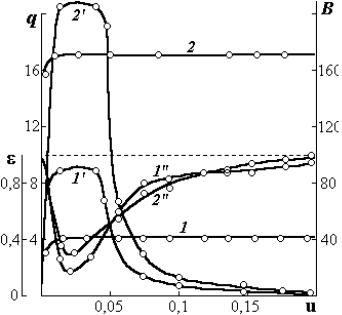
Рис. 4.3. Зависимости скорости сушки q (1, 2) |
ровой фазе. При этом значе- |
|||||
(%/ч); выноса радиоактивной метки В (1′, 2′) |
ния ε |
стремятся |
к единице |
|||
(%/ч); критерия фазового превращения ε (1′′, 2′′) |
(рис. 4.3, кривые 1′′, 2′′). |
|
||||
от влагосодержания u пористого образца кварца |
Для |
гидрофобных |
об- |
|||
в процессе сушки при Тс =323 К |
разцов |
из пористого кварца |
||||
|
наблюдается |
постоянный |
и |
|||
переменный периоды сушки (рис. 4.4). При малых влажностях наблюдается резкое снижение интенсивности испарения внутри образца и пароперенос по системе макропор. Скорость сушки q на 20 – 30% меньше, чем для гидрофильного кварца.
113

|
В гидрофобных образцах от- |
||
|
сутствует пленочный перенос влаги. |
||
|
При низкой средней влажности по- |
||
|
верхностные слои образца пол- |
||
|
ностью высушиваются, поэтому воз- |
||
|
растает поток бета-излучения в |
||
|
счетчик. Об этом свидетельствует |
||
|
незначительное увеличение |
радио- |
|
|
активности |
поверхности, |
которое |
|
наблюдается |
при влагосодержании |
|
|
меньше 0,05. |
|
|
|
Сушка дисковых образцов по- |
||
|
ристого стекла проходила в тех же |
||
|
условиях, что и кварцевых. Она име- |
||
Рис. 4.4. Кривые скорости сушки q (1 – 4) |
ет периоды постоянной и пере- |
||
(%/ч) и выноса радиоактивности N/N0 |
менной скорости сушки. |
|
|
(1′– 4′) на поверхность пористых гидро- |
В постоянном периоде ско- |
||
фобных сферических кварцевых образцов |
рость сушки мало изменяется для |
||
при ϕ=0,76 (1, 3, 1′, 3′) и 0,1 ((2, 4, 2′, 4′) |
образцов, имеющих размеры пор |
||
и температурах Т=323 (1, 2, 1′, 2′) и 343 |
больше 40 мкм, и существенно выше |
||
(3, 4, 3′, 4′) К |
для образца с размером пор 5 мкм |
||
|
|||
(табл. 4.1). Влагосодержание, соответствующее переходу постоянного периода сушки к переменному (первое критическое влагосодержание uк) практически не зависит от пористости этих образцов, но для гидрофобных образцов оно больше. Скорость сушки гидрофильных образцов выше, чем гидрофобных из-за пленочного переноса. Период постоянной скорости сушки сохраняется вплоть до разрыва водопроводящих пленок.
Таблица 4.1. Первое критическое влагосодержание uк и скорость сушки в постоянном периоде qп (%/ч) для пористых стекол
Размер |
|
|
Гидрофильные |
|
|
|
Гидрофобные |
|
||
пор, |
|
ϕ=0,1 |
ϕ=0,76 |
|
ϕ=0,1 |
ϕ=0,76 |
||||
мкм |
uк |
|
qп |
uк |
qп |
uк |
|
qп |
uк |
qп |
5 |
1,2 |
|
51,4 |
0,6 |
12,9 |
2,6 |
|
45,6 |
2,2 |
11,5 |
40 |
0,9 |
|
35 |
0,6 |
10,2 |
4,4 |
|
26,4 |
3 |
8,7 |
100 |
0,8 |
|
38,2 |
0,6 |
9,7 |
2,4 |
|
32,4 |
2 |
8,7 |
160 |
0,8 |
|
35,4 |
0,4 |
9,5 |
4 |
|
26,5 |
3,5 |
7,5 |
Для оценки критерия фазового превращения ε можно взять отношение скорости сушки гидрофобного к подобному гидрофильному образцу (рис. 4.5а, б). Значения ε можно определять по формуле (4.1.1) с помощью метки (в, г). Кривые зависимости ε от влажности подобны, но количественно имеют отличия. Это вызвано тем, что методом радиоактивных индикаторов определяются значения ε испаряемой влаги с поверхностных
114
