
- •Кафедра теоретических основ материаловедения
- •Гринева с.И., Сычев м.М., Лукашова т.В.,
- •Коробко в.Н., Мякин с.В.
- •Коррозия и методы защиты
- •Содержание
- •Введение
- •1 Краткие сведения о коррозионных процессах
- •1.1 Классификация коррозионных разрушений
- •1.2 Методы оценки коррозионной стойкости
- •1.3 Методы коррозионных испытаний
- •2 Факторы, влияющие на развитие коррозии материалов
- •2.1 Внутренние факторы коррозии
- •2.1.1 Термодинамическая устойчивость металла
- •2.1.2 Положение металла в периодической системе элементов
- •2.1.3 Химический состав и структура сплавов
- •2.1.4 Шероховатость поверхности и внутренние напряжения в деталях
- •2.2 Внешние факторы коррозии
- •2.2.1 Влияние рН на скорость коррозии
- •2.2.2 Влияние кислорода на скорость коррозии
- •2.2.3 Влияние температуры на скорость коррозии
- •2.2.4 Влияние давления на скорость коррозии
- •2.2.5 Влияние скорости движения электролита на скорость коррозии
- •2.2.6 Влияние состава и концентрации нейтральных солей на скорость коррозии
- •3 Химическая коррозия металлов
- •3.1 Газовая коррозия
- •3.1.1 Образование оксидных соединений на поверхности металла
- •3.1.2 Условия образования, защитных оксидных пленок
- •3.1.3 Скорость роста пленки на металлах
- •3.1.4 Газовая коррозия стали и чугуна
- •3.1.5 Катастрофическая газовая коррозия
- •3.1.6 Водородная коррозия. Водородный износ
- •3. 1.7 Карбонильная коррозия
- •3.1.8 Коррозия, вызываемая сернистыми соединениями
- •3.1.9 Коррозия, вызываемая хлором
- •3.1.10 Защита от газовой коррозии
- •3.2 Коррозия металлов в неэлектролитах
- •4. Электрохимическая коррозия
- •4.1 Особенности строения электролитов
- •4.2 Образование двойного электрического слоя
- •4.3 Электродные потенциалы
- •4.4 Механизм электрохимической коррозии
- •4.5 Поляризация электродов
- •4.6 Деполяризация электродов
- •4.7 Коррозионная диаграмма Эванса
- •4.8 Факторы, ограничивающие электрохимическую коррозию
- •5. Пассивность металлов
- •5.1 Теория пассивности металлов
- •5.2 Кинетика анодных процессов при пассивации металлов
- •6 Атмосферная коррозия металлов
- •6.1 Факторы, вызывающие атмосферную коррозию
- •6.2 Виды и механизм атмосферной коррозии
- •6.3 Скорость атмосферной коррозии
- •7. Подземная коррозия
- •7.1 Почвенная коррозия
- •7.2 Коррозия, вызванная действием блуждающих токов
- •8. Локальная коррозия
- •8.1 Точечная (питтинговая) коррозия
- •8.2 Щелевая коррозия
- •8.3 Межкристаллитная коррозия
- •8.4 Ножевая коррозия
- •9 Методы защиты от коррозии
- •9.1 Защита металлов от коррозии обработкой коррозионной среды
- •9.1.1 Удаление агрессивных компонентов из коррозионной среды
- •9.1.2 Защита металлов от коррозии ингибиторами
- •9.1.3 Механизм защитного действия ингибиторов
- •9.1.4 Влияние некоторых факторов на эффективность действия
- •9.2 Защитные покрытия
- •9.2.1 Металлические покрытия
- •9.2.2 Защитные покрытия на органической основе
- •9.2.3 Защитные покрытия на неорганической основе
- •9.3 Электрохимическая защита
- •9.3.1 Катодная зашита
- •9.3.2 Анодная защита
- •9.3.3 Защита от коррозии, вызываемой блуждающими
- •9.4 Защита от коррозии на стадии проектирования
- •9.4.1 Выбор материалов
- •9.4.2 Рациональные геометрические формы конструкций
- •Литература
- •Коррозия и методы защиты
2.2.2 Влияние кислорода на скорость коррозии
Источником кислорода в подавляющем большинстве случаев является воздух. Кислород может оказывать положительное и отрицательное влияние на скорость коррозии. Растворенный кислород в электролитах, выступающий в качестве деполяризатора, усиливает коррозионное разрушение, причем скорость коррозии возрастает по линейной зависимости с ростом концентрации растворенного кислорода. Если же кислород выступает в роли пассиватора, то прямая зависимость наблюдается до тех пор, пока слишком высокая концентрация кислорода не приводит к

Рисунок 5 — Зависимость скорости коррозии железа
от концентрации кислорода в воде
пассивации поверхности металла, после чего происходит снижение скорости коррозии. На рисунке 5 показана зависимость скорости коррозии железа от концентрации растворенного в воде кислорода. Из графика видно, что при малых и средних концентрациях кислорода скорость коррозии резко возрастает, а при больших концентрациях понижается вследствие образования защитных пленок.
Следует отметить, что кислород способствует уменьшению числа коррозионных центров на поверхности металла, на которых может возникнуть коррозионный процесс, но вместе с тем увеличивает скорость коррозии в точке, начавшей корродировать.
2.2.3 Влияние температуры на скорость коррозии
С повышением температуры скорость коррозии, как и многих химических процессов, возрастает, так как увеличивается скорость диффузии, растворимость продуктов коррозии и др. На рисунке 6 показана характерная экспоненциальная кривая зависимости скорости коррозии от температуры. Наблюдаемая зависимость скорости коррозии от температуры может быть приближенно выражена уравнением
K= Ae-Q/RT ,
где К — скорость коррозии; А — константа, зависящая от конкретных условий коррозии; Q — величина энергии активации, необходимой для ослабления связи внутри молекул и возбуждения их до способности реагирования с молекулами окружающей среды; R — универсальная газовая постоянная; Т — абсолютная температура.
Из уравнения видно, что скорость коррозии будет возрастать с повышением температуры и понижением энергии активации. Однако, следует учитывать, что с повышением температуры уменьшается растворимость кислорода в воде.

Рисунок 6 — Зависимость скорости коррозии от температуры
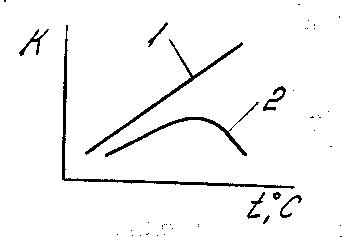
1 — в закрытой системе; 2 — в открытой системе
Рисунок 7 — Зависимость скорости коррозии железа в воде
от температуры
При комнатной температуре в открытой системе в 1 дм3 воды содержится около 6 см3 растворенного кислорода, а при температуре кипения кислорода в воде практически нет. Вследствие этого скорость коррозии железа в воде при повышении температуры будет зависеть от того, открыта или закрыта система (рисунок 7). В закрытой системе, когда удаление кислорода из раствора затруднено, скорость коррозии изменяется пропорционально температуре. В открытой системе скорость коррозии железа растет с повышением температуры примерно до 70—80°С, при дальнейшем повышении температуры растворимость кислорода значительно снижается и скорость коррозии железа в воде уменьшается.
