
- •Кафедра теоретических основ материаловедения
- •Гринева с.И., Сычев м.М., Лукашова т.В.,
- •Коробко в.Н., Мякин с.В.
- •Коррозия и методы защиты
- •Содержание
- •Введение
- •1 Краткие сведения о коррозионных процессах
- •1.1 Классификация коррозионных разрушений
- •1.2 Методы оценки коррозионной стойкости
- •1.3 Методы коррозионных испытаний
- •2 Факторы, влияющие на развитие коррозии материалов
- •2.1 Внутренние факторы коррозии
- •2.1.1 Термодинамическая устойчивость металла
- •2.1.2 Положение металла в периодической системе элементов
- •2.1.3 Химический состав и структура сплавов
- •2.1.4 Шероховатость поверхности и внутренние напряжения в деталях
- •2.2 Внешние факторы коррозии
- •2.2.1 Влияние рН на скорость коррозии
- •2.2.2 Влияние кислорода на скорость коррозии
- •2.2.3 Влияние температуры на скорость коррозии
- •2.2.4 Влияние давления на скорость коррозии
- •2.2.5 Влияние скорости движения электролита на скорость коррозии
- •2.2.6 Влияние состава и концентрации нейтральных солей на скорость коррозии
- •3 Химическая коррозия металлов
- •3.1 Газовая коррозия
- •3.1.1 Образование оксидных соединений на поверхности металла
- •3.1.2 Условия образования, защитных оксидных пленок
- •3.1.3 Скорость роста пленки на металлах
- •3.1.4 Газовая коррозия стали и чугуна
- •3.1.5 Катастрофическая газовая коррозия
- •3.1.6 Водородная коррозия. Водородный износ
- •3. 1.7 Карбонильная коррозия
- •3.1.8 Коррозия, вызываемая сернистыми соединениями
- •3.1.9 Коррозия, вызываемая хлором
- •3.1.10 Защита от газовой коррозии
- •3.2 Коррозия металлов в неэлектролитах
- •4. Электрохимическая коррозия
- •4.1 Особенности строения электролитов
- •4.2 Образование двойного электрического слоя
- •4.3 Электродные потенциалы
- •4.4 Механизм электрохимической коррозии
- •4.5 Поляризация электродов
- •4.6 Деполяризация электродов
- •4.7 Коррозионная диаграмма Эванса
- •4.8 Факторы, ограничивающие электрохимическую коррозию
- •5. Пассивность металлов
- •5.1 Теория пассивности металлов
- •5.2 Кинетика анодных процессов при пассивации металлов
- •6 Атмосферная коррозия металлов
- •6.1 Факторы, вызывающие атмосферную коррозию
- •6.2 Виды и механизм атмосферной коррозии
- •6.3 Скорость атмосферной коррозии
- •7. Подземная коррозия
- •7.1 Почвенная коррозия
- •7.2 Коррозия, вызванная действием блуждающих токов
- •8. Локальная коррозия
- •8.1 Точечная (питтинговая) коррозия
- •8.2 Щелевая коррозия
- •8.3 Межкристаллитная коррозия
- •8.4 Ножевая коррозия
- •9 Методы защиты от коррозии
- •9.1 Защита металлов от коррозии обработкой коррозионной среды
- •9.1.1 Удаление агрессивных компонентов из коррозионной среды
- •9.1.2 Защита металлов от коррозии ингибиторами
- •9.1.3 Механизм защитного действия ингибиторов
- •9.1.4 Влияние некоторых факторов на эффективность действия
- •9.2 Защитные покрытия
- •9.2.1 Металлические покрытия
- •9.2.2 Защитные покрытия на органической основе
- •9.2.3 Защитные покрытия на неорганической основе
- •9.3 Электрохимическая защита
- •9.3.1 Катодная зашита
- •9.3.2 Анодная защита
- •9.3.3 Защита от коррозии, вызываемой блуждающими
- •9.4 Защита от коррозии на стадии проектирования
- •9.4.1 Выбор материалов
- •9.4.2 Рациональные геометрические формы конструкций
- •Литература
- •Коррозия и методы защиты
4.7 Коррозионная диаграмма Эванса
Качественные закономерности процесса коррозии принято рассматривать на поляризационных коррозионных диаграммах Эванса, построенных в координатах потенциал — ток. На рисунке 19 показана коррозионная (поляризационная) диаграмма Эванса.
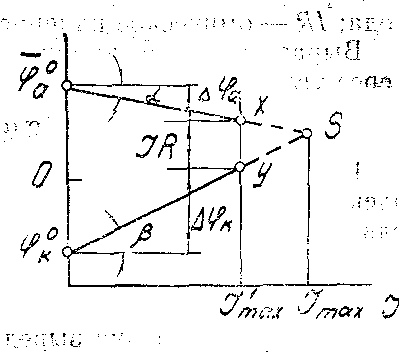
Рисунок 19 — Коррозионная диаграмма Эванса
На оси абсцисс отложен коррозионный ток J, величина которого пропорциональна скорости коррозии. На верхней части оси ординат отложены отрицательные значения потенциалов электродов. В упрощенном виде поляризационные кривые анода и катода представлены в виде прямых. На графике приняты обозначения: φа0; φк0 — начальное положение потенциалов анода и катода при разомкнутом состоянии электродов, т. е. при бесконечно большом омическом сопротивлении цепи микроэлемента и отсутствии тока; S — точка пересечения анодной и катодной поляризационных кривых, соответствующая короткому замыканию анода и катода, без омического сопротивления; α, β — углы наклона кривых, характеризующих поляризационные сопротивления анода и катода; JR — омическое падение потенциала.
Выразим поляризационные сопротивления анода и катода через углы наклона кривых:
Ра = tgα ; Pk = tgβ
Из графика видно, что начальная разность потенциалов электродов микроэлемента расходуется на поляризационный сдвиг потенциалов анода и катода и на омическое падение потенциала:
φk —φa = JR + JРa + JPk
Из этого уравнения выведем значение силы коррозионного тока:
![]()
Сила коррозионного тока, а, следовательно, электрохимическая коррозия, тем больше, чем больше начальная разность потенциалов анода и катода микроэлемента и чем меньше омическое сопротивление пары и поляризуемость электродов. При R=0 получим пересечение поляризационных кривых в точке S и, следовательно, максимальный ток в микроэлементе:
![]()
Максимальный ток в реальных условиях не может существовать. Внутреннее омическое сопротивление микропары имеет определенное значение за счет сопротивления на границах участков анода и катода, а также за счет сопротивления электролита, омывающего эти участки. На графике точками х и у обозначено падение разности потенциалов за счет указанных сопротивлений. Следовательно, в реальных условиях максимальный коррозионный ток — J'mах.
При изучении диаграммы Эванса может показаться странным, что при падении разности потенциалов растет сила тока, что противоречит закону Ома. Это противоречие отпадает, если учесть, что с ростом силы тока резко падает внутреннее сопротивление микропары, причем уменьшение сопротивления обгоняет понижение разности потенциалов. Причины этого явления еще недостаточно изучены. Равновесные потенциалы электродных реакций и сопротивление цепи, а также поляризуемость электрода зависят в свою очередь от природы, состава и свойств металла и электролита (коррозионной среды), а также от внешних условий, таких как температура, перемешивание раствора и других. Коррозионная диаграмма Эванса широко используется при исследовании коррозионных процессов.
