
- •Содержание
- •2. Классификация органических соединений.
- •3. Соединения с открытой цепью.
- •3.1. Углеводороды
- •3.1.1. Алканы
- •3.1.2. Алкены или олефины (соединения этиленового ряда).
- •3.1.3. Углеводороды с двумя двойными связями (алкадиены).
- •3.1.4. Алкины (ацетиленовые углеводороды).
- •3.2. Производные углеводородов.
- •3.2.1. Галогенопроизводные алканов.
- •3.2.2. Металлоорганические соединения.
- •3.2.3. Спирты.
- •3.2.4. Простые эфиры.
- •3.2.5. Нитросоединения.
- •3.2.6. Амины.
- •3.2.7. Альдегиды и кетоны.
- •3.2.8. Карбоновые кислоты.
- •4. Карбоциклические соединения.
- •4.1. Алициклические соединения.
- •4.2. Ароматические соединения.
- •4.2.1. Ароматические углеводороды ряда бензола.
- •4.2.2. Галогенопроизводные аренов.
- •4.2.3. Ароматические сульфокислоты.
- •4.2.4. Ароматические нитросоединения.
- •4.2.5. Ароматические амины.
- •4.2.6. Диазо- и азосоединения.
- •4.2.7. Фенолы.
- •4.2.8. Ароматические альдегиды и кетоны.
- •4.2.9. Ароматические карбоновые кислоты.
- •4.2.10. Ароматические соединения с конденсированными ядрами.
- •5. Полимеры.
- •5.1. Полимеры, получаемые методом поликонденсации.
- •5.2. Полимеры, получаемые методом полимеризации.
- •6. Указания к выполнению контрольных работ.
- •7. Типовые задачи и их решение.
- •8. Контрольные задания
- •8.1. Контрольная работа 1.
- •8.2. Контрольная работа 2.
- •8.3. Контрольная работа 3.
3.2. Производные углеводородов.
3.2.1. Галогенопроизводные алканов.
Галогенопроизводные углеводородов можно рассматривать как продукты замещения в углеводородах одного или нескольких атомов водорода атомами галогенов. Изомерия их зависит от изомерии углеродной цепи и положения галогена. Поляризация связи в алкилгалогенидах способствует замещению галогена на другие атомы или частицы, обладающие нуклеофильным характером.
В зависимости от структуры алкилгалогенида, силы нуклеофильного агента, условий процесса и природы растворителя реакции нуклеофильного замещения могут быть реализованы по механизмам бимолекулярного нуклеофильного замещения (SN2) или мономолекулярного нуклеофильного замещения (SNI).
Часто реакции, протекающие по механизму SNI, сопровождаются побочными реакциями мономолекулярного нуклеофильного отщепления Е I. Скорость-определяющей стадией реакции, протекающей по механизму SNI, является диссоциация алкилгалогенида на ионы
![]()
Завершающей стадией является быстрое взаимодействие образующегося карбкатиона с нуклеофилом:
![]()
В то же время, при достаточно сильных основных свойствах нуклеофила, последний может выполнять отщепляющую функцию по отношению к карбкатиону (ЕI):

Таким образом, соотношение продуктов замещения - отщепления определяется конкуренцией реакций (2) и (3). Ключевой стадией для обеих реакций (SN1 и Е1) является реакция (I). Скорость процесса в целом определяется скоростью этой стадии, а следовательно ее энергетическим барьером. Образование более стабильного карбкатиона в реакции (I) обсуловливает понижение ее барьера и, следовательно, более высокую скорость процесса в целом. Это, в конечном счете, определяет ряд реакционной способности алкилгалогенидов в реакциях SN1: ( R )3CHaI > ( R )2CHHaI > RCH2HaI и предпочтительное протекание по этому механизму реакций третичных алкилгалогенидов.
С другой стороны реакционная способность алкилгалогенида зависит от галогена в субстрате и возрастает в соответствии с уменьшением энергии диссоциации связей С-НаI в алкилгалогениде:
Энергия диссоциации связи С-НаI
C-F > C-Cl > C-Br > C-I
Скорость реакции SNI (EI)
R-F < R-Cl < R-Br < R-I
Поскольку в скорость-определяющей стадии нуклеофил :Nu не участвует, природа и концентрация последнего не оказывают влияния на скорость процесса.
В бимолекулярном нуклеофильном замещении SN2 происходит синхронный разрыв связи С-Наl и образование связи С-Nu
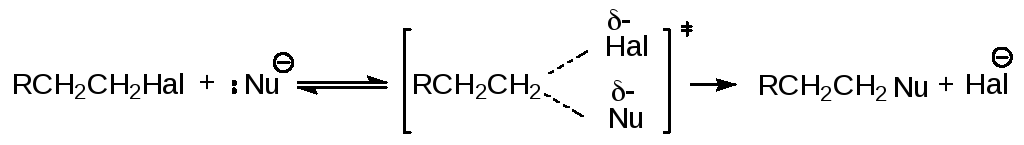
Как правило, эта реакция сопровождается конкурентной реакцией нуклеофильного отщепления Е2

И в SNI и в SN2 - реакциях соотношение продуктов замещения и отщепления определяется соотношением поляризуемости и основности в нуклеофиле.
Как правило, если атакующим агентом при реализации SN2–механизма является нуклеофил-анион, то электроноакцепторные заместители при атакуемом углероде ускоряют процесс, а электронодонорные - наоборот.
Реакционная способность различных галогенидов в бимолекулярном нуклеофильном замещении увеличивается в соответствии с уменьшением энергии диссоциации связей С-НаI, как и в случае SNI, поскольку в обоих случаях разрыв связей С-НаI происходит на скорость-определяющей стадии.
Реакция SN2 протекает в одну стадию с участием нуклеофила, поэтому его сила и концентрация оказывает ускоряющее действие на процесс.
Реакция замещения позволяют перейти от алкилгалогенидов ко многим классам органических соединений:

Важнейшими реакциями нуклеофильного отщепления (Е) является дегидратация спиртов, дегидрогалогенирование с образованием алкенов, алкинов и др.
Галогенопроизводные углеводородов находят применение в препаративной органической химии и в промышленном органическом синтезе (ядохимикаты, растворители и др.).
