
- •Содержание
- •2. Классификация органических соединений.
- •3. Соединения с открытой цепью.
- •3.1. Углеводороды
- •3.1.1. Алканы
- •3.1.2. Алкены или олефины (соединения этиленового ряда).
- •3.1.3. Углеводороды с двумя двойными связями (алкадиены).
- •3.1.4. Алкины (ацетиленовые углеводороды).
- •3.2. Производные углеводородов.
- •3.2.1. Галогенопроизводные алканов.
- •3.2.2. Металлоорганические соединения.
- •3.2.3. Спирты.
- •3.2.4. Простые эфиры.
- •3.2.5. Нитросоединения.
- •3.2.6. Амины.
- •3.2.7. Альдегиды и кетоны.
- •3.2.8. Карбоновые кислоты.
- •4. Карбоциклические соединения.
- •4.1. Алициклические соединения.
- •4.2. Ароматические соединения.
- •4.2.1. Ароматические углеводороды ряда бензола.
- •4.2.2. Галогенопроизводные аренов.
- •4.2.3. Ароматические сульфокислоты.
- •4.2.4. Ароматические нитросоединения.
- •4.2.5. Ароматические амины.
- •4.2.6. Диазо- и азосоединения.
- •4.2.7. Фенолы.
- •4.2.8. Ароматические альдегиды и кетоны.
- •4.2.9. Ароматические карбоновые кислоты.
- •4.2.10. Ароматические соединения с конденсированными ядрами.
- •5. Полимеры.
- •5.1. Полимеры, получаемые методом поликонденсации.
- •5.2. Полимеры, получаемые методом полимеризации.
- •6. Указания к выполнению контрольных работ.
- •7. Типовые задачи и их решение.
- •8. Контрольные задания
- •8.1. Контрольная работа 1.
- •8.2. Контрольная работа 2.
- •8.3. Контрольная работа 3.
4.2.6. Диазо- и азосоединения.
Ароматическими
диазосоединениями называют различные
по строению, однако легко взаимопревращаемые
соединения: соли диазония
![]() ,
диазогидраты
,
диазогидраты![]() ,
диазотаты
,
диазотаты![]() .
.
Реакцию образования диазосоединений из аминов называют диазотированием. Диазотирование проводят действием на водный раствор амина азотистой кислоты, получаемой из ее солей, в присутствии избытка минеральной кислоты (2,5 эквивалента).
Превращения диазосоединений могут протекать:
с выделением азота;
без выделений азота.
Первый тип реакции используют для получения ароматических соединений различных классов с функцией в ароматическом ядре. Ко второму типу реакций относятся реакции восстановления, окисления и азосочетания.
Реакции азосочетания легко идут при действии солей диазония на фенолы в слабощелочном растворе и ароматические амины в слабокислом растворе. Эти реакции протекают по механизму электрофильного замещения. Азосоединения лежат в основе обширной группы красителей, цвет и оттенки которых создаются сочетанием различных диазо- и азосоставляющих. Эти красители отличаются разнообразием окраски и обладают хорошими окрашивающими свойствами.
4.2.7. Фенолы.
Ароматические оксисоединения разделяются на две группы: фенолы и ароматические спирты. В фенолах гидроксильная группа связана непосредственно с ядром. Ароматические спирты содержат гидроксильную группу в боковой цепи и по многим свойствам они идентичным алифатическим спиртам.
Необходимо изучить способы получения фенолов: сплавление солей сульфокислот со щелочами; гидролиз галогенпроизводных; разложение гидропероксидов алкиларенов; окислительное декарбоксилирование аренкарбоновых кислот; из ароматических аминов.
В фенолах свободная р-электронная пара атома кислорода гидроксила делокализуется за счет сопряжения ее с электронной системой кольца. Это приводит к ослаблению связи О-Н и обусловливает кислотные свойства фенолов:

Ф![]() енолы
ведут себя как слабые кислоты. Они
взаимодействуют со щелочами, образуя
феноляты:
енолы
ведут себя как слабые кислоты. Они
взаимодействуют со щелочами, образуя
феноляты:
Кислотные свойства фенолов усиливаются при наличии в их кольце электроноакцепторных заместителей; так, тринитрофенол (пикриновая кислота) является сильной кислотой.
К реакциям фенольного гидроксила относятся также реакции алкилирования по кислородному атому с помощью галогенпроизводных или диазометана (CH2N2) и реакция ацилирования с помощью ангидридов или галогенангидридов кислот. Фенольный гидроксил ускоряет реакции электрофильного замещения в ароматическом кольце: галогенирование, нитрование, сульфирование. По такому же механизму протекают реакции конденсации фенола с алифатическими альдегидами в щелочной и кислой среде. На использовании этих реакций основано получение фенолформальдегидных смол резольного и новолачного типов.
4.2.8. Ароматические альдегиды и кетоны.
Ароматические альдегиды и кетоны - это соединения с карбонильной группой, связанной с атомом углерода бензольного кольца или боковой цепи.
Ароматические альдегиды и кетоны получают гидролизом геминальных арилалкилдигалогенидов; окислением углеводородов и ароматических спиртов; по реакции Гаттермана-Коха (прямое введение альдегидной группы); при конденсации ароматических альдегидов по Кляйзену и по реакции Фриделя-Крафтса (ацилирование):
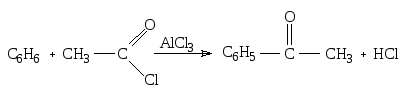
Ароматические альдегиды вступают в большинство реакций, свойственных альдегидам алифатического ряда, имеющим третичный -углеродный атом. Однако есть отличающие их особенности: самопроизвольное окисление альдегидов на воздухе; реакция бензоиновой конденсации; реакция Кляйзена (конденсация с альдегидами оснований); реакция Перкина (конденсация с ангидридами кислот в присутствии уксусного ангидрида); конденсация альдегидов с фенолами.
В то же время ароматические альдегиды неспособны выступать в качестве метиленовой компоненты в реакциях альдольной конденсации.
Альдегидная группа является электроноакцепторной группой и дезактивирует ароматическое кольцо в реакциях электрофильного замещения (SЕ), способствуя м-ориентации.
Ароматические кетоны менее реакционноспособны, чем кетоны алифатического ряда. Они легко вступают в реакции с гидроксиламином, фенилгидразином, в реакции со сложными эфирами, ангидридами кислот и т.д. Несимметричные алкилароматические и ароматические кетоны с гидроксиламином образуют по два изомерных оксима -син- и -анти-.
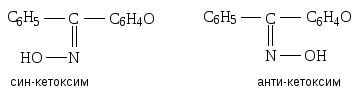
Более стойкой является анти-форма. Под действием сильных минеральных кислот оксимы перегруппировываются в амиды кислот. Эта перегруппировка называется перегруппировкой Бекмана.
Кетонная группы дезактивирует кольцо в реакциях электрофильного замещения и является для них м-ориентантом.
