
- •1. Теория электролитической диссоциации
- •1.1. Примеры решения задач
- •2. Растворы сильных электролитов. Активность электролитов
- •2.1. Примеры решения задач
- •2.2. Задачи для самостоятельного решения
- •3. Ионное произведение воды. Водородный показатель
- •3.1. Примеры решения задач
- •3.2. Задачи для самостоятельного решения
- •4. Растворы солей в воде и их гидролиз
- •4.1. Примеры решения типовых задач
- •4.2. Задачи для самостоятельного решения
- •5. Труднорастворимые соли. Произведение растворимости
- •5.1. Примеры решения типовых задач
- •5.2. Задачи для самостоятельного решения
- •6. Окислительно-восстановительные реакции
- •6.1. Определение коэффициентов уравнений окислительно-восстановительных реакций методом электронного баланса
- •6.2. Определение коэффициентов уравнений окислительно-восстановительных реакций методом ионно-электронного баланса
- •6.3. Задачи для самостоятельного решения
- •7. Электропроводность растворов электролитов. Числа переноса
- •7.1. Примеры решения задач
- •7.2. Задачи для самостоятельного решения
- •8. Электрохимические процессы на электродах. Типы электродов. Электродный потенциал
- •8.1.Примеры решения задач
- •8.2. Задачи для самостоятельного решения
- •9. Электролиз. Законы Фарадея
- •9.1. Примеры решения задач
- •9.2. Задачи для самостоятельного решения
- •10. Химические источники тока
- •10.1. Примеры решения задач
- •10.2. Задачи для самостоятельного решения
- •Библиографический Список
- •Приложения
- •Оглавление
2.2. Задачи для самостоятельного решения
1. Определить активность ионов Mn2+и Cl–в растворе, содержащем 0,005 моль/л CuSO4, 0,003 моль/л MnSO4и 0,005 моль/л CaCl2.
Ответ:
![]()
2. Молярная концентрация раствора соли
Na3PO4равна 0,02 моль/л,
средний ионный коэффициент активности![]() .
Определить активность электролита.
.
Определить активность электролита.
Ответ: 3,6410–8моль/л.
3. Какова активность ионов Ca2+, Cl–, K+и CH3COO–в 0,0001 М растворе CaCl2, к которому добавили столько CH3COOK, что ионная сила раствора стала равной 0,2?
Ответ: 1,18410–4; 1,2210–5; 0,1184 моль/л
4. На сколько изменится активность иона
![]() в 0,001 М растворе NH4Cl, если в этот
раствор будет добавлена соль Fe2(SO4)3до концентрации 0,01 моль/л?
в 0,001 М растворе NH4Cl, если в этот
раствор будет добавлена соль Fe2(SO4)3до концентрации 0,01 моль/л?
Ответ: 34,2%.
5. Вычислить активность ионов в растворе, содержащем 0,006 М CuSO4, 0,01 MNa2SO4и 0,005MAl2(SO4)3.
Ответ:
![]()
![]()
6. Растворимость соли AgI при 25 С составляет 2,1410–6г/л. Определить произведение растворимости.
Ответ: 8,3110–17(моль/л)2.
7. Растворимость соли Ag3PO4в воде при 25С равна 6,710–3г/л. Определить, во сколько раз увеличится растворимость этой соли, если к насыщенному раствору Ag3PO4прибавить соль KNO3до концентрации 0,1 моль/л.
Ответ: 2,8 раза.
8. Растворимость Ag2CO3 при 25 С в воде составляет 3,510–2 г/л. Определить, во сколько раз уменьшится растворимость соли Ag2CO3 в 0,1 М растворе Na2CO3.
Ответ: 4,1 раза.
9. Произведение растворимости CaSO4 при 25 С равно 9,110–8 (моль/л)2.Определить: 1) во сколько раз понизится растворимость CaSO4 в 0,05 н растворе Na2SO4; 2) во сколько раз повысится растворимость CaSO4 в 0,025 н растворе NaCl.
Ответ: 6,4; 2,1.
10. Произведение растворимости Ba3(PO4)2 при 25 С равно 610–39 (моль/л)5. Определить: 1) во сколько раз понизится растворимость Ba3(PO4)2 в 0,3 н растворе Na3PO4; 2) во сколько раз повысится растворимость Ba3(PO4)2 в 0,08 н растворе MgCl2.
Ответ: 7,7; 11,4.
11. Определить
активность и среднюю активность
![]() в 0,01-моляльном растворе, если
в 0,01-моляльном растворе, если![]() = 0,148.
= 0,148.
Ответ:
![]() = 2,19·10–4;
= 2,19·10–4;![]() = 1,48·10–2.
= 1,48·10–2.
12. Определить активность
![]() в 0,01-моляльном растворе, если средний
коэффициент активности
в 0,01-моляльном растворе, если средний
коэффициент активности![]() = 0,571.
= 0,571.
Ответ: 2,87·10–8.
13. Определить ионную силу раствора,
содержащего 0,01 моля
![]() и 0,02 моля
и 0,02 моля![]() в 1000 г воды.
в 1000 г воды.
Ответ: 0,11.
14. Ионная сила раствора
![]() равна 0,2. Какова молярность этого
раствора? Какой должна быть молярность
водного раствора
равна 0,2. Какова молярность этого
раствора? Какой должна быть молярность
водного раствора![]() ,
чтобы ионная сила раствора была такой
же?
,
чтобы ионная сила раствора была такой
же?
Ответ: 0,2 и 0,0666 моль/л.
15. Определить коэффициент активности
водородного иона в растворе, содержащем
0,01 моля
![]() ,
0,001 моля
,
0,001 моля![]() и 0,001 моля
и 0,001 моля![]() в 1000 г воды.
в 1000 г воды.
Ответ: 0,86.
16. Определить средний коэффициент
активности
![]() (
(![]() )
в растворе, содержащем 0,001 моля
)
в растворе, содержащем 0,001 моля![]() и 0,005 моля
и 0,005 моля![]() в 1000 г воды. Использовать для решения
предельный закон Дебая–Гюккеля, считаяА= 0,509.
в 1000 г воды. Использовать для решения
предельный закон Дебая–Гюккеля, считаяА= 0,509.
Ответ: 0,6.
17. Определить активность
![]() в водном растворе, моляльность которого
в водном растворе, моляльность которого![]() = 0,02 и
= 0,02 и![]() = 0,894.
= 0,894.
Ответ: 3,197·10–4.
18. Средний коэффициент активности
![]() в растворе, моляльность которого
в растворе, моляльность которого![]() = 0,01
= 0,01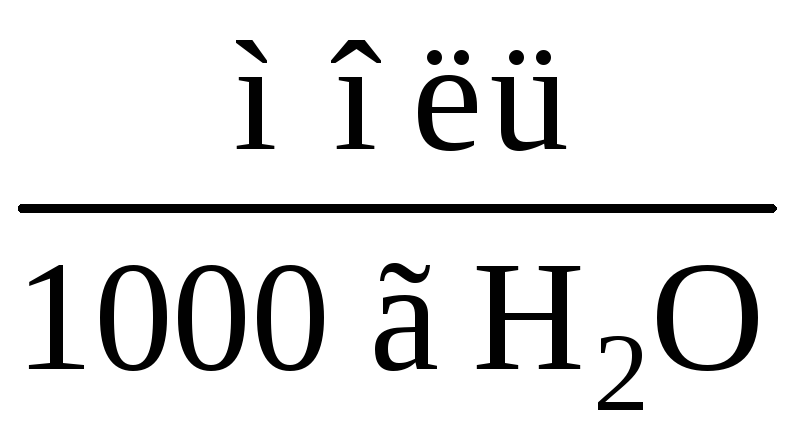 ,
равен 0,922. Средний коэффициент активности
,
равен 0,922. Средний коэффициент активности![]() при
при![]() = 0,01
= 0,01 равен 0,916. Определить
коэффициент активности иона
равен 0,916. Определить
коэффициент активности иона
![]() ,
если
,
если![]() .
.
Ответ: 0,91.
19. Растворимость
![]() в воде равна 8·10–4моль/л. Определить
произведение растворимости
в воде равна 8·10–4моль/л. Определить
произведение растворимости![]() :
а) считая
:
а) считая![]() = 1; б) используя для решения предельный
закон Дебая–Гюккеля и считаяА=
0,509.
= 1; б) используя для решения предельный
закон Дебая–Гюккеля и считаяА=
0,509.
Ответ: 2,048·10–9и 1,45·10–9.
20. Определить
растворимость
![]() а) в чистой воде; б) в растворе, содержащем
0,001 моль
а) в чистой воде; б) в растворе, содержащем
0,001 моль![]() в 1000 г воды; в) в растворе, содержащем
0,1 моль
в 1000 г воды; в) в растворе, содержащем
0,1 моль![]() в 1000 г воды. Произведение растворимости
в 1000 г воды. Произведение растворимости![]() равно 1,56·10–10
(моль/л)2.
Считать А=0,509.
равно 1,56·10–10
(моль/л)2.
Считать А=0,509.
Ответ: 1,25·10–5; 1,7·10–7и 2,56·10–9моль/л.
21. Во сколько раз растворимость
![]() в 0,01-моляльном растворе
в 0,01-моляльном растворе![]() больше растворимости в чистой воде?
больше растворимости в чистой воде?
Ответ: . 1,55.
22. Произведение растворимости
![]() равно 9·10–12(моль/л)3.
Какова растворимость
равно 9·10–12(моль/л)3.
Какова растворимость![]() в растворе
в растворе![]() ,
молярность которого 0,01?
,
молярность которого 0,01?
Ответ: 2,57·10–5моль/л.
23. Произведение растворимости
![]() равно 1,36·10–9(моль/л)3.
Какова растворимость этой соли в водном
растворе
равно 1,36·10–9(моль/л)3.
Какова растворимость этой соли в водном
растворе![]() ,
молярность которого 0,1, и в растворе
,
молярность которого 0,1, и в растворе![]() ,
молярность которого 0,03?
,
молярность которого 0,03?
Ответ: 1,21·10–3и 2,3·10–4моль/л.
24. С помощью
предельного закона Дебая–Гюккеля найти
средний коэффициент активности
![]() в растворе, молярность которого 0,001,
еслиА
= 0,509.
в растворе, молярность которого 0,001,
еслиА
= 0,509.
Ответ: 0,76.
