
- •1. Теория электролитической диссоциации
- •1.1. Примеры решения задач
- •2. Растворы сильных электролитов. Активность электролитов
- •2.1. Примеры решения задач
- •2.2. Задачи для самостоятельного решения
- •3. Ионное произведение воды. Водородный показатель
- •3.1. Примеры решения задач
- •3.2. Задачи для самостоятельного решения
- •4. Растворы солей в воде и их гидролиз
- •4.1. Примеры решения типовых задач
- •4.2. Задачи для самостоятельного решения
- •5. Труднорастворимые соли. Произведение растворимости
- •5.1. Примеры решения типовых задач
- •5.2. Задачи для самостоятельного решения
- •6. Окислительно-восстановительные реакции
- •6.1. Определение коэффициентов уравнений окислительно-восстановительных реакций методом электронного баланса
- •6.2. Определение коэффициентов уравнений окислительно-восстановительных реакций методом ионно-электронного баланса
- •6.3. Задачи для самостоятельного решения
- •7. Электропроводность растворов электролитов. Числа переноса
- •7.1. Примеры решения задач
- •7.2. Задачи для самостоятельного решения
- •8. Электрохимические процессы на электродах. Типы электродов. Электродный потенциал
- •8.1.Примеры решения задач
- •8.2. Задачи для самостоятельного решения
- •9. Электролиз. Законы Фарадея
- •9.1. Примеры решения задач
- •9.2. Задачи для самостоятельного решения
- •10. Химические источники тока
- •10.1. Примеры решения задач
- •10.2. Задачи для самостоятельного решения
- •Библиографический Список
- •Приложения
- •Оглавление
6.2. Определение коэффициентов уравнений окислительно-восстановительных реакций методом ионно-электронного баланса
Используя метод электронного баланса, можно определить коэффициенты в уравнении ОВ реакций при окислителе, восстановителе, восстановленной и окисленной формах. Однако, недостатком этого методаявляется формальное понятие атомного иона и степени его окисления и игнорирование существования в растворах реальных многоатомных ионов, умалчивание механизма протекания химических превращений.
В методе ионно-электронных уравнений используются только реально существующие ионы, а труднорастворимые соединения, малодиссоциирующие электролиты и газообразные вещества записываются в молекулярной форме (из-за этого встречается название «метод молекулярно-ионных уравнений»). Это позволяет определить коэффициенты не только у окислителя и восстановителя. Ионно-электронные схемы удобно применять для реакций с участием веществ, в которых трудно определить степени окисления элементов, например, KCNS.
Ионно-электронные схемы составляются по разному в зависимости от характера среды.
Реакции в кислой среде
Если ОВ реакция идет в среде, содержащей сильную кислоту, то в полуреакциях рационально использовать ионы водорода и молекулы воды.
Если у соединения нужно отнять атом кислорода, то его связывают ионами водорода в молекулу воды:
ЭОn+ 2Н+ЭОn-1+H2O,
а если нужно добавить атом кислорода, то его «отбирают» у молекулы воды, при этом высвобождаются два иона водорода:
ЭОn+H2OЭОn+1+ 2Н+.
Следует отметить, что эти схемы иллюстрируют лишь переход кислорода, но не отражает баланс зарядов в левой и правой частях полуреакций.
Пример 30.При окислении сульфита натрия азотной кислотой образуется сульфат натрия и оксид азота (II):
Na2SO3 + HNO3 Na2SO4 + NO +… .
Составить уравнение реакции.
Решение
Составляем схемы перехода электронов:
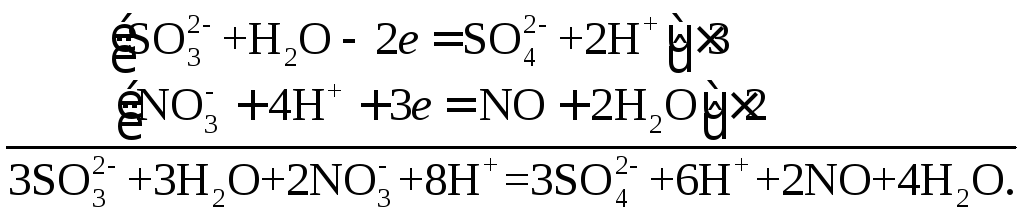
После приведения подобных слагаемых в данном уравнении уравнение реакции примет вид:
3Na2SO3 + 2HNO3 = 3Na2SO4 + 2NO + H2O.
Реакции в щелочной среде
В этом случае в ионно-электронных полуреакциях целесообразно применять только гидроксид-ионы и молекулы воды.
Если у соединения нужно отнять атом кислорода, то добавляют молекулу воды и освобождаются два гидроксид-иона ОН:
ЭОn+H2OЭОn-1+ 2OН.
Если нужно добавить атом кислорода, то добавляют 2 иона OНи получают молекулу воды
ЭОn+ 2OНЭОn+1+H2O.
Пример 31. При окислении сульфата железа (II) пероксидом водорода в среде КОН получают гидроксид железа (III) и сульфат калия:
FeSO4 + H2O2 + KOH Fe(OH)3 + K2SO4.
Составить уравнение реакции.
Решение
Ионно-электронные схемы таковы:
[Fe2+ + 3OH – e = Fe(OH)3]2
[H2O2 + 2e = 2OН]1
2 Fe2+
+ 6OH
+ H2O2
= 2Fe(OH)3
+ 2OН,
Fe2+
+ 6OH
+ H2O2
= 2Fe(OH)3
+ 2OН,
2Fe2+ + 4OH + H2O2 = 2Fe(OH)3.
Окончательно уравнение реакции принимает вид:
2FeSO4 + H2O2 + 4KOH = 2Fe(OH)3 + 2K2SO4.
Пример 32. При окислении серы в средеNaOHгипохлоритом натрия получают сульфат натрия и хлорид натрия:
S + NaClO + NaOH Na2SO4 + NaCl + … .
Составить уравнение реакции.
Решение
Ионно-электронные схемы такие:
[S
+ 8OН
– 6e =
![]() + 4H2O]1
+ 4H2O]1
[ClO + H2O +2e = Cl + 2OH]3
S + 3ClO
+2OH
=
+ 3ClO
+2OH
=
![]() + 3Cl
+ H2O.
+ 3Cl
+ H2O.
Окончательно уравнение реакции принимает вид
S + 3NaClO + 2NaOH = Na2SO4 + 3NaCl + H2O.
Реакции в нейтральной среде
В этом случае в ионно-электронных схемах в левую часть полуреакций надо добавлять только воду.
При этом, если нужно отнять кислород, то добавляют молекулу воды и получают два гидроксид-иона:
ЭОn+H2OЭОn-1+ 2OН,
а если нужно добавить кислород, то добавляют тоже молекулу воды и получают два иона водорода:
ЭОn+H2OЭОn+1+ 2Н+.
В правой части, если есть и ионы водорода, и гидроксид-ионы, то они образуют воду.
Пример 33. При окислении сульфита натрия перманганатом калия получают сульфат натрия и оксид марганца (IV):
Na2SO3 + KMnO4 = Na2SO4 + MnO2 + … .
Составить уравнение реакции.
Решение
Ионно-электронные схемы такие:
[![]() +H2O– 2е=
+H2O– 2е=![]() +
2Н+]3
+
2Н+]3
[![]() + 2H2O+3е=
+ 2H2O+3е=![]() + 4OН]2
+ 4OН]2
3
![]() + 2
+ 2![]() + 3H2O+ 4H2O= 3
+ 3H2O+ 4H2O= 3![]() + 2
+ 2![]() + 6Н++ 8OН.
+ 6Н++ 8OН.
После приведения подобных слагаемых получаем уравнение в ионно-молекулярной форме
3![]() + 2
+ 2![]() +H2O= 3
+H2O= 3![]() + 2
+ 2![]() + 2OН.
+ 2OН.
Окончательно уравнение реакции принимает вид:
3Na2SO3 + 2KMnO4 + H2O = 3Na2SO4 + 2MnO2 + 2КOН.
