
- •Особенности водно-электролитного баланса организма человека
- •Осмоляльность и коллоидно-осмотическое давление
- •Гипертоническая дегидратация
- •Изотоническая дегидратация
- •Гипотоническая дегидратация
- •Гипотоническая гипергидратация
- •Изотоническая гипергидратация
- •Гипертоническая гипергидратация
- •Нарушение обмена натрия
- •Нарушение обмена калия
- •Нарушение обмена хлора
- •Кислотно-основное состояние и его нарушение
- •Определение кислот и оснований
- •Буферные системы организма
- •Основные показатели кислотно-основного состояния
- •Метаболический ацидоз
- •Респираторный ацидоз
- •Метаболический алкалоз
- •Респираторный алкалоз
Основные показатели кислотно-основного состояния
Процессы, обеспечивающие поддержание кислотно-основного состояния в организме, можно оценить с помощью следующих показателей:
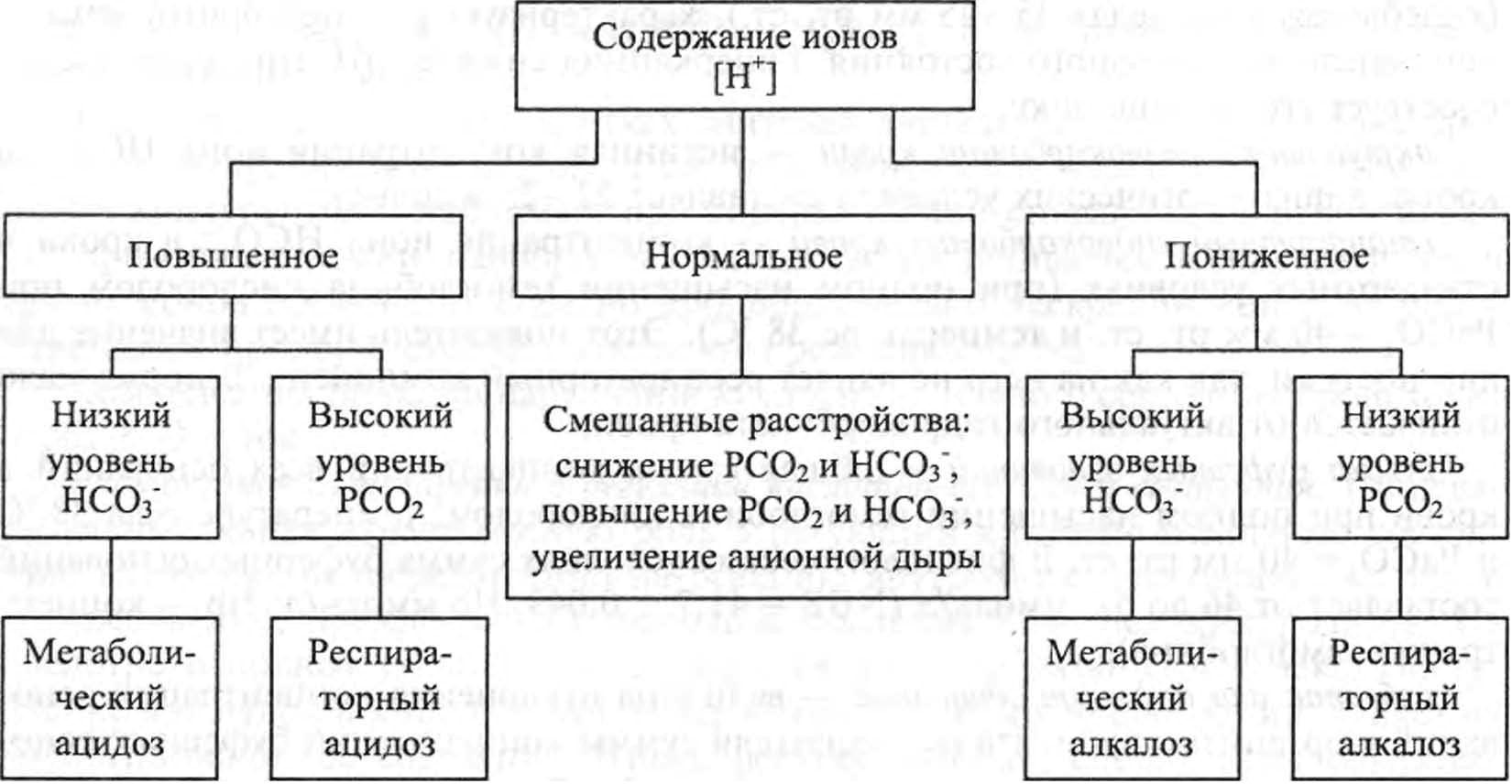
pH раствора — чаще всего измеряется в крови. В норме колеблется от 7,35 до 7,45, его снижение свидетельствует о сдвиге реакции раствора в кислую сторону, и наоборот, повышение — о сдвиге реакции раствора в сторону оснований;
парциальное давление, или напряжение диоксида углерода в крови (РаС02), в норме в физиологических условиях при нормальной вентиляции равно 40 мм. рт. ст.(колеблется в пределах 35—45 мм рт. ст.), характеризует респираторный компонент кислотно-основного состояния. Гиперкапния снижает pH, гипокапния способствует его повышению;
актуальный гидрокарбонат крови — истинная концентрация иона НС03- в крови, в физиологических условиях составляет 22—25 ммоль/л;
стандартный гидрокарбонат крови — концентрация иона НС03- в крови в стандартных условиях (при полном насыщении гемоглобина кислородом при РаС02 = 40 мм рт. ст. и температуре 38 °С). Этот показатель имеет значение для диагностики, так как на него не влияет респираторный компонент. В норме мало отличается от актуального гидрокарбоната крови;
сумма буферных оснований — общая сумма концентраций всех оснований в крови при полном насыщении гемоглобина кислородом, температуре тела 38°С и РаС02 = 40 мм рт. ст. В физиологических условиях сумма буферных оснований составляет от 46 до 52 ммоль/л (NВВ = 41,7 + 0,043 • Нb ммоль/л; Нb — концентрация гемоглобина);
избыток или дефицит оснований — величина отклонения концентраций оснований в организме пациента от показателя суммы концентраций буферных оснований в норме, рассчитывается как разность между показателем суммы концентраций буферных оснований и фактическим их показателем в организме пациента. Таким образом, если сумма концентраций буферных оснований в норме больше, чем фактическая их сумма, то это свидетельствует о дефиците оснований, если же меньше — об их избытке. Этот показатель характеризует метаболический компонент кислотно-основного состояния. В норме избыток или дефицит основ составляет ± 2,5 ммоль/л.
Терминология, применяемая при исследовании кислотно-основного состояния. Снижение pH крови ниже 7,35 определяется как ацидемия, или ацидоз, повышение pH свыше 7,45 — как алкалемия, или алкалоз. Для ацидоза и алкалоза часто используют дополнительное определение, характеризующее генез этих процессов, — респираторный или метаболический. Если расстройства кислотно-основного состояния связаны с нарушением выделения С02, то они являются респираторными, с нарушением выведения или образования кислот или оснований — метаболическими, или нереспираторными. Приоритет в определении зависит от первичности процесса.
Метаболический ацидоз
Декомпенсированный метаболический ацидоз проявляется снижением pH ниже 7,35 и показателя уровня оснований в крови (стандартный гидрокарбонат крови и избыток или дефицит оснований). Определение этиологического фактора метаболического ацидоза гораздо сложнее чем респираторного. Важную роль при этом играет диагностика основного заболевания, тем не менее и показатели нарушения кислотно-основного состояния в сочетании с биохимическими могут оказать серьезную помощь в диагностике основного заболевания.
По этиопатогенезу можно выделить два типа метаболического ацидоза: с нормальной и увеличенной анионной дырой.
Анионная дыра (anion gamp): один из универсальных принципов существования живого организма — поддержание его электронейтральности. Это означает, что суммарный заряд анионов в организме должен равняться суммарному заряду катионов в нем. Основными внеклеточными катионами является натрий и калий, а анионами — хлор и гидрокарбонат-ион. Таким образом, суммарный заряд Na++ К+должен быть равен суммарному заряду Сl-+ НС03-. Существует группа анионов, концентрация которых не определяются обычными исследованиями. Эти анионы и обуславливают возникновение анионной дыры (AG), которая, таким образом, составляет:
AG = суммарный заряд (Na+ + К+) - суммарный заряд (Сl- + НС03-).
Анионную дыру образуют отрицательно заряженные ионы, образующиеся при отщеплении ионов водорода от молекул белков, прежде всего альбумина (15 мЭкв/л), ионы кислотных остатков органических кислот (5 мЭкв/л), фосфатов (2 мЭкв/л) и сульфатов (1 мЭкв/л) — всего 23 мЭкв/л. Тем не менее, необходимо учитывать и заряды катионов, которые обычно не учитываются, — кальций (5 мЭкв/л), магний (1,5 мЭкв/л). Поэтому в норме AG = 10—16 мЭкв/л (не превышает 20 мЭкв/л).
Увеличение анионной дыры свидетельствует о наличии метаболического ацидоза. Наиболее частыми причинами увеличения являются повышение уровня лактата в крови (при гипоксии тканей), а также кетонемия (при сахарном диабете, голодании), отравление салицилатами, уремия. Это может быть связано со снижением экскреции почками неорганических кислот (серной, фосфорной). Такое явление часто отмечается при хронической почечной недостаточности, когда нарушается еще и экскреция аммония хлорида. Как правило, при этом концентрация НС03_ в крови снижается до 16 ммоль/л и ниже. Причиной увеличения анионной дыры может быть интоксикация спиртами (этанолом, метанолом, эти- ленгликолем).
Наиболее частыми причинами развития метаболического ацидоза с нормальной анионной дырой являются большие потери гидрокарбоната. При этом возрастает концентрация хлоридов, и анионная дыра может не изменяться (это происходит в тех случаях, когда в проксимальных канальцах нарушается реабсорбция гидрокарбоната, а также при его потерях через пищеварительный тракт, при гемодилюции кислыми растворами). При расстройстве функции дистальных канальцев возникает нарушение регенерации НС03- в результате реабсорбции ионов водорода с возвращением их в кровь. При гипоальдостеронизме, что часто сочетается с интерстициальным поражением почек, отмечается снижение реабсорбции натрия и секреции дистальными канальцами водорода, развивается гиперхлоремический гиперкалиемический ацидоз. Сходные нарушения могут возникнуть при продолжительном применении в высоких дозах таких диуретиков, как триамтерен, спиронолактон и амилорид. Коррекция проксимального канальцевого ацидоза применением растворов гидрокарбоната приводит к дальнейшему увеличению его выведения с мочой.
Дилюционный ацидоз возникает при переливании больших количеств растворов с pH < 7,4. Применение ингибиторов карбоангидразы вызывает снижение реабсорбции НС03_ в почечных канальцах, а первичный гиперпаратироидизм снижает гидрокарбонатный барьер в проксимальных канальцах и приводит к увеличению концентрации хлоридов.
Поскольку в содержимом кишечника наблюдается повышенное количество НС03-, понос или кишечные свищи вызывают значительную потерю этих ионов с развитием ацидоза (некоторые авторы называют его выделительным). Понос, не превышающий 1 л в сутки, как правило, не сопровождается тяжелыми нарушениями кислотно-основного состояния из-за почечной компенсации ионов НС03 (почки могут генерировать 200 ммоль/л через сутки). Пациенты с уретросигмостомой теряют НС03- с мочой, вымывающей его из содержимого кишки.
Причиной гиперхлоремического ацидоза может быть также употребление в большом количестве солей, образованных сильной кислотой и слабым основанием, — аммония гидрохлорида, лизина гидрохлорида, аргинина гидрохлорида. В процессе их метаболизма образуется соляная кислота. Часто гиперхлоремический ацидоз возникает при парентеральном введении большого объема растворов синтетических аминокислот со значительным содержанием аргинина, лизина, гистидина.
Клиническая картина. Метаболический ацидоз может проявляться нарушением функции центральной нервной системы вплоть до коматозного состояния, при снижении pH < 7,1 отмечается артериальная гипотензия вследствие кардиодепрессивного эффекта, повышается давление в легочных артериях, снижается чувствительность к катехоламинам.
Механизмы компенсации метаболического ацидоза. Компенсация метаболического ацидоза происходит прежде всего за счет увеличения вентиляции легких и снижения РаС02. В норме в ответ на снижение содержания НС03- на 1 ммоль РаС02 должно снизиться на 1,2 мм рт. ст. Если этот показатель снижается еще более, можно допускать наличие дополнительного респираторного ацидоза. Обычно и в случае тяжелейшего метаболического ацидоза РаС02 не опускается ниже 10 мм рт. ст.
Лечение. Прежде всего необходимо определить первичный патофизиологический процесс и проводить его терапию. Например, при лактатацидозе следует улучшить доставку кислорода тканям, при кетоацидозе — нормализовать жировой и водно-электролитный обмен. Тем не менее при критическом снижении pH ниже 7,2—7,1 требуется срочная коррекция кислотно-основного состояния. Обычно с этой целью используют ощелачиваемые растворы, в первую очередь раствор натрия гидрокарбоната (питьевой соды). Основной целью применения соды в большинстве случаев является нормализация гемодинамики при выраженной артериальной гипотензии за счет увеличения чувствительности адренорецепторов к экзогенным и эндогенным катехоламинам. Применение раствора натрия гидрокарбоната может вызвать такие неблагоприятные эффекты, как гиперна-триемия, гиперосмолярность, усиление внутриклеточного ацидоза, особенно нейронов головного мозга (за счет быстрого поступления С02 в спинномозговую жидкость и внутрь клетки). Передозировка натрия гидрокарбоната угрожает переходом метаболического ацидоза в метаболический алкалоз на фоне компенсаторного респираторного алкалоза со сдвигом кривой диссоциации оксигемоглобина ш1ево и еще большим дефицитом кислорода. При этом возможно развитие опасной для жизни гипокалиемии.
МЛ. Гальперин и М.Б. Гольдштейн (M.L. Halperin, М.В. Goldstein, 1994) предложили следующие показания к применению натрия гидрокарбоната:
при лактатацидозе: снижение концентрации НС03- до 8 ммоль/л, что сопровождается снижением сердечного выброса, артериальной гипотензией или недостаточной респираторной компенсацией;
при кетоацидозе: при наличии гиперкалиемии, несмотря на введение инсулина, при выраженном дефиците основ (НС03-< 5 ммоль/л), при выраженной гипергликемии, не корректирующейся с помощью инсулинотерапии.
При таких состояниях как гемоглобинурическая недостаточность почек или отравление салицилатами и некоторыми другими токсическими веществами применение натрия гидрокарбоната может быть одним из методов этиопатогенетического лечения. Положительный результат от применения раствора натрия гидрокарбоната следует ожидать при остром ацидозе, связанном с большой потерей ионов гидрогенкарбоната (понос, кишечные свищи). При определении показаний к применению натрия гидрокарбоната обязательно необходимо учитывать положительные и отрицательные его последствия.
Для первичного определения дозы натрия гидрокарбоната предложено несколько формул, например:
24 ммоль / л - актуальный НСО3 -
NaHCO3- = Масса тела · 0,3---------------------------------------------------.
2
Тем не менее сами исследователи отмечают, что выбор этой формулы, как и других, преимущественно имеет эмпирический характер, она годится только для начального применения с дальнейшим повторным определением показателей кислотно-основного состояния.
В качестве ощелачивающих растворов можно применять натрия лактат и натрия ацетат. Оба они метаболизируются в печени до ионов гидрокарбоната, поэтому по механизму действия мало отличаются от раствора натрия гидрокарбоната. При коррекции этими растворами снижается риск развития гипернатриемии, гиперосмолярности плазмы крови, внутриклеточного ацидоза, повышается уровень диоксида углерода; их действие более мягкое и продолжительное, чем раствора натрия гидрогенкарбоната. Противопоказано введение натрия лактата и натрия ацетата при недостаточности функции печени и дефиците лактатацидозы, что значительно ограничивает их применение.
Многие недостатки, свойственные раствору натрия гидрокарбоната, отсутствуют у трисамина, который является органическим акцептором ионов водорода как внутри, так и вне клетки. Это щелочной гиперосмолярный раствор, обеспечивающий осмодиуретический эффект, способствует снижению концентрации ионов калия в плазме крови. При быстром введении вызывает угнетение дыхания. Скорость внутривенной инфузии растворов триасмина не должна превышать 5 мл/кг в 1 ч. При попадании паравазально триасмин вызывает некроз клетчатки, что может послужить причиной дегидратации, особенно внутриклеточной.
Дозу 3,66% раствора трисамина (в мл) определяют как произведение показателей излишка или дефицита оснований в организме пациента и массы его тела. Препарат противопоказан при нарушении фильтрующей функции почек.
