
- •Домашние задания по химии и методические указания по их выполнению для студентов дневной формы обучения
- •Содержание
- •Введение
- •Раздел 1. Основные классы неорганических соединений
- •Раздел 2. Газовые законы. Закон Авогадро и следствия из него. Уравнение Клапейрона-Менделеева. Моль. Молярный объём газов.
- •Примеры решения задач 71-82.
- •Раздел 3. Эквиваленты. Нахождение формул вещества. Стехиометрические расчеты.
- •Раздел 4. Строение атома и периодическая система д.И. Менделеева.
- •Раздел 5. Химическая связь и строение молекул
- •Относительная электроотрицательность атомов
- •Типовые задачи с решениями по разделу 5.
- •Раздел 6 Термохимия. Элементы химической термодинамики.
- •Раздел 7.Окислительно-восстановительные реакции
- •Раздел 8 Скорость химической реакции. Химическое равновесие.
- •Примеры решения задач к разделу 8:
- •Раздел 9.Концентрации растворов. Коллигативные свойства растворов
- •Раздел 10. Растворы электролитов. Константа и степень диссоциации. Водородный показатель. Реакции ионного обмена. Произведение растворимости
- •Типовые задачи с решениями по разделу 10:
- •Раздел 11. Гидролиз солей. Обменные реакции в растворах электролитов
- •Раздел 12.Электродные потенциалы. Химические источники электрической энергии
- •Типовые задачи к разделу 12.
- •Раздел 13. Комплексные соединения
- •Содержание
- •Литература
Раздел 8 Скорость химической реакции. Химическое равновесие.
Вычислить, как изменится скорость реакции (401-410):
H2 (газ) + I2 (газ) → 2HI (газ), если увеличить концентрацию водорода в 2 раза, а концентрацию йода – в 4 раза
2SO3(газ) → 2SO2(газ) +O2(газ) при уменьшении концентрации реагента в 2,5 раза
2NO2(газ) → 2NO(газ) +O2(газ) при уменьшении концентрации реагента в 4 раза
2CO(газ) + O2(газ) → 2CO2(газ), если давление в системе повысить в 5 раз
2HBr(газ) → H2(газ) + Br2(газ), если давление в системе понизить в 4 раза
H2(газ) + CO2(газ) → H2O(газ) + CO(газ) при понижении давления в системе в 2,5 раза
2C(графит) + H2(газ) → C2H2(газ), если давление в системе повысить в 3,25 раза
FeO(тверд) + CO(газ) → Fe(тв) + CO2(газ), если концентрацию СО уменьшить с 26,22 до 0,69 моль/л
N2(газ) + 3H2(газ) → 2NH3(газ), если уменьшить объем системы в 2 раза
2NO(газ) + O2(газ) → 2NO2(газ) при уменьшении объема системы в 3 раза
Вычислить, как изменится скорость реакции (411-420):
При охлаждении системы от 90 ºС до 30 ºС, если температурный коэффициент равен 2.
При повышении температуры системы на 30 ºС, если температурный коэффициент равен 3.
При охлаждении системы на 40 ºС, если температурный коэффициент равен 3.
При повышении температуры системы на 20 ºС, если температурный коэффициент равен 2, 45.
При повышении температуры системы от 20 ºС до 60 ºС, если температурный коэффициент равен 4.
При охлаждении системы от 95 ºС до 65 ºС, если температурный коэффициент равен 2,7.
При охлаждении системы на 50 ºС, если температурный коэффициент равен 3,5.
Определить скорость реакции при 100ºС, если при 60ºС скорость этой реакции равна 4 моль/ч, а температурный коэффициент равен 3?
 Определить
скорость реакции при 30 ºС, если при 70
ºС скорость этой реакции равна 12 моль/ч,
а температурный коэффициент равен 2?
Определить
скорость реакции при 30 ºС, если при 70
ºС скорость этой реакции равна 12 моль/ч,
а температурный коэффициент равен 2?Определить скорость реакции при 80 ºС, если при 60 ºС скорость этой реакции равна 5 моль/ч, а температурный коэффициент равен 2,5?
Константа равновесия следующей реакции равна 0,1 при 673 К
|
N2(г)+ 3Н2 |
|
2NH3(г) |
Равновесные концентрации (моль/л): Н2=0,6 и NH3= 0,18. Вычислить начальную и равновесную концентрации азота .
Определить равновесную концентрацию водорода в реакции:
-
2НI

H2 + I2
Если исходная концентрация HI составляет 0,55моль/л, а константа равновесия Кравн=0,12.
При некоторой температуре константа равновесия термической диссоциации следующей реакции равна 0,26.
-
N2O4

2NO2
Равновесная концентрация [NO2]равн равна 0,28 моль/л. Вычислить равновесную и начальную концентрации [N2O4]равн. Сколько этого вещества (в процентах) продиссоциировало к моменту равновесия?
При синтезе фосгена имеет место равновесие реакции:
-
Cl2 + CO

COCl2
Определить исходные концентрации хлора и оксида углерода, если равновесные концентрации равны (моль/л): [Cl2]равн = 2,5; [CO]равн = 1,8; [COCl2]равн = 3,2.
Исходные концентрации [NO]исх и [Cl2]исх в гомогенной системе
|
2NO(г) + Cl2(г ) |
|
2NОCI(г) |
составляют соответственно 0,5 и 0,2 моль/л. Вычислить константу равновесия, если к моменту равновесия прореагировало 20% NO.
При некоторой температуре равновесие системы
-
2NO + O2
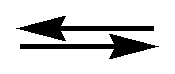
2NO2
установилось при следующих концентрациях реагирующих веществ (моль/л): [NO]равн = 0,2; [O2]равн = 0,1; [NO2]равн = 0,1. Вычислить константу равновесия Кр и исходные концентрации [NO]исх и [O2]исх
Константа равновесия гомогенной системы:
-
СО(г) + Н2О(г)
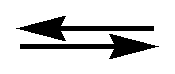
СО2(г) + Н2(г)
при некоторой температуре равна 1. Вычислить равновесные концентрации всех реагирующих веществ, если исходные концентрации (моль/л): [CO]исх = 0,1; [H2O]исх = 0,4.
Равновесие гомогенной системы
-
4HCl(г) + О2(г)

2Н2О(г) + 2Cl2(г)
установилось при следующих концентрациях реагирующих веществ (моль/л): [H2O]равн = 0,14; [Cl2]равн = 0,14; [HCl]равн = 0,20; [O2]равн = 0,32. Вычислить начальные концентрации исходных веществ [HCl]исх и [O2]исх.
В гомогенной системе:
-
СО(г) + Cl2(г)

СОСl2(г)
равновесные концентрации реагирующих веществ (моль/л): [CO]равн = 0,2; [Cl2]равн = 0,3; [COCl2]равн = 1,2. Вычислить константу равновесия Кр и начальные концентрации исходных веществ [CO]исх и [Cl2]исх.
В гомогенной газовой системе
-
А + В
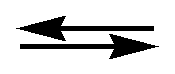
С + Д
равновесие установилось при концентрациях (моль/л): [B] = 0,05; [C] = 0,02. Константа равновесия Кр равна 0,04. Вычислить начальные концентрации исходных веществ [A]исх и [B]исх.
В какую сторону сместится равновесие реакции при уменьшении температуры, если энергии активации прямой и обратной реакций составляют Е1 и Е2 соответственно (431-440):
|
|
Е1 |
Е2 |
|
|
10 ккал/моль |
20000 кал/моль |
|
|
15 ккал/моль |
5·104 Дж/моль |
|
|
20 ккал/моль |
3·104 кал/моль |
|
|
25 ккал/моль |
30 кДж/моль |
|
|
30 ккал/моль |
100·103 Дж/моль |
|
|
35 ккал/моль |
100·106 Дж/кмоль |
|
|
80 кДж/моль |
27000 кал/моль |
|
|
90 кДж/моль |
15 ккал/моль |
|
|
100 кДж/моль |
15·103 ккал/кмоль |
|
|
1·105 кДж/кмоль |
20 ккал/моль |
В какую сторону сместится равновесие при увеличении давления, если константа равновесия выражается уравнением:
![]() (441-450):
(441-450):
|
|
a |
b |
c |
d |
|
|
1 |
2 |
2 |
2 |
|
|
2 |
2 |
2 |
1 |
|
|
2 |
0 |
1 |
1 |
|
|
0 |
1 |
1 |
2 |
|
|
1 |
1 |
1 |
2 |
|
|
2 |
1 |
0 |
1 |
|
|
0 |
1 |
1 |
0 |
|
|
1 |
2 |
0 |
2 |
|
|
1 |
1 |
1 |
0 |
|
|
2 |
1 |
2 |
2 |
