
- •Домашние задания по химии и методические указания по их выполнению для студентов дневной формы обучения
- •Содержание
- •Введение
- •Раздел 1. Основные классы неорганических соединений
- •Раздел 2. Газовые законы. Закон Авогадро и следствия из него. Уравнение Клапейрона-Менделеева. Моль. Молярный объём газов.
- •Примеры решения задач 71-82.
- •Раздел 3. Эквиваленты. Нахождение формул вещества. Стехиометрические расчеты.
- •Раздел 4. Строение атома и периодическая система д.И. Менделеева.
- •Раздел 5. Химическая связь и строение молекул
- •Относительная электроотрицательность атомов
- •Типовые задачи с решениями по разделу 5.
- •Раздел 6 Термохимия. Элементы химической термодинамики.
- •Раздел 7.Окислительно-восстановительные реакции
- •Раздел 8 Скорость химической реакции. Химическое равновесие.
- •Примеры решения задач к разделу 8:
- •Раздел 9.Концентрации растворов. Коллигативные свойства растворов
- •Раздел 10. Растворы электролитов. Константа и степень диссоциации. Водородный показатель. Реакции ионного обмена. Произведение растворимости
- •Типовые задачи с решениями по разделу 10:
- •Раздел 11. Гидролиз солей. Обменные реакции в растворах электролитов
- •Раздел 12.Электродные потенциалы. Химические источники электрической энергии
- •Типовые задачи к разделу 12.
- •Раздел 13. Комплексные соединения
- •Содержание
- •Литература
Раздел 10. Растворы электролитов. Константа и степень диссоциации. Водородный показатель. Реакции ионного обмена. Произведение растворимости
Вычислите кажущуюся степень диссоциации NaCl в 2 М растворе, если осмотическое давление раствора при 0 0С равно 68,1 атм.
Понижение давления пара, производимое растворением 12 г NaCl в 200 мл воды при 20 0С, равно 0,142 мм. рт. ст. При какой температуре замерзнет этот раствор?
Найдите изотонический коэффициент для раствора, содержащего 0,2 моль хлорида магния в 2000 г воды, зная, что этот раствор замерзает при -0,461 ºС.
Определите осмотическое давление 0,01 н MgSO4 при 18 0С, если кажущаяся степень диссоциации этого электролита равна 66%.
Одинаково ли осмотическое давление 1 М растворов следующих веществ: глюкозы С6Н12О6, уксусной кислоты СН3СООН и азотной кислоты HNO3? В растворе какого вещества осмотическое давление наибольшее и какое наименьшее? Почему?
Изотонический коэффициент 6,8% водного раствора соляной кислоты равен 1,66. Вычислите температуру замерзания этого раствора. КH2O= 1,86 ºС.
Раствор, содержащий 16,05 г Ba(NO3)2 в 500 г воды, кипит при 100,122 0С. Расчитайте изотонический коэффициент этого раствора. ЕH2O= 0,52 ºС.
Вычислите кажущуюся степень диссоциации хлорида магния в 0,5% водном растворе с плотностью 1 г/см3, если при 18 0С осмотическое давление этого раствора равно 3,2·105 Па.
Найдите относительное понижение давления водяного пара над раствором, содержащим 0,1 моль Na2SO4 в 900 г воды при 70 0С. Кажущаяся степень диссоциации в этом растворе равна 80%.
В 500 мл воды растворили 0,71 г Na2SO4. Найдите, при какой температуре начнет замерзать данный раствор. Степень диссоциации Na2SO4 принять равной 70%. КH2O= 1,86 ºС.
При растворении 0,1 моль некоторого вещества в 5 л воды температура кипения воды повышается на 0,016 0С. Покажите, чем является растворенное вещество: электролитом или неэлектролитом. КH2O= 1,86 ºС.
В 1 л раствора содержится 0,01 моль хлорида натрия. Осмотическое давление этого раствора при 0 0С равно 4,33·104 Па. Во сколько раз это давление больше, чем осмотическое давление в растворе сахара при той же молярной концентрации? Найдите кажущуюся степень диссоциации соли.
Осмотическое давление 0,04 М раствора электролита равно 2,15 атм. при 0 0С. Кажущаяся степень диссоциации электролита в растворе равна 70 %. На сколько ионов диссоциирует молекула электролита?
При растворении в 400 г воды 0,06 моля некоторого вещества температура замерзания раствора оказалась равной -0,36 0С. Является ли растворенное вещество электролитом? КH2O= 1,86 ºС.
Имеются 0,1 М растворы хлорида алюминия AlCl3 и хлорида кальция CaCl2. Степень электролитической диссоциации обеих солей в этих растворах одинакова. Какой раствор будет замерзать при более низкой температуре? Почему?
Температура замерзания раствора хлорида цинка, содержащего 0,85 г ZnCl2 в 125 г воды, равна -0,23 0С. Вычислите степень электролитической диссоциации хлорида цинка. КH2O= 1,86 ºС.
Осмотическое давление 0,05 н раствора HBr при 20 0С равно 2,27 атм. Вычислите степень электролитической диссоциации бромоводородной кислоты.
Вычислите температуру замерзания раствора хлорида кальция, если известно, что в 400 мл воды содержится 8 г CaCl2. Степень диссоциации хлорида кальция принять равной 70%.
На сколько ионов диссоциирует молекула электролита, если известно, что осмотическое давление 0,01 н раствора данного электролита при 0 0С равно 0,44 атм. Степень диссоциации равна 96%.
Вычислите температуру кипения раствора сульфата калия, содержащего 0,26 моль K2SO4 в 50 мл воды, если известно, что степень электролитической диссоциации раствора 53 %.
Степень электролитической диссоциации раствора, содержащего 0,05 г нитрата калия в 100 мл воды, равна 95 %. Чему равно осмотическое давление этого раствора при 0 0С?
Раствор, содержащий 1,06 г карбоната натрия в 400 г воды, кристаллизируется при -0,13 0С. Вычислите кажущуюся степень диссоциации соли. КH2O= 1,86 ºС.
В равных количествах воды растворено в одном случае 0,5 моля сахара, а в другом – 22,2 г хлорида кальция. Температуры замерзания обоих растворов одинаковы. Вычислите кажущуюся степень диссоциации хлорида кальция. КH2O= 1,86 ºС.
Степень диссоциации CaCl2 в растворе, содержащем 1,332 г CaCl2 в 250 г воды равна 75 %. Вычислите температуру замерзания раствора. КH2O= 1,86 ºС.
Раствор содержит 3,38 % нитрата кальция, кажущаяся степень диссоциации которого составляет 0,65. Вычислите осмотическое давление раствора при 0 0С, приняв плотность его равной 1,01 г/см3.
Определить степень диссоциации HCN в 1 н растворе, если константа диссоциации Кдисс=7,2·10-10. Вычислите концентрацию Н+, CN- и рН раствора.
Вычислите концентрацию ионов Н+, СН3СОО- и рН в 0,1 н растворе СН3СООН, если Кдисс=1,8·10-5. Чему равна степень диссоциации кислоты в этом растворе?
Вычислите концентрацию ионов ОН-, NH4+, pH, pOH в 0,8 М растворе NH4OH. Чему равна степень диссоциации NH4OH в этом растворе? Константа диссоциации Кдисс=1,8·10-5.
Вычислите степень диссоциации и концентрацию ионов Н+ в 1%-ном растворе уксусной кислоты СН3СООН (плотность 1 г/см3), если константа диссоциации К =1,85·10-5.
2 мл 96% серной кислоты плотностью 1,84 г/см3 разбавили до трех литров. Вычислить рН раствора при αкаж=1.
В 10 л раствора содержится 1 г NaOH. Вычислите рН и рОН этого раствора.
Что называется водородным и гидроксильным показателями? Вычислите рН и рОН 0,1 н раствора синильной кислоты. Кдисс= 7,2·10-10.
Произведение растворимости сульфата кальция равно 6,26·10-5. Образуется ли осадок, если смешать равные объемы 0,04 н раствора CaCl2 и Na2SO4?
Вычислите произведение растворимости карбоната стронция, если в 5 л насыщенного раствора содержится 0,05 г этой соли.
Произведение растворимости SrSO4 равно 3,6·10-7. Вычислите растворимость этой соли в молях на литр и в граммах на литр.
Вычислите ПРFe(OH)2, если в 100 мл его насыщенного раствора содержится 9,6·10-5 г этого гидроксида.
Сколько воды потребуется для растворения одного грамма ВаСО3, ПР которого равно 1,9·10-9?
В 100 мл насыщенного раствора PbI2 содержится 0,0268 г ионов свинца. Вычислите ПРPbI2.
Произведение растворимости MgF2 равно 7,0·10-9. Вычислите растворимость этой соли в моль/л и в г/л. Концентрация ионов Mg+2 в насыщенном растворе Mg(OH)2 составляет 2,6 · 10-3 г/л. Вычислите ПРMg(OH)2.
ПРAg2SO4 равно 7,0·10-5. Образуется ли осадок, если к 1 л 0,02 н раствора AgNO3 прибавить равный объем 1 н раствора H2SO4?
Сколько воды потребуется для растворения 1 г СаСО3? ПРCaCO3= 5·10-9 при 25 0С.
Чему равна масса Ag+ в 1 л насыщенного раствора AgCl? ПРAgCl= 1,8·10-10.
Во сколько раз уменьшится концентрация ионов серебра в насыщенном растворе AgCl, если прибавить NaCl столько, чтобы концентрация Cl- стала равной 0,01 моль/л? ПРAgCl= 1,8·10-10.
Почему Mg(OH)2 растворяется: а) в кислотах; б) в растворах аммонийных солей?
 ПРMg(OH)2=
2·10-11;
КдиссН2О
= 1,8 ·10-16;
КдиссNH4OH=1,8·10-5.
ПРMg(OH)2=
2·10-11;
КдиссН2О
= 1,8 ·10-16;
КдиссNH4OH=1,8·10-5.Почему при действии сероводородом на растворы солей Fe+2 осадок сульфида не выпадает, а при действии сульфидом аммония – выпадает. Ответ подтвердите расчетами. ПРFeS= 5·10-18; суммарная КдиссH2S= 6·10-8.
Пользуясь величинами произведений растворимости, объяснить, почему сульфид марганца растворяется в разбавленной серной кислоте, а сульфид меди (II) – нет. ПРMnS= 1,4·10-15; ПРCuS= 4·10-38; суммарная константа диссоциации KдиссH2S= К1К2 = 6·10-22.
Учитывая величины произведения растворимости малорастворимых солей, указать стрелками направление реакций:
|
а |
CaSO4 |
|
б)
BaCO3 |
BaSO4 |
|
в) 2Cr(OH)3 + 3 MgCl2 |
3Mg(OH)2 |
Если ПРCaCO3= 4,8 ·10-9; ПРCaSO4 = 6,1·10-5; ПРBaCO3= 7·10-9; ПРBaSO4= 1·10-10.
548. Чему равна масса Ag+ в 1 л насыщенного раствора AgCI? ПРAgCl= 1,8 . 10-10.
549. Выпадает ли осадок при сливании равных объемов следующих растворов:
|
Вариант |
Растворы, г-экв/л |
Осадок |
ПР | |
|
А |
CaCl2 0,02 |
Na2SO4 0,02 |
CaSO4 |
1,0 · 10-5 |
|
Б |
LaCl3 0,02 |
NaOH 0,03 |
La(OH)3 |
5 · 10-21 |
|
В |
Sr(NO3)2 0,002 |
K2SO4 0,002 |
SrSO4 |
3,6 · 10-7 |
|
Г |
CuSO4 0,01 |
(NH4)2S 0,02 |
CuS |
4 · 10-38 |
|
Д |
MnSO4 0,01 |
H2S
c
|
MnS |
1,4 · 10-15 |
Вычислить активную концентрацию ионов Fe+2, Ca+2, SO4-2 в растворе после травления металла, содержащем 0,05 моль/л FeSO4 и 0,01 моль/л CaSO4.

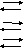 )
СаСО3
)
СаСО3