
- •ЗАНЯТТЯ № 1
- •р-Елементи
- •d-Елементи
- •ЗАНЯТТЯ № 5
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •ЗАНЯТТЯ № 6
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •ЗАНЯТТЯ № 7
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •ЗАНЯТТЯ № 8.
- •ЗАНЯТТЯ № 10.
- •Буферні розчини
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •ЗАНЯТТЯ № 12
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •Вказівки до навчальних дій
- •Вказівки до навчальних дій
- •Вказівки до навчальних дій
- •Вказівки до навчальних дій
- •Вказівки до навчальних дій
- •Вказівки до навчальних дій
- •Зміст і послідовність дій
- •8. ВКАЗІВКИ ДО РОБОТИ СТУДЕНТІВ НА ЗАНЯТТІ.
- •Перелік питань до підсумкового контролю модулю 1.
- •Хімічна термодинаміка
- •Енергія Гіббса
- •ЗАНЯТТЯ № 7
- •ЗАНЯТТЯ № 11
- •ЗАНЯТТЯ № 12
- •Підсумковий контроль засвоєння модулю 2
- •“Рівноваги в біологічних системах на межі поділу фаз”
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •ПРАВИЛЬНІ ВІДПОВІДІ
- •Заняття № 1. Вступ до практикуму. Техніка безпеки роботи в лабораторії.
- •Заняття № 5. Величини, що характеризують кількісний склад розчинів………………… 22
- •Заняття № 6. Приготування розчинів……………………………………………………….. 27
- •Заняття № 7. Основи титриметричного аналізу…………………………………………….. 31.
- •Заняття № 8. Основи титриметричного аналізу……………………………………………. 35
- •Заняття № 10. Буферні системи, класифікація та механізм дії..............................………... 43
- •Заняття № 11. Визначення буферної ємності. Роль буферів у біосистемах………………. 46.
- •Заняття № 12. Колігативні властивості розчинів…………………………………………… 50.
- •Перелік питань до підсумкового контролю модулю 1 ……………………………………. 55
- •Заняття № 7. Іонний обмін. Хроматографія………………………………………………... 87
- •Заняття № 11. Властивості розчинів біополімерів. Ізоелектрична точка білка…………. 104.
- •Заняття № 12. Підсумковий контроль засвоєння модулю 2
- •“Рівноваги в біологічних системах на межі поділу фаз”
- •1.3. Умови утворення та розчинення осадів.
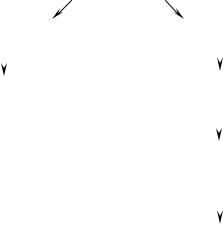
5.ГРАФ ЛОГІЧНОЇ СТРУКТУРИ
Ро з ч и н и
Класифікація |
Склад розчинів |
||
розчинів |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Розчини у |
Величини, що характеризують |
||
життєдіяльності |
кількісний склад розчинів |
||
організму |
|
|
|
|
|
||
|
|
Розрахунки по визначенню кількості |
|
|
|
розчиненої речовини для приготування |
|
|
|
розчинів певної концентрації |
|
|
|
|
|
|
|
Зважування наважки на терезах |
|
6. ОРІЄНТОВНА КАРТКА ДЛЯ САМОПІДГОТОВКИ ДО ЗАНЯТТЯ (самостійна позааудиторна робота студентів)
Зміст та послідовність дій |
Вказівки до навчальних дій |
1.Класифікація розчинів. |
1.1. Газоподібні, тверді та рідкі розчини. |
|
1.2. Насичені, ненасичені, пересичені |
|
розчини. |
2. Склад розчинів (розчинена |
|
речовина та розчинник). |
|
3. Величини, що характеризу- |
3.1. Масова, об’ємна та молярна частки (відсотки, |
ють кількісний склад розчинів. |
проміле). |
|
3.2. Позасистемні одиниці: мг-процентна та мкг- |
|
процентна концентрації. |
|
3.3. Молярна концентрація еквівалента (деци-, |
|
санти-, міліта мікромолі). |
|
3.4. Моляльна концентрація. |
|
3.5. Титр. |
ЗАДАЧІ ДЛЯ САМОСТІЙНОГО РОЗВ’ЯЗУВАННЯ (самостійна позааудиторна робота студентів)
Задача № 1.
Вміст катіонів натрію в плазмі крові складає 142 ммоль/л. Визначити титр плазми по катіону натрію.
Задача № 2.
Водний розчин, одержаний розчиненням 0,005 кг глюкози (Мr = 180) у 0,095 кг води, є ізотонічним по відношенню до плазми крові. Визначити масову та молярну частки глюкози в розчині.
Задача № 3.
Титр розчину хлориду кальцію (Мr = 111), що використовується в медичній практиці при алергічних, шкіряних та інших захворюваннях дорівнює 0,0999 г/мл. Розрахувати молярну концентрацію та молярну концентрацію еквівалента хлориду кальцію в розчині та співвідношення між ними.
Задача № 4.
23
Визначити моляльність фізіологічного розчину, масова частка хлориду натрію в якому дорівнює 0,85%.
Задача № 5.
У лабораторії є розчин з масовою часткою хлориду натрію 10% та 0,5%. Визначити масу кожного з розчинів, що необхідна для приготування 0,5 л фізіологічного розчину з масовою часткою 0,85% та густиною 1,003 кг/л.
ПРАВИЛЬНІ ВІДПОВІДІ
Задача № 1.
Титр (Т) означає масу розчиненої речовини, що міститься в 1 мл розчину. Масу частіше виражають у грамах (г).
Отже, маємо: |
|
|
||
T(Na+ ) = |
m(Na +) |
= n(Na+ )M(Na+ ) |
, де : |
|
V( розчину) |
||||
|
V( розчину) |
|
||
m(Na+) - маса катіонів натрію, г ; V (розчину) - об'єм розчину, мл;
n(Na+) - кількість речовини катіонів натрію, моль; М (Na+) - молярна маса катіону натрію, г/моль;
Т (Na+) = 0,142´ 23 = 3,266´10-3 г/мл
1000
Задача № 2.
Масова частка ( W ) - це відношення маси компоненту (розчиненої речовини) до загальної маси системи (розчину, суміші). Це безрозмірна величина, що виражається частками одиниці, відсотками (частки сотні), проміле (частки тисячі), млн-1 (частки мільйону).
W (глюкози) = m(глюкози) |
= |
0,005 |
= 0,05 = 5% = 50‰ = 5´104 млн-1 |
|
0,005 + 0,095 |
||||
т( розчину) |
|
|
Молярна частка ( χ ) - це відношення кількості речовини компонента (розчиненої речовини) до загальної кількості речовини системи (розчину, суміші). Вона має таку ж розмірність, як і масова частка.
c(глюкози) = |
n(глюкози) |
|
|
||||||
|
= |
|
|
|
|||||
n(глюкози) + n(H2O) |
|
|
|||||||
|
m(глюкози) ¸ М(глюкози) |
= |
|
||||||
m(глюкози) ¸ М(глюкози) + m(H2O) ¸ M (H2O) |
|
|
|||||||
= |
0,005 ¸180 |
= |
0,0000278 |
|
= |
0,0278 |
|||
0,005 ¸180 + 0,095 ¸18 |
0,0000278 + 0,00528 |
5,3056 |
|||||||
|
|
|
|||||||
= 0,00524 або 0,524%
Задача № 3.
Молярна концентрація речовини X, що позначається С(Х), - це відношення кількості речовини Х до об’єму розчину V. Молярна концентрація виражається в моль/м3, моль/л, або в їх похідних (ммоль/л).
c(CaCl2 ) = |
n(CaCL2 ) |
, |
де: |
|
V ( розчину) |
||||
n – кількість речовини СаСl2, моль; |
|
|
||
|
|
|
24

V(розчину) – об’єм розчину, л.
Якщо Т(СаСl2) = 0,0999 г/мл = 0,0999 кг/л, то в 1 л розчину маємо 0,0999 кг солі.
От ж е, V( розчину) =1 л, m(CaCl2 ) = 0,0999 кг. Тоді:
n |
= |
m(CaCl2 ) |
= |
0,0999 кг |
= 9´10-4 кмоль = 0,9 моль |
||
|
|
||||||
(CaCl2 ) |
|
M(CaCl2 ) |
111 кг/ кмоль |
||||
|
|
||||||
Тоді маємо: |
C |
(CaCl2 ) |
= 0,9 моль = 0,9 моль/ л |
||||
|
|
|
|
1 л |
|||
|
|
|
|
|
|
||
Молярна концентрація еквівалента речовини X, що позначається як С(fX), - це
відношення кількості речовини еквівалента n(fX) дo об’єму розчину.
Молярна концентрація еквівалента виражається в моль/м3, моль/л, або в їх похідних (ммоль/л)
C( fX ) = n(VfX ) , де: n( fX ) - кількість речовини еквівалента, моль;
f - фактореквівалентності; V - об'єм розчину в літрах.
Еквівалент - це така частина речовини Х (реальна або умовна), що в реакції еквівалентна (відовідає)одному моль атомів водню (Гідрогену), або одному моль катіонів водню (Гідрогену), або в окисно-відновних реакціях - одному електрону. Фактор еквівалентності f показує, яка частка моль речовини відповідає її еквіваленту. Отже, для речовини Х фактор еквівалентності f(X) показує співвідношення між молярною масою еквівалента M(fХ) та молярною масою М(Х) речовини:
|
|
|
|
|
|
f (X) = M( fX) |
|
|
||||||
|
|
|
|
|
|
|
M(X) |
|
|
|
||||
Наприклад для сірчаної кислоти Н2SO4: |
|
|||||||||||||
f (H |
2 |
SO ) = M(1/ 2 H2SO4 ) |
= 49 г/ моль = 1/ 2. |
|||||||||||
|
|
|
4 |
|
M(H2SO4 ) |
|
|
98 г/ моль |
|
|||||
|
|
|
|
|
|
|
|
|
||||||
Отже, для СaCl2: |
|
|
|
|
|
|
|
|||||||
С(1/ 2 CaCl2 ) = n(1/ 2 CaCl2 ) , |
де: n(1/ 2 CaCl2 ) = |
|||||||||||||
|
|
|
|
|
|
|
V |
|
|
|
|
|
||
= |
|
m(CaCl2 ) |
= |
m(CaCl2 ) |
|
|
= |
2m(CaCl2 ) |
= 2n(CaCl2 ) = |
|||||
M |
(1/ 2 CaCl2 ) |
1/ 2M(CaCl2 ) |
||||||||||||
|
|
|
M(CaCl2 ) |
|
||||||||||
= 2´ 0,9 моль =1,8 моль. |
|
|
|
|
|
|||||||||
Тоді: С(1/ 2 CaCl2 ) = 1,8 моль |
=1,8 моль/ л |
|
||||||||||||
|
|
|
|
|
|
|
1 л |
|
|
|
|
|
||
Таким чином: |
|
С(СaCl2 ) |
0,9 |
1 |
|
|||||||||
|
= |
1,8 |
= 2 , |
|
||||||||||
C(1/ 2 CaCl2 ) |
|
|||||||||||||
або в загальномувигляді: С(X) = f ´C( fX)
Задача № 4.
Моляльна концентрація речовини X, що позначається Сm(X) є відношенням кількості речовини Х до маси розчинника У.
Cm(X) = n(X) , де: n(Х) - кількість речовини X, моль; m(Y)
m(У) - маса розчинника, кг.
25
Якщо масова частка хлориду натрію в розчині дорівнює 0,85%, то це означає, що 0,85 г солі припадає на 99,15 г води. Отже,
n(NaCl) = m(NaCl) = 0,85 = 0,0145 (моль), M (NaCl) 58,5
m(H2O) = 99,15 г = 0,09915 кг,
Cm(NaCl) = 0,0145 моль = 0,146 моль/ кг. 0,09915 кг
Задача № 5.
По-перше, зробимо необхідні позначення: W1(NaCl) = 10% W2(NaCl) = 0,5% Wx(NaCl) = 0,85% Vx(розчину) = 0,5л ρx(розчину) = 1,003 кг/л
Знайдемо масу розчину, який треба приготувати:
mx(розчину) = Vx(розчину) ×ρx(розчину) = 0,5×1,003 = 0,5015 кг
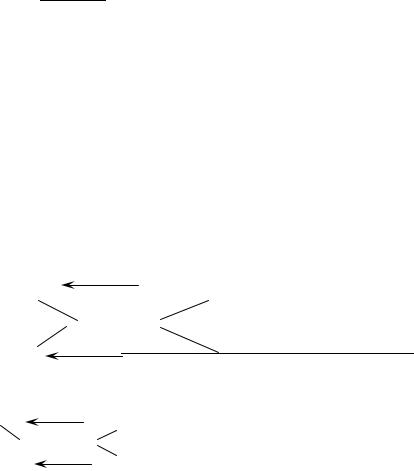
2) Проведемо розрахунки за правилом змішування ("хреста"). У загальному вигляді:
W1(NaCl)
W2(NaCl)
Або: 10%
0,5%
m1' ( розчину) = Wx -W2
Wx(NaCl)
m2' ( розчину) = W1 -Wx
mх' ( розчину) = m1' ( розчину) + m2' ( розчину)
0,35 кг
0,85%
9,15 кг
m' |
(розчину) = 9,5 кг |
|
|
|
|
||
x |
|
|
|
|
|
|
|
Знаходимо необхідні маси розчинів: |
|
|
|
||||
m |
( розчину) = |
mx ( розчину) |
|
´ m' ( розчину) = 0,5015 ´ 0,35 |
= 0,0185 кг = 18,5 г |
||
|
|||||||
1 |
|
mx' ( розчину) |
1 |
9,5 |
|
|
|
|
|
|
|
|
|||
т2 |
( розчину) = |
тх ( розчину) |
' |
0,5015 |
´ 9,15 |
= 0,483 кг = 483 г |
|
тх' ( розчину) |
´ т2 ( розчину) = |
9,5 |
|||||
Висновок: треба змішати 18,5 г розчину з W1=10% та 483 г розчину з W2= 0,5%.
8.ВКАЗІВКИ ДО РОБОТИ СТУДЕНТІВ НА ЗАНЯТТІ.
8.1.Розв'язування задач на концентрацію розчинів.
Задача № 1.
У воді об’ємом 0,200 л розчинили сіль масою 0,040 кг. Визначити масову частку солі в розчині, якщо густина води дорівнює 1 кг/л.
Задача № 2.
Визначити масу розчину з масовою часткою СuSО4 10% і масу води, що необхідні для приготування розчину масою 0,5 кг з масовою часткою СuSО4 2%.
Задача № 3.
Визначити молярну концентрацію розчину з масовою часткою гідроксиду Натрію 0,2. Густина розчину - 1,29 кг/л.
26
