
- •Міністерство освіти і науки україни національний університет харчових технологій
- •Методи контролю біотехнологічних, фармацевтичних і харчових виробництв лабораторний практикум
- •Київ нухт 2014
- •Інструкція з охорони праці при проведенні робіт у навчальних лабораторіях кафедри
- •1. Загальні вимоги до техніки безпеки
- •2. Правила техніки безпеки
- •3. Вимоги безпеки у аварійних ситуаціях
- •4. Надання першої допомоги
- •5. Вимоги до оформлення лабораторних робіт
- •Лабораторна робота 1 розділення амінокислот методом тшх на силуфолових пластинках
- •Реактиви
- •Матеріали та обладнання
- •Загальні відомості
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •Матеріали та обладнання
- •Загальні відомості
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •Розчинність речовин у воді при різних температурах (г/100 г h2o)
- •Залежність густини і концентрації розчинів NaCl від температури
- •Густина речовин
- •Залежність густини розчинів h2so4 від її масової долі у водному розчині при 25 °c
- •Хід роботи
- •Густина розчинів NaCl та kCl в г/см3, що відповідає різним концентраціям у %
- •Завдання на виконання
- •Контрольні запитання
- •Рекомендована література
- •Хід роботи
- •Завдання на виконання:
- •Контрольні запитання
- •Матеріали та обладнання
- •Загальні відомості
- •Закон Бугера – Ламберта – Бера. При прохожденні випромінення через розчин світлопоглинаючої речовини світловий потік слабшає.
- •Фотометричні методи аналізу
- •Залежність кольору речовини від довжини хвилі поглинутого світла
- •Приготування робочих розчинів для побудови калібрувальної кривої
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •Рекомендована література
- •Матеріали та обладнання
- •Загальні відомості
- •Методом Лоурі
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •Рекомендована література
- •Лабораторна робота 8
- •Коефіцієнт молярної екстинкції деяких цитохромів
- •Хід роботи
- •Завдання для виконання
- •Контрольні запитання
- •3. Методи генної інженерії.
- •Рекомендована література
Залежність кольору речовини від довжини хвилі поглинутого світла
-
Колір розчину
Довжина хвилі
частини спектра, нм
жовто-зелений
400-450
жовтий
450-480
оранжевий
480-490
красний
490-500
пурпурний
500-560
фіолетовий
560-575
синій
575-590
синьо-зелений
590-625
зелений
625-750
Сучасні прилади дозволяють проводити виміри у видимій області спектра (400-760 нм) і в тих, що примикають до неї: ультрафіолетовій (300-400 нм) та інфрачервоній (760-1000 нм) областях.
У видимій області колір розчину обумовлений довжиною хвилі випромінювання, не поглиненого цим розчином, і є додатковим до кольору поглиненої частини світла. Якщо речовина не забарвлена, то проводять реакцію, в результаті якої утворюються забарвлені розчинні сполуки.
Принцип роботи ФЕК. Фотоелектроколориметр застосовується для визначення концентрації забарвлених розчинів за їх здатностю до світлопропускання (оптична густина).
Прилад працює від мережі змінного струму. В якості джерела світла в приладі використовують лампу “Л” розжарювання (для роботи у видимій частині спектру) та ртутно-кварцеву лампу високого тиску (для вимірювання в ультрафіолетовій частині спектру). Величину світлового потоку виражають в одиницях оптичної густини (екстинкція). Схема однопроменевого фотоелектроколориметра представлена на рис.6.5.
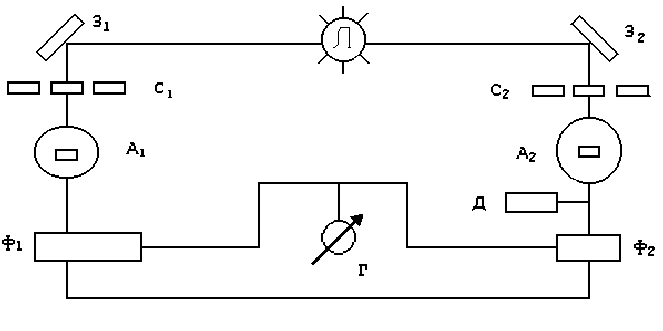
Рис.6.5. Принципова схема будови фотоелектроколориметра
Принцип роботи фотоелектроколориметра полягає в порівнянні інтенсивності потоків світла, що пройшло через розчин порівняння і через досліджуваний розчин (Рис. 3.2.).
Світлові пучки від лампи "Л" відбиваються від дзеркала "З1" і "З2", проходять через світлофільтри "С1" та "С2" (пропускає випромінювання лише певної довжини хвилі). Монохроматичне випромінювання спочатку проходить через кювету з чистим розчинником, потрапляє на фотоелемент і за допомогою поглинаючого оптичного клину показання вимірювального приладу встановлюють точно на 100 відсотків пропускання. Потім замість кювети з розчинником на шляху променя вміщують кювету з досліджуваним розчином - вимірювальний прилад відразу показує його коефіцієнт пропускання і оптичну щільність, за якими можна визначити концентрацію поглинаючої речовини в розчині.
Джерела випромінювання, що використовуються фотометрії це випромінювачі безперервного спектру. Це вольфрамові лампи розжарювання, газонаповнені лампи (воднева, ртутна).
У лампі розжарювання вольфрамова спіраль дає світло в широкому спектральному інтервалі, проте, скло пропускає світло з довжинами хвиль 350-1000 нм, тобто ближній ультрафіолет, видиме світло і випромінювання ближній ІЧ- області. У водневій (дейтерієвій, ксеноновій) лампах відбувається світіння газу при розряді - виникає суцільне випромінювання в області 200-350 нм.
Світлофільтри. Для того, щоб з усієї видимої області спектру виділити промені певних довжин хвиль у фотоколориметрах на шляху світлових потоків перед поглинаючими розчинами встановлюють вибіркові поглиначі світла - світлофільтри. Світлофільтри - це забарвлені стекла, що пропускають полоску світла 20 - 50 нм. Світлофільтри пропускають промені лише в певному інтервалі довжин хвиль і практично повністю поглинають промені інших довжин хвиль. Чим вужча область максимального пропускання променів світлофільтру, тим вище його вибірковість до променів цього інтервалу довжин хвиль.
Світлофільтри застосовують в колориметрах для виділення спектральної ділянки, в якій аналізований розчин має найбільшу величину абсорбції(поглинання). Колориметри мають набір світлофільтрів, що безперервно перекривають усю видиму ділянку спектру.
Вибір світлофільтрa. В фотоелектроколориметрах спектральні діапазони виділені за допомогою світлофільтрів, тому число ділянок спектра з певною довжиною хвилі, в якому може проводитися вимірювання на даному приладі, дорівнює числу світлофільтрів і вказане на панелі приладу.
Вибраний світлофільтр повинен мати мінімальне поглинання свідлофільтра, що співпадає з максимальним поглинанням досліджуваного розчину (рис.6.6).

довжина хвилі, нм
Рис. 6.6. Поглинання світлового потоку: 1- досліджуваний розчин;
2 - світлофільтр
Для вибору світлофільтра, який найбільш підходить для проведення фотометричних вимірювань, досліджуваний забарвлений розчин наливають у кювету та вимірюють його абсорбцію за допомогою усіх наявних у приладі світлофільтрів, будують криву, відкладаючи на горизонтальній осі довжину хвиль (у нм), а на вертикальній – значення оптичної щільності. Визначають світлофільтри, що відображають найбільшу величину абсорбції. Із двох близьких за областями пропускання світлофільтрів обирають той, при роботі з яким чутливість приладу, що оцінюється за максимальним значенням абсорбції, є найвищою.
Спектрофотометри – це прилади більш високого класу, ніж фотоелектроколориметри.
Принцип роботи спектрофотометра (рис.6.7.). Від джерела випромінювання 1 світловий потік за допомогою системи дзеркал розділяється на два рівноцінні потоки (промені). Один промінь проходить через кювету 11, в якій знаходиться розчинена речовина, а інший через кювету порівняння 2, в якій знаходиться розчинник. Обидва світлові потоки проходять модулятор 4 - дзеркальну пластину, що швидко обертається, влаштовану так, що, обертаючись, вона по черзі перекриває один з променів і пропускає інший.

Рис.6.7. Принципова блок-схема двопроменевого спектрофотометра
Промені, пройшовши модулятор 4, потрапляють по черзі у вхідну щілину монохроматора 5, який складається з вхідної спектральної щілини, призми або дифракційної решітки де промені розкладаються, фокусуючого об'єктива і вихідної спектральної щілини, яка виділяє випромінювання вузького інтервалу довжини хвилі. Можливість вибору потрібного спектрального діапазону забезпечується шляхом повороту спеціального механізму в різних моделях може здійснюватися вручну (послідовно перебираючи необхідні довжини хвиль) або автоматично (за допомогою програмного забезпечення).
Вузька ділянка спектру променів подається на фоточутливий пристрій 6, в якому світловий потік перетвориться в електричний сигнал, що відповідає йому. Електричні сигнали поступають на обладнання порівняння 7, яке віднімає один сигнал з іншого. Різниця двох сигналів подається на підсилювач 8 і самописець 10, система управління яким відградуйована у відсотках оптичної щільності.
Самописець 10 реєструє спектральну криву поглинання, що складається з набору піків різної висоти і ширини, частот, що знаходяться в досліджуваному діапазоні УФ, видимої або ІЧ області спектра.
Джерелом випромінювання у видимій і ближній ІЧ області спектра є розжарена вольфрамова нитка лампи розжарювання (350-1000 нм).
Для отримання випромінювання УФ діапазону використовують водневі або криптонові лампи, для отримання потужних світлових пучків - ртутні лампи високого тиску. ІЧ випромінювання отримують за допомогою спеціальних джерел, виконаних з платини.
Спектрофотометри дають можливість записати спектр поглинання речовини (рис.6.8).

Рис. 6.8. Спектр поглинання вітаміну А (суцільна лінія) і продигіозину (пунктир) в УФ і видимому світлі
Усі елементи оптичної системи приладу, у тому числі і робочі кювети, мають бути максимально прозорі. Найбільш широко поширеним матеріалом для виготовлення кювет є кварц.
Розчин порівняння. Вимірювання оптичної щільності стандартного і досліджуваного розчинів завжди проводиться по відношенню до розчину порівняння. В якості розчину порівняння можна використати усі компоненти розчину, окрім реагенту, що утворює забарвлене з'єднання.
У тому випадку, коли сам реагент має забарвлення, розчин порівняння готують таким чином: до невеликої кількості дистильованої води додають реагент і усі компоненти (окрім визначуваного) в тих же кількостях, що і при приготуванні забарвлених розчинів.
Кювети. Досліджувану речовину розчиняють у відповідному розчині і вміщують в оптично прозору посудину для вимірів - кювету. Оскільки скло поглинає ультрафіолетове світло, для проведення вимірювання в ультрафіолетовій області спектра використовують кварцеві кювети. Для вимірювання у видимій області можна використати пластикові або скляні кювети. При роботі з леткими або хімічно активними речовинами кювети закривають кришками.
Оскільки кювета, вміщена в спектрофотометр, стає складовою частиною його оптичної системи, з нею треба поводитися дуже акуратно. Подряпини і бруд на стінках кювети розсіюють і поглинають світло, спотворюючи результати вимірювання. Про це особливо потрібно пам'ятати при роботі в ультрафіолетовій області. Кювети можна протирати м'якими тканинами, наприклад, з бавовни. Не рекомендується використати для цих цілей фільтрувальний папір. Оскільки органічні молекули поглинають в ультрафіолетовій області, ні в якому разі не можна торкатися пальцями оптичних (прозорих) стінок кювети. Кювети досить крихкі, особливо кварцеві, тому працювати з ними потрібно обережно, не допускаючи механічних ушкоджень.
Вміст кювети має бути гомогенним - це необхідна умова отримання відтворюваних даних. Треба стежити за тим, щоб розчин не був мутним. Особливо заважають вимірам бульбашки повітря, що дуже збільшують розсіяння світлового потоку. Не можна наливати в кювету дуже холодний розчин, оскільки при цьому на зовнішніх стінках кювети конденсується пар і її стінки стають непрозорими.
Якщо кювети забруднені сторонніми домішками, їх слід промити дистильованою водою або розчинником, в якому розчинена досліджувана речовина. Кювети можна мити м'якими детергентами. Не рекомендується мити кювети концентрованими кислотами або лугами.
Кювети треба заповнювати до такого рівня, щоб потік світлового випромінювання проходив цілком через шар розчину. Найчастіше використовуються кювети з оптичним шляхом 1 см, в які зазвичай заливають 2,5-3 мл розчину. У такі кювети входить 4-5 мл, але заповнюють їх не повністю. Є кювети з оптичним шляхом 50, 20, 5, 2 і 1 мм.
Побудова калібрувальної кривої. Концентрація білку в досліджуваному розчині визначається за калібрувальною кривою. Калібрувальна крива відображає залежність між абсорбцією (А), що називається також оптичною щільністю (D) або екстинкцією (Е) та концентрацією (С) речовини в серії стандартних розчинів.
Для побудови калібрувального графіка готують серію стандартних розчинів з відомою концентрацією речовини. В якості стандарту можна використати альбумін сироватки крові бика або яєчний альбумін. Перед приготуванням стандартного розчину альбумін висушують в вакуумі при 600С до постійної маси. Стандартні розчини повинні готуватися особливо ретельно з наважки, отриманої на терезах дуже точного зважування (наприклад, аналітичних). Стандартні речовини для приготування таких розчинів повинні мати високий ступінь чистоти та достатню стабільність, не були гігроскопічними і не взаємодіяли із газами повітря.
Наважка повинна бути достатньо великою, що дозволяє зменшити технічну помилку під час зважування. Цьому сприяє зважування стандартної речовини не у звичайному бюксі, а на поліетиленовій плівці із подальшим кількісним повним перенесенням речовини у скляний мірний посуд. Речовина перед зважуванням має бути висушена до постійної маси у сушильній шафі при температурі 110 °С.
Мірний посуд, що використовується для отримання стандартних розчинів, необхідно попередньо ретельно знежирити та вимити. Не рекомендується сушити мірний посуд у сушильний шафі, оскільки за високої температури змінюється його об’єм та порушується градуювання.
Розведення стандартної речовини повинні не тільки охоплювати діапазон фізіологічних концентрацій, але й виходити за межі їх мінімальних та максимальних величин. У більшості випадків ряд калібрувальних розчинів отримують шляхом розбавлення основного (маточного) розчину. Відомо, що чим концентрованішим є розчин стандартної речовини, тим довше вона зберігається у ньому.
Щоб приготувати маточний розчин на аналітичних вагах робимо наважку 0,5 г ліофілізованого альбуміну, обережно переносими його в колбу і додаєм 4,5 мл фізіологічного розчину. Легкими обертальними рухами перемішуємо вміст колби до повного розчинення. Зберігати такий розчин можна при температурі від +2 до +40С.
Для побудови калібрувального графіка з основного стандартного розчину білка (1 мл основного стандартного розчину містить 0,1 г білку) готують робочі стандартні розчини, як зазначено в таблиці 6.3.
Для кожної точки роблять не менше 3 визначень (готують 3 розчини однакової концентрації).
Вимірюють оптичну щільність розчинів проти розчину порівняння, поглинання якого приймають рівним нулю. Вимірювання починають з розчину меншої концентрації.
Таблиця 6.3.
