
- •Київ кнуБіА пробірочний практикум
- •Якісний аналіз органічних речовин
- •Лабораторна робота № 1 якісні реакції органічних речовин
- •Дослід і. Виявлення карбону й гідрогену
- •Дослід 2. Виявлення нітрогену за реакцією лассеня
- •Дослід 3. Виявлення сульфуру
- •Дослід 4. Виявлення галогенів
- •Вуглеводні
- •Насичені вуглеводні
- •Лабораторна робота № 2
- •Дослід 2. Взаємодія алканів із бромною водою і розчином калій перманганату
- •Дослід 3. Добування етилену і вивчення його властивостей
- •Дослід 7. Добування ацетилену з карбіду кальцію та вивчення його властивостей
- •Дослід 11. Добування ацетиленіду аргентуму та ацетиленіду купруму
- •Ароматичні вуглеводні ( арени )
- •Лабораторна робота № 3 добування й властивості ароматичних вуглеводнів
- •Дослід 1. Добування бензену з бензоату натрію
- •Дослід 2. Взаємодія бензену із бромом
- •Дослід 3. Взаємодія гомологів бензену із бромом
- •З розчином калій перманганату
- •Дослід 6. Окислення гомологів бензену
- •Дослід 7. Нітрування бензену
- •Дослід 9. Сульфування фенолу
- •Дослід11. Окислення фенолу
- •Дослід12. Сублімація нафталену
- •Дослід 13. Нітрування нафталену
- •Дослід 14. Бромування нафталену
- •Галогенопохідні вуглеводнів
- •Лабораторна робота № 4 добування й властивості галогенопохідних
- •Дослід 1. Добування хлористого етилу
- •Дослід 2. Синтез брометану
- •Дослід 3. Добування йодоформу зi спирту
- •Дослід 6. Порівняння рухливості атомів галогену у бензеновому кільці та у боковому ланцюзі
- •Оксигенвмісні сполуки та їх похідні.
- •Одноатомні спирти
- •Лабораторна робота № 5 хімічні властивості одноатомних спиртів
- •Дослід 2. Виділення тепла під час розчинення етилового спирту у воді
- •Дослід 3. Горючість спиртів
- •Дослід 4. Виявлення води в спирті
- •Дослід 5. Висолювання етилового спирту
- •Дослід 6. Утворення алкоголятів натрію та їх гідроліз
- •Дослід 7. Окислення етилового спирту калій перманганатом
- •Дослід 8. Окислення спиртів оксидом купруму (II)
- •Дослід 9. Добування ectepib
- •Дослід 10. Виявлення сивушного масла у спирті
- •Дослід 11. Реакція на ненасичені одноатомні спирти
- •Дослід 12. Взаємодія етиленгліколю з натрієм
- •Дослід 13. Утворення гліколяту і гліцерату купруму
- •Дослід 14. Дегідратація гліцерину
- •Дослід 15. Розчинність фенолу у воді та його кислотні властивості
- •Дослід 16. Добування феноляту натрію
- •А л ь д e гіди та k e t o н и
- •Лабораторна робота № 6
- •Дослід 4. Реакція срібного дзеркала
- •Дослід 5. Реакція відновлення альдегідами гідроксиду купруму (II)
- •Дослід 6. Реакція відновлення альдегідами реактиву фелінга
- •Дослід 8. Взаємодія альдегідів із лугом
- •Дослід 13. Реакція канніццаро
- •Дослід 14. Окислювальні властивості хінону
- •Карбонові кислоти та їх похідні одноосновні карбонові кислоти. Жири
- •Лабораторна робота № 7
- •Карбонових кислот і жирів
- •Дослід 1. Розчинність карбонових кислот
- •Дослід 2. Виявлення карбонових кислот за допомогою індикаторів
- •Дослід 3. Утворення солей карбонових кислот
- •Дослід 4. Гідроліз солей карбонових кислот
- •Дослід 7. Відновлення амоніачного
- •Дослід 13. Взаємодія олеїнової кислоти із бромом
- •Дослід 15. Акролеїнова проба на жири
- •Дослід 16 визначення ненасиченост1 жиру
- •Дослід 18. Розчинність жирів
- •Дослід 20. Декарбоксилування малонової кислоти
- •Дослід 21. Гідроліз аспірину
- •Нітрогенobmichi органічні сполуки hitpo- і аміносполуки жирного ряду
- •Лабораторна робота № 8. Хімічні властивості hitpo- та аміносполук жирного та ароматичного ряду
- •Дослід 1. Кислотні властивості нітрометану
- •Дослід 7. Взаємодія амінів із солями феруму й купруму
- •Дослід 8. Реакція первинних аміносполук з нітритною кислотою
- •Дослід 9. Взаємодія аніліну з мінеральними кислотами
- •Дослід 12. Реакція аніліну із хлорним вапном
- •Дослід 16. Реакція діазотування
- •Амінокислоти і білкові речовини
- •Лабораторна робота №9 хімічні властивості амінокислот і білків
- •Дослід 2. Утворення комплексної солі купруму амінооцтової кислоти
- •Дослід 6. Висолювання білків
- •Дослід 7. Кольорові реакції на білки
- •Вуглеводи моносахариди (монози)
- •Полісахариди (поліози, несахароподібні вуглеводи)
- •Лабораторна робота № 10 хімічні властивості моносахаридів, дисахаридів та полісахаридів
- •Дослід 1. Якісна реакція на вуглеводи 3 α-нафтолом (реакція Моліша)
- •Дослід 2. Окислення моноз оксидом аргентуму (реакція срібного дзеркала)
- •Дослід 3. Окислення глюкози реактивом фелінга
- •Дослід 5. Реакція селіванова на кетогексози
- •Дослід 6. Реакція на наявність гідроксильних груп у дисахаридах
- •Дослід 7. Відношення дисахаридів до фелінгової рідини
- •Дослід 8. Відношення дисахаридів до амоніачного розчину оксиду аргентуму
- •Дослід 9. Гідроліз (інверсія) сахарози
- •Дослід 10. Якісна реакція на сахарозу
- •Дослід 12. Виявлення крохмалю в картоплі та зерні
- •Дослід 13. Розчинення клітковини у купрум-амоніачному розчині (реактив Швейцера)
- •Дослід 14. Розчинення клітковини в сульфатній кислоті
- •Полімери. Високомолекулярні сполуки
- •Лабораторна робота № 11
- •Дослід 1. Добування полібутилметакрилату
- •Лабораторна робота № 12
Лабораторна робота № 4 добування й властивості галогенопохідних
Реактиви й матеріали: етиловий спирт; хлороформ; йодоформ; бромоформ; резорцин; хлорид натрію; бромід калію; сульфатна кислота; гідроксид натрію; нітрит аргентуму; оксид кальцію; мідна спіраль; лакмус; фільтрувальний папір.
Дослід 1. Добування хлористого етилу
У пробірку приливають 2–3 мл заздалегідь приготовленого розчину етилового спирту з концентрованою сульфатною кислотою. Добавляють 1–2 г хлориду натрію. Пробірку закривають пробкою з невеликою газовідвідною трубкою, закріплюють на штативі та обережно нагрівають над полум'ям пальника. Якщо піднести через деякий час до отвору газовідвідної трубки запалений сірник чи скалку, хлористий етил, утворюваний під час реакції, горітиме із характерним зеленим кільцем по краях газовідвідної трубки. Реакція утворення хлористого етилу проходить за такою схемою:
C
 H3-CH2OH
+ HOSO2OH
CH3-CH2OSO2OH
+ H2O;
H3-CH2OH
+ HOSO2OH
CH3-CH2OSO2OH
+ H2O;
2
 NaCl+
H2SO4
2HCl +
Na2SO4;
NaCl+
H2SO4
2HCl +
Na2SO4;
C
 H3-CH2OSO2OH
+
HCl
CH3-CH2Cl
+
H2SO4.
H3-CH2OSO2OH
+
HCl
CH3-CH2Cl
+
H2SO4.
Після проведення досліду прилад слід охолодити у витяжній шафі, а потім промити пробірку і пробку водою. Пам'ятайте, що в пробірці була концентрована сульфатна кислота.
Дослід 2. Синтез брометану
Реактиви : етанол 96% - 10 мл, бромід калію – 15 г, сульфатна кислота (густина 1,84 г/см3 , вода – 9 мл, хлорид кальцію( безводний) – 20 г.
У колбу В’юрка ( 250 мл) обережно наливають 10 мл етилового спирту, додають 9 мл води і охолоджують під холодною водою з крану. Не припиняючи охолодження, обережно, невеликими порціями додають 16 мл концентрованої сульфатної кислоти. До охолодженої суміші добавляють 15 г розтертого в фарфоровій ступці порошок броміду калію. Колбу закріплюють на штативі і закривають пробкою з термометром, поміщають у пісочну баню та з'єднують з холодильником Лібіха. Кінець його занурюють у конічну колбу, заповнену холодною водою із льодом. Реакційну суміш обережно нагрівають до слабкого кипіння. Бромистий етил, утворюваний під час реакції, збирається на дні приймача у вигляді важкої олієподібної рідини. Як тільки перестануть відганятися краплі бромистого етилу, нагрівання припиняють і виймають алонж із приймача. Реакція утворення бромистого етилу аналогічна схемі утворення хлористого етилу.
По закінченні реакції продукт переливають у ділильну воронку, відокремлюють бром етан від води, висушують безводним хлоридом кальцію, зважують на терезах та розраховують вихід продукту. Розрахунок провести по броміду калію.
З отриманим препаратом слід зробити пробу Бейльштейна. Для цього на кінець окисленої мідної спіралі треба нанести кілька крапель добутого бромистого етилу і внести у полум'я пальника. Полум'я забарвлюється в характерний зелений колір, що свідчить про наявність галогену.
Дослід 3. Добування йодоформу зi спирту
У пробірку наливають 1 мл води, 0,5 мл етилового спирту і 3–4 мл розчину йоду в йодиді калію. В цю суміш по краплях додають 10 %-ний розчин гідроксиду натрію до зникнення бурого забарвлення. Через деякий час спостерігається поява жовтого осаду йодоформу, що легко розпізнається за характерним запахом. Реакція проходить за схемою:
взаємодія йоду з лугом: J2 + NaOH → Н20 + NaJ + NaOJ;
окислення спирту в альдегід:
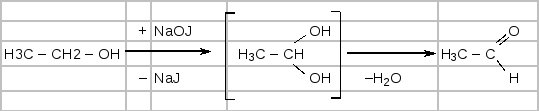 заміна
атомів Гідрогену в залишку оцтового
альдегіду на галоген:
заміна
атомів Гідрогену в залишку оцтового
альдегіду на галоген:
СH3-CHO + 3 J2 + NaOH → CJ3-CHO + 3NaJ + 3H2O;
розщеплення трийодоцтового альдегіду: CJ3-CHO + NaOH→CHJ3 +H-COONa.
Сумарне рівняння :CH3-CH2OH + 4J2 + 6NaOH → CHJ3 + H-COONa + 5NaJ + 5Н2О.
Дослід 4. ЗАМІЩЕННЯ ГАЛОГЕНУ НА ГІДРОКСИЛ ПІД ДІЄЮ ЛУГУ У пробірку до 0,5 мл хлороформу приливають 2–3 мл 10 %-ного розчину гідроксиду натрію й обережно при збовтуванні нагрівають суміш до кипіння. Потім охолоджують, відстоюють і зливають частину водно-лужного шару. До цієї частини обережно добавляють нітратну кислоту до кислого середовища (проба на лакмус) і кілька крапель 1 % -ного розчину нітрату аргентуму.
Утворюється білий осад хлориду аргентуму, не розчинний у нітратній кислоті:
![]()

 H–COOH;
H–COOH;
H-COOH + NaOH → H-COONa + H2O;
NaCl + AgNO3 → AgCl + NaNO3.
За однакової будови галогенопохідних легкість заміни галогену понижується в ряду J>Br>Cl>F.
Дослід 5. РЕЗОРЦИНОВА ПРОБА НА ХЛОРОФОРМ
Характерною якісною реакцією на хлороформ, бромоформ і йодоформ є, так звана, резорцинова проба.
У пробірку наливають 1–2 мл свіжо приготовленого 10 % -ного розчину резорцину, кілька крапель 10 %-ного розчину гідроксиду натрію і кілька крапель хлороформу або кристаликів йодоформу. Суміш нагрівають. З'являється забарвлення.
