
- •Работа № 1 Качественное определение ионов токсичных металлов в воде
- •Бесцветные ионы Цинк
- •Опыт 1. Определение цинка
- •Опыт 2. Определение кадмия
- •Опыт 3. Определение свинца
- •Опыт 4. Определение ртути иодидом калия
- •Опыт 5. Определение висмута (III) тиомочевиной
- •Окрашенные ионы Железо
- •Опыт 6. Определение железа (III)
- •Опыт 7. Определение хрома
- •Опыт 8. Определение меди
- •Опыт 9. Анализ воды на содержание ионов тяжелых металлов (контрольная задача)
- •Определение ионов тяжелых металлов
- •Работа № 2 Качественное определение ионов токсичных неметаллов в воде
- •Опыт 1. Определение сульфид-иона
- •Опыт 2. Обнаружение иона аммония
- •Опыт 3. Определение нитрит-иона no2‾
- •Опыт 4. Обнаружение нитрат-иона no3‾
- •Опыт 5. Определение аниона фтора
- •Опыт 6. Определение фосфора
- •Опыт 7. Определение мышьяка
- •Опыт 8. Анализ воды на содержание анионов неметаллов (контрольная задача)
- •Определение ионов неметаллов
- •Работа № 3 Жесткость воды
- •А. Определение карбонатной жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором hCl
- •Б. Определение общей жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором эдта
- •Работа № 4 Определение окисляемости воды методом перманганатометрии
- •Оборудование и реактивы
- •А. Определение окисляемости воды обратным титрованием
- •Б. Определение окисляемости воды прямым титрованием
- •Работа № 5 Фотометрическое определение примесей тяжелых металлов в пресной воде
- •А. Определение железа в виде роданидного комплекса
- •Результаты фотометрирования растворов
- •Оборудование и реактивы
- •Описание определения
- •Б. Определение меди в виде аммиачного комплекса а) Метод калибровочного графика Оборудование и реактивы
- •Описание определения
- •Б) Метод стандартных добавок
- •Описание определения
- •В. Определение висмута в виде тиокарбамидного комплекса
- •Оборудование и реактивы
- •Описание определения
- •Г. Определение титана и ванадия при их совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 6 Спектрофотометрическое определение примесей нефти и нефтепродуктов в природной воде
- •Внешний вид пленки нефти на поверхности воды в зависимости от ее толщины и количества нефти
- •Оборудование и реактивы
- •Описание определения
- •Электрохимические методы анализа объектов окружающей среды
- •Работа № 7 Определение рН воды и почвы
- •Оборудование и реактивы
- •А. Определение рН воды с применением индикаторов
- •Изменение окраски индикаторов
- •Б. Определение рН воды на иономере методом прямой потенциометрии
- •Описание определения
- •В. Определение рН почвы
- •Нормы внесения молотого известняка (кг/10 м2) при различных значениях pH почвы
- •Оборудование и реактивы
- •Работа № 8 Ионоселективное определение примесей различных ионов в природной и питьевой воде а. Определение хлорид-ионов
- •Основные характеристики ионоселективных электродов
- •Оборудование и реактивы
- •Описание определения
- •Результаты ионометрического определения ионов в воде
- •Б. Определение фторид-ионов
- •Оборудование и реактивы
- •Описание определения
- •В. Определение примесей железа
- •Оборудование и реактивы
- •Описание определения
- •Результаты титрования
- •Г. Определение нитрат-ионов
- •Оборудование и реактивы
- •Описание определения
- •Работа № 9 Определение содержания токсичных ионов тяжелых металлов в питьевой воде методом инверсионной вольтамперометрии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 10 Определение меди и цинка при их совместном присутствии на катионите ку-2
- •Раздельное вымывание примесей с катионита ку-2
- •Оборудование и реактивы
- •Описание определения
- •Работа № 11 Определение кадмия в растворах методом хроматографии на бумаге
- •Оборудование и реактивы
- •Описание определения
- •Результаты хроматографического определения ионов кадмия Работа № 12 Определение уровня радиационного загрязнения окружающей среды
- •Оборудование
- •Описание определения
- •Литература
- •Содержание
Работа № 7 Определение рН воды и почвы
При определении рН по методу нейтрализации наиболее применимы индикаторы: метиловый оранжевый, метиловый красный, лакмус и фенолфталеин. Поведение их упрощенно объясняет ионная теория индикаторов.
Согласно этой теории, индикаторы - слабые органические кислоты (или слабые основания), у которых недиссоциированные молекулы и образуемые ими ионы имеют различную окраску. Поэтому они носят общее название кислотно-основных индикаторов.
Если обозначить молекулы фенолфталеина через HInd, а его анионы - через Ind–, то уравнение диссоциации имеет вид:
HInd H+ + Ind ‾.
бесцветный малиновый
Если к этому раствору прибавить какую-нибудь сильную кислоту (или внести фенолфталеин в раствор кислоты), равновесие диссоциации его сместится влево, Н+-ионы сильной кислоты почти полностью свяжут окрашенные ионы Ind – в бесцветные молекулы HInd, и раствор обесцветится. Если же к раствору фенолфталеина прибавить щелочь (или внести фенолфталеин в раствор щелочи), то ее ОН–-ионы будут связывать Н+-ионы фенолфталеина, равновесие сместится вправо, в сторону увеличения ионов Ind –, и раствор окрасится в малиновый цвет.
Каждый индикатор меняет окраску раствора в определенном, характерном для него интервале значений рН, который называется областью перехода индикатора. Так, в присутствии фенолфталеина раствор бесцветен при рН ≤ 8, а при рН ≥ 10 имеет интенсивно-малиновую окраску. Область перехода фенолфталеина лежит в интервале рН, равном 8 - 10, т.е. в щелочной среде.
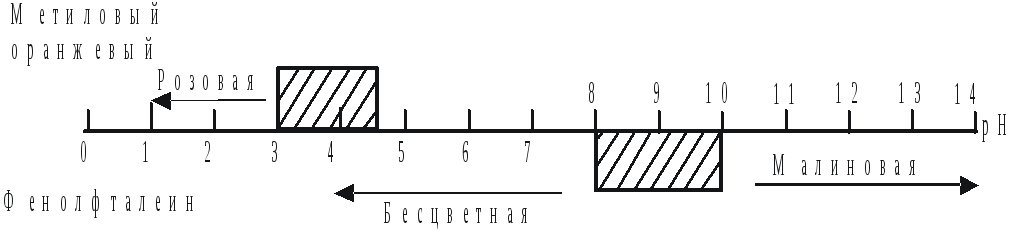
На рис.4 показано изменение окраски метилового оранжевого и фенолфталеина при различных значениях рН.
Рис.4.
Окраска метилового оранжевого и
фенолфталеина при различных
значениях
рН. ![]() - область перехода индикатора
- область перехода индикатора
Д
Оборудование и реактивы
Индикаторы: лакмус, фенолфталеин, метиловый оранжевый, метиловый красный, универсальная индикаторная бумага.
Растворы: соляной кислоты (0,1 н, 1 н); гидроксида натрия (0,1 н, 1 н).
Иономер.
Буферные растворы с номинальными значениями рН = 1,65; 4,01; 9,18.
Электрод ионоселективный стеклянный.
Электрод сравнения хлоридсеребряный.
Стаканы стеклянные на 100, 250 мл.
Пробирки 10 шт.
Фильтровальная бумага.
А. Определение рН воды с применением индикаторов
Для определения рН в кислой и щелочной средах наиболее часто применяют четыре индикатора: метиловый оранжевый, метиловый красный, лакмус и фенолфталеин. Наблюдения проведите в сильнокислой и сильнощелочной средах, чтобы в первом случае рН был заведомо ниже, а во втором - заведомо выше рН области перехода указанных индикаторов. Для этого в четыре пронумерованные пробирки внесите по 10 капель 0,1 н раствора соляной кислоты; в другие четыре пробирки, пронумерованные теми же номерами, - такой же объем 0,01 н раствора гидроксида калия. После этого в пробирки с кислотой и щелочью добавьте по 1 капле индикатора метилового оранжевого, метилового красного, лакмуса (5 капель) и фенолфталеина.
Наблюдения по изменению окраски индикаторов в кислой и щелочной средах запишите в форму табл.7, где уже указаны интервалы рН области перехода каждого индикатора и его окраска в этой области.
Форма таблицы 7
