
- •Работа № 1 Качественное определение ионов токсичных металлов в воде
- •Бесцветные ионы Цинк
- •Опыт 1. Определение цинка
- •Опыт 2. Определение кадмия
- •Опыт 3. Определение свинца
- •Опыт 4. Определение ртути иодидом калия
- •Опыт 5. Определение висмута (III) тиомочевиной
- •Окрашенные ионы Железо
- •Опыт 6. Определение железа (III)
- •Опыт 7. Определение хрома
- •Опыт 8. Определение меди
- •Опыт 9. Анализ воды на содержание ионов тяжелых металлов (контрольная задача)
- •Определение ионов тяжелых металлов
- •Работа № 2 Качественное определение ионов токсичных неметаллов в воде
- •Опыт 1. Определение сульфид-иона
- •Опыт 2. Обнаружение иона аммония
- •Опыт 3. Определение нитрит-иона no2‾
- •Опыт 4. Обнаружение нитрат-иона no3‾
- •Опыт 5. Определение аниона фтора
- •Опыт 6. Определение фосфора
- •Опыт 7. Определение мышьяка
- •Опыт 8. Анализ воды на содержание анионов неметаллов (контрольная задача)
- •Определение ионов неметаллов
- •Работа № 3 Жесткость воды
- •А. Определение карбонатной жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором hCl
- •Б. Определение общей жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором эдта
- •Работа № 4 Определение окисляемости воды методом перманганатометрии
- •Оборудование и реактивы
- •А. Определение окисляемости воды обратным титрованием
- •Б. Определение окисляемости воды прямым титрованием
- •Работа № 5 Фотометрическое определение примесей тяжелых металлов в пресной воде
- •А. Определение железа в виде роданидного комплекса
- •Результаты фотометрирования растворов
- •Оборудование и реактивы
- •Описание определения
- •Б. Определение меди в виде аммиачного комплекса а) Метод калибровочного графика Оборудование и реактивы
- •Описание определения
- •Б) Метод стандартных добавок
- •Описание определения
- •В. Определение висмута в виде тиокарбамидного комплекса
- •Оборудование и реактивы
- •Описание определения
- •Г. Определение титана и ванадия при их совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 6 Спектрофотометрическое определение примесей нефти и нефтепродуктов в природной воде
- •Внешний вид пленки нефти на поверхности воды в зависимости от ее толщины и количества нефти
- •Оборудование и реактивы
- •Описание определения
- •Электрохимические методы анализа объектов окружающей среды
- •Работа № 7 Определение рН воды и почвы
- •Оборудование и реактивы
- •А. Определение рН воды с применением индикаторов
- •Изменение окраски индикаторов
- •Б. Определение рН воды на иономере методом прямой потенциометрии
- •Описание определения
- •В. Определение рН почвы
- •Нормы внесения молотого известняка (кг/10 м2) при различных значениях pH почвы
- •Оборудование и реактивы
- •Работа № 8 Ионоселективное определение примесей различных ионов в природной и питьевой воде а. Определение хлорид-ионов
- •Основные характеристики ионоселективных электродов
- •Оборудование и реактивы
- •Описание определения
- •Результаты ионометрического определения ионов в воде
- •Б. Определение фторид-ионов
- •Оборудование и реактивы
- •Описание определения
- •В. Определение примесей железа
- •Оборудование и реактивы
- •Описание определения
- •Результаты титрования
- •Г. Определение нитрат-ионов
- •Оборудование и реактивы
- •Описание определения
- •Работа № 9 Определение содержания токсичных ионов тяжелых металлов в питьевой воде методом инверсионной вольтамперометрии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 10 Определение меди и цинка при их совместном присутствии на катионите ку-2
- •Раздельное вымывание примесей с катионита ку-2
- •Оборудование и реактивы
- •Описание определения
- •Работа № 11 Определение кадмия в растворах методом хроматографии на бумаге
- •Оборудование и реактивы
- •Описание определения
- •Результаты хроматографического определения ионов кадмия Работа № 12 Определение уровня радиационного загрязнения окружающей среды
- •Оборудование
- •Описание определения
- •Литература
- •Содержание
Электрохимические методы анализа объектов окружающей среды
Каждый электрохимический параметр (потенциал, сила тока, сопротивление и др.) связан с концентрацией анализируемого раствора.
В основе электрохимических методов лежит процесс электролиза - химические реакции, протекающие под действием электрического тока на электродах, помещенных в раствор электролита.
Различают прямые и косвенные электрохимические методы. В прямых методах используют зависимость потенциала (силы тока и т.д.) от концентрации определяемого компонента, в косвенных методах потенциал (силу тока и т.д.) измеряют с целью нахождения конечной точки титрования, т.е. используют зависимость измеряемого параметра от объема титранта.
Для любого рода электрохимических измерений необходима электрохимическая ячейка, составной частью которой является анализируемый раствор.
Если электрохимическая ячейка работает в режиме гальванического элемента (ГЭ) (ток возникает в результате самопроизвольной химической реакции), необходимо наличие двух электродов: индикаторного и электрода сравнения.
Индикаторными электродами могут служить: стеклянный, хингидронный, сурьмяный, водородный, серебряный, платиновый.
Индикаторный электрод обратим по катиону:
Me – nē Men+.
Уравнение Нернста для него имеет вид:
![]() или
или
![]() ,
,
a = [Men+] f,
где а - активность ионов; f - коэффициент активности; φ - стандартный электродный потенциал; [Men+] - концентрация ионов металлов, моль/л.
Электродами сравнения могут быть: хлоридсеребряный, каломельный, водородный.
Для измерения pH раствора необходим электрод, который реагирует на изменение [H+]. Такими электродами могут быть водородный, хингидронный, стеклянный, сурьмяный.
Наиболее удобен в работе стеклянный электрод, состоящий из тонкой pH-чувствительной мембраны, изготовленной из стекла, содержащего 22% оксида натрия, 6% оксида кальция и 72% оксида кремния. Внутри стеклянной мембраны находится хлоридсеребряный электрод, погруженный в 0,1 н раствор HCl.
В качестве электрода сравнения наиболее часто применяют хлоридсеребряный электрод, состоящий из серебряной проволочки, электролитически покрытой слоем хлорида серебра, и погруженный в раствор хлорида калия. Потенциал такого электрода определяется уравнением AgCl + ē = Ag + Cl− , φ = φAgCl/Ag,Cl− − 0,059lg[Cl−] и при 25 С равен 0,222 В.
Схема ГЭ имеет вид:
Ag|AgCl|0,1 н HCl|стекло[H+]|HClнасыщ.|AgCl|Ag.
Потенциал стеклянного электрода описывается уравнением
φ = K +0,059lg aH+,
где K - константа, зависящая от сорта стекла и устройства электрода; aH+ - активность ионов водорода.
Для определения K стеклянный электрод калибруют по нескольким буферным растворам. Электрод позволяет измерять pH от 0 до 13. На рис.3 показаны стеклянный и хлоридсеребряный электроды.
В качестве электрода сравнения вместо хлоридсеребряного электрода можно применять каломельный электрод. Он состоит из ртути, покрытой пастой Hg2Cl2, и погружен в насыщенный раствор KCl. Проволочка из пластины, опущенная в эту пасту, осуществляет контакт.
В основе работы каломельного электрода лежит окислительно-восстановительная полуреакция:
Hg2Cl2 (тв.) + 2ē 2Hg + 2 Cl–.
Схема ГЭ с использованием каломельного электрода в качестве электрода сравнения имеет вид:
Ag|AgCl|0,1 н HCl|стекло|[H+]|KClнасыщ.|Hg2Cl2|Hg.
Потенциал насыщенного каломельного электрода при 25 C равен 0,24 B.
Электроды сравнения содержат два раствора хлорида калия, один из которых (внешний) служит солевым мостиком и одновременно предотвращает загрязнение другого (внутреннего) раствора, исключая его
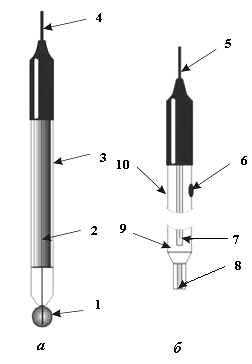
Рис.3. Стеклянный (а) и хлоридсеребряный (б) электроды: 1 - рН-чувствительная мембрана; 2 - 0,1 М раствор HCl, насыщенный AgCl; 3, 7 - серебряная проволочка, покрытая осадком AgCl и погруженная в KCl насыщ. (внутренний раствор); 4, 5 - контакты; 6 - отверстие для ввода раствора KCl; 8 - асбестовое волокно, обеспечивающее контакт с анализируемым раствором; 9 - внешний раствор KCl насыщ.; 10 - стеклянный корпус
контакт с анализируемым раствором. Такие электроды называют электродами с двойным солевым мостиком. ЭДС ГЭ Е рассчитывается по разнице потенциалов электродов сравнения и индикаторного:
E = φAgCl/Ag, Cl− − φстекл, так как φстекл = 0,059[H+],
E = φAgCl/Ag, Cl− − 0,059[H+] (pH = − lg[H+]),
pH =
![]() .
.
Этот расчет автоматически выполняет иономер, и на панели прибора сразу выдается значение pH.
