
- •Работа № 1 Качественное определение ионов токсичных металлов в воде
- •Бесцветные ионы Цинк
- •Опыт 1. Определение цинка
- •Опыт 2. Определение кадмия
- •Опыт 3. Определение свинца
- •Опыт 4. Определение ртути иодидом калия
- •Опыт 5. Определение висмута (III) тиомочевиной
- •Окрашенные ионы Железо
- •Опыт 6. Определение железа (III)
- •Опыт 7. Определение хрома
- •Опыт 8. Определение меди
- •Опыт 9. Анализ воды на содержание ионов тяжелых металлов (контрольная задача)
- •Определение ионов тяжелых металлов
- •Работа № 2 Качественное определение ионов токсичных неметаллов в воде
- •Опыт 1. Определение сульфид-иона
- •Опыт 2. Обнаружение иона аммония
- •Опыт 3. Определение нитрит-иона no2‾
- •Опыт 4. Обнаружение нитрат-иона no3‾
- •Опыт 5. Определение аниона фтора
- •Опыт 6. Определение фосфора
- •Опыт 7. Определение мышьяка
- •Опыт 8. Анализ воды на содержание анионов неметаллов (контрольная задача)
- •Определение ионов неметаллов
- •Работа № 3 Жесткость воды
- •А. Определение карбонатной жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором hCl
- •Б. Определение общей жесткости воды Оборудование и реактивы
- •Результаты титрования воды раствором эдта
- •Работа № 4 Определение окисляемости воды методом перманганатометрии
- •Оборудование и реактивы
- •А. Определение окисляемости воды обратным титрованием
- •Б. Определение окисляемости воды прямым титрованием
- •Работа № 5 Фотометрическое определение примесей тяжелых металлов в пресной воде
- •А. Определение железа в виде роданидного комплекса
- •Результаты фотометрирования растворов
- •Оборудование и реактивы
- •Описание определения
- •Б. Определение меди в виде аммиачного комплекса а) Метод калибровочного графика Оборудование и реактивы
- •Описание определения
- •Б) Метод стандартных добавок
- •Описание определения
- •В. Определение висмута в виде тиокарбамидного комплекса
- •Оборудование и реактивы
- •Описание определения
- •Г. Определение титана и ванадия при их совместном присутствии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 6 Спектрофотометрическое определение примесей нефти и нефтепродуктов в природной воде
- •Внешний вид пленки нефти на поверхности воды в зависимости от ее толщины и количества нефти
- •Оборудование и реактивы
- •Описание определения
- •Электрохимические методы анализа объектов окружающей среды
- •Работа № 7 Определение рН воды и почвы
- •Оборудование и реактивы
- •А. Определение рН воды с применением индикаторов
- •Изменение окраски индикаторов
- •Б. Определение рН воды на иономере методом прямой потенциометрии
- •Описание определения
- •В. Определение рН почвы
- •Нормы внесения молотого известняка (кг/10 м2) при различных значениях pH почвы
- •Оборудование и реактивы
- •Работа № 8 Ионоселективное определение примесей различных ионов в природной и питьевой воде а. Определение хлорид-ионов
- •Основные характеристики ионоселективных электродов
- •Оборудование и реактивы
- •Описание определения
- •Результаты ионометрического определения ионов в воде
- •Б. Определение фторид-ионов
- •Оборудование и реактивы
- •Описание определения
- •В. Определение примесей железа
- •Оборудование и реактивы
- •Описание определения
- •Результаты титрования
- •Г. Определение нитрат-ионов
- •Оборудование и реактивы
- •Описание определения
- •Работа № 9 Определение содержания токсичных ионов тяжелых металлов в питьевой воде методом инверсионной вольтамперометрии
- •Оборудование и реактивы
- •Описание определения
- •Работа № 10 Определение меди и цинка при их совместном присутствии на катионите ку-2
- •Раздельное вымывание примесей с катионита ку-2
- •Оборудование и реактивы
- •Описание определения
- •Работа № 11 Определение кадмия в растворах методом хроматографии на бумаге
- •Оборудование и реактивы
- •Описание определения
- •Результаты хроматографического определения ионов кадмия Работа № 12 Определение уровня радиационного загрязнения окружающей среды
- •Оборудование
- •Описание определения
- •Литература
- •Содержание
Оборудование и реактивы
Фотоколориметр.
Стеклянные кюветы на 3 см, 2 шт.
Цилиндр на 20 мл, 1 шт.
Пипетка на 10 мл, 1 шт.
Мерные колбы на 50 мл, 7 шт.
Азотная кислота, 1 н.
Тиомочевина, 10%-ный раствор.
Стандартный раствор висмута 0,1 мг Bi3+ в 1 мл готовят, растворяя 0,2321 г соли Bi(NO3)3∙5H2O в 100 мл HNO3 (1:3) в мерной колбе на 1000 мл и добавляя дистиллированную воду до метки.
Описание определения
Для построения калибровочного графика в четыре мерные колбы на 50 мл отмерьте пипеткой соответственно 1, 2, 3 и 5 мл стандартного раствора Bi3+. В каждую колбу добавьте по 15 мл 1 н HNO3, 10 мл 10%-ного раствора тиомочевины, дистиллированной воды до метки и перемешайте.
Измерив оптическую плотность всех растворов, постройте калибровочный график. При этом по оси абсцисс отложите известные концентрации ионов Bi3+ (т.е. 0,02; 0,04; 0,06; 0,10 мг висмута в 1 мл), а по оси ординат - соответствующие им оптические плотности растворов.
Для определения висмута в исследуемом растворе, приготовленном в колбе на 50 мл, добавьте 15 мл 1 н HNO3, 10 мл 10%-ного раствора тиомочевины, дистиллированной воды до метки и перемешайте. Наполните раствором кювету и измерьте оптическую плотность раствора при тех же условиях, при каких был получен калибровочный график.
Зная оптическую плотность, найдите по графику концентрацию иона Bi3+ в мг на 1 мл раствора. Умножив ее на объем всего анализируемого раствора (50 мл), вычислите общее количество висмута.
Г. Определение титана и ванадия при их совместном присутствии
Определение титана и ванадия при их совместном присутствии основано на различии спектров поглощения пероксидных комплексов титана [TiO(H2O2)]2+ и ванадия [VO(H2O2)]3+.
Приготавливают окрашенный раствор смеси катионов титана и ванадия и измеряют ее оптическую плотность при 619 нм, когда свет поглощает практически лишь окрашенный комплекс ванадия, и при 400 нм, когда наблюдается суммарное светопоглощение окрашенными соединениями обоих катионов.
М
Рис.2.
Калибровочные графики для определения
титана и ванадия при их совместном
присутствии: 1
- ванадий
(λ = 400 нм); 2 - ванадий
(λ = 619 нм); 3 - титан
(λ = 400 нм)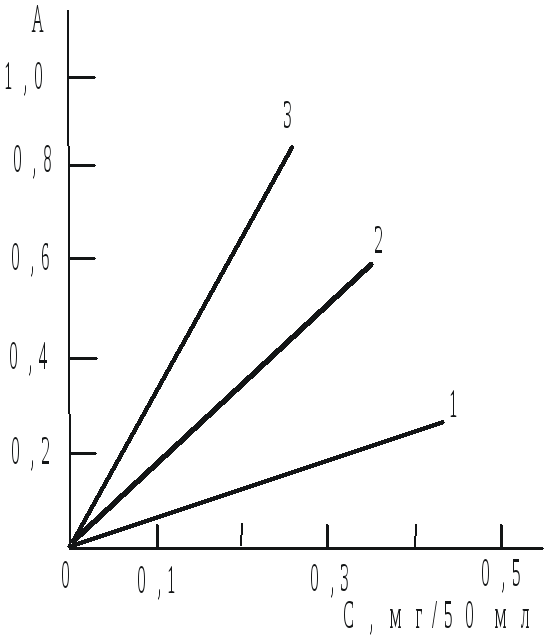
Затем измеряют оптическую плотность (Ax619) исследуемого раствора, содержащего вместе ионы титана и ванадия, при λ = 619 нм и по кривой 2 сразу же определяют концентрацию ванадия в анали-зируемом растворе. Одновременно по кривой 3 находят по этой концентрации оптическую плотность (Ax400) раствора ванадия при λ = 400 нм, оставив только долю (ATi400 = A400Ti+V – AV400), и по кривой 1 определяют концентрацию Ti в исследуемой смеси.
Оборудование и реактивы
Фотоколориметр или спектрофотометр.
Кюветы на 2 см, 3 - 4 шт.
Пипетки на 10 мл, на 2 мл по 2 шт.
Колбы мерные на 50 мл, 12 шт.
Пероксид водорода, 3%-ный раствор.
Серная кислота, 5%-ный раствор.
Стандартный раствор ванадия - 0,2 мг V (V) в 1 мл - готовят растворением 0,4593 г NH4VO3 в 100 мл H2SO4 (1:1) и разбавлением водой до 1 л.
Стандартный раствор титана - 0,2 мг Ti (IV) в 1 мл - готовят растворением 0,8183 г TiOSO42H2O в 100 мл H2SO4 (1:1) и разбавлением водой до 1 л.
