
- •Г.А. Тихановская, л.М. Воропай, в.В. Кочетова химия
- •Предисловие
- •Введение
- •Основные понятия и законы в химии
- •1.1. Основные химические понятия
- •1.2 Закон эквивалентов. Понятие эквивалент. Молярная масса эквивалента
- •1.3. Законы газового состояния. Определение молярных масс газообразных веществ
- •2. Строение атома и периодический закон д.И.Менделеева
- •2.1. Этапы на пути создания квантовой механики
- •2.2. Элементы квантово-механической теории атома
- •Характеристика квантовых чисел
- •3. Типы химической связи
- •3.1. Ковалентная связь. Метод валентных связей
- •Возможная геометрическая конфигурация молекул при Sp3 – гибридизации
- •3.2. Ионная связь
- •3.3. Металлическая связь
- •3.4. Водородная связь
- •3.5. Молекулярное взаимодействие
- •4. Общие закономерности протекания и типы химических реакций
- •4.1. Энергетика химических превращений
- •4.1.1. Термохимия. Закон Гесса
- •4.1.2. Энтропия
- •4.1.3. Энергия Гиббса и направленность химических процессов
- •4.2. Химическая кинетика
- •Стандартные теплоты (энтальпии) образования некоторых веществ
- •Стандартная энергия Гиббса образования некоторых веществ
- •Стандартные абсолютные энтропии некоторых веществ
- •4.2.1. Скорость химической реакции
- •4.2.2. Физические методы стимулирования химических превращений
- •4.2.3. Катализ
- •4.3. Химическое равновесие
- •4.3.1. Константа химического равновесия
- •4.3.2. Принцип Ле Шателье
- •5. Дисперсные системы
- •5.1. Способы выражения концентрации растворов
- •5.2. Свойства разбавленных растворов
- •5.3 Растворы электролитов
- •Степень диссоциации различных электролитов
- •5.4. Ионное произведение воды. Водородный показатель
- •5.5 Равновесие в гетерогенных системах, произведение растворимости
- •6. Гидролиз солей
- •Примеры сильных и слабых кислот и оснований
- •6.1. Произведение растворимости. Примеры решения задач
- •7. Жесткость воды
- •8. Окислительно-восстановительные процессы
- •8.1. Электродные потенциалы и электродвижущие силы
- •Стандартные электронные потенциалы(∆е0) некоторых металлов
- •8.2. Электролиз
- •8.3. Коррозия металлов
- •9. Кристаллическое состояние
- •9.1.Основные понятия
- •9.2 Симметрия кристаллов. Система кристаллов
- •9.3. Кристаллические решетки
- •10. Сплавы
- •10.1. Диаграммы состояния металлических систем
- •Библиографический список
- •Произведение растворимости малорастворимых веществ в воде при 25оС
- •Стандартные, окислительно – восстановительные потенциалы ( по отношению к потенциалу стандартного водородного электрода при t 25oC).
- •Термодинамические константы некоторых веществ
- •Оглавление
1.3. Законы газового состояния. Определение молярных масс газообразных веществ
Три параметра – объем V, давление P и температура T (T=273+t) – определяют физическое состояние газа. Давление 1,013∙105Па (760 мм рт. ст.) и температура 273 К или 0оС называют нормальными условиями состояния газа, что в буквенных обозначениях этих величин указывается индексом: Po, To, to. Объем газа при н.у. – Vo.
Закон Бойля – Мариотта. При постоянной температуре объем данной массы газа изменяется обратно пропорционально давлению:
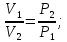
или V1 P1= V2 P2=V3P3…, т.е. V∙P=const.
Закон Гей-Люссака. При постоянном давлении объем данной массы газа меняется прямо пропорционально абсолютной температуре
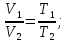
При постоянном объеме:

Уравнение Менделеева – Клапейрона. Объединение законов Бойля, Мариотта и Гей-Люссака дает уравнение состояния газа
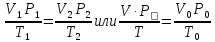
если
одно из состояний является нормальным.
Для любого газа количеством вещества
1 моль величина
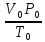 постоянна
и одинакова, поэтому её называют
универсальной газовой постояннойR.
Если
постоянна
и одинакова, поэтому её называют
универсальной газовой постояннойR.
Если
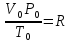 ,
тоVP=RT,
а для газа количеством вещества n
моль Vp=nRT.
Так как n
равно отношению массы вещества к его
молярной массе, то
,
тоVP=RT,
а для газа количеством вещества n
моль Vp=nRT.
Так как n
равно отношению массы вещества к его
молярной массе, то
 – это равенство и являетсяурав-нением
Менделеева – Клапейрона
в окончательном виде. Числовые значения
универсальной газовой постоянной
зависят от того, в каких единицах выражены
объем и давление газа. Так, в системе СИ
единица объема – кубический метр, а
единица давления – паскаль (Па), т.е.
сила в 1 ньютон, приходящаяся 1м2
площади (Н/м2).
Ньютон (Н) – сила, сообщающая массе в
1кг ускорение в 1 м/с. Джоуль – работа
силы в 1 ньютон на расстоянии в 1м.
Подставляя соответствующие значения
в формулу
– это равенство и являетсяурав-нением
Менделеева – Клапейрона
в окончательном виде. Числовые значения
универсальной газовой постоянной
зависят от того, в каких единицах выражены
объем и давление газа. Так, в системе СИ
единица объема – кубический метр, а
единица давления – паскаль (Па), т.е.
сила в 1 ньютон, приходящаяся 1м2
площади (Н/м2).
Ньютон (Н) – сила, сообщающая массе в
1кг ускорение в 1 м/с. Джоуль – работа
силы в 1 ньютон на расстоянии в 1м.
Подставляя соответствующие значения
в формулу , получим
, получим
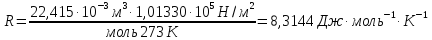
Если объем газа измерен в литрах, а давление газа в мегапаскалях (МПа=106Па), то R=0,083л∙МПа∙моль-1∙К-1. В расчетах обычно используют числа, имеющие три значащие цифры, что дает вполне достаточную точность: 22,4910-3 м3, 22,4 л, 273 К, 8,31 Дж∙моль-1∙К-1.
Согласно закону Авогадро, в равных объемах любых газов, взятых при одной и той же температуре и одинаковом давлении, содержится одинаковое число молекул.
Иными словами, одно и то же число молекул любого газа занимает при одинаковых условиях один и тот же объем. Вместе с тем 1 моль любого газа содержит одинаковое число молекул. Следовательно, при одинаковых условиях 1 моль любого газа занимает один и тот же объем. Этот объем называется мольным объемом газа и при нормальных условиях (00С, давление 101,325 кПа) равен 22,4 л.
Пример 1.Определить объём, занимаемый 5,25 г азота при 260С и давлении 98,9 кПа (742 мм рт.ст.).
Решение. Зная мольный объём и мольную массу (28,0 г/моль) азота, находим объём, который будут занимать 5,25 г азота при нормальных условиях:
28,0 г азота занимают объём 22,4л
5,25 г азота занимают объём VO ,
откуда VO = 5,25∙22,4/ 28,0 = 4,20 л
Затем приводим полученный объём к указанным в задаче условиям:
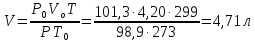
Пример 2. При 250С и давлении 99,3 кПа (745 мм рт.ст.) некоторое количество газа занимает объём 152 мл. Найти, какой объём займет это же количество газа при 00С и давлении101,33 кПа.
Решение. Подставляя данные задачи в последнее уравнение, получаем:

Пример 3. Некоторый газ массой 5,6 г занимает объём 4,84 л при температуре 170С и давлении 0,997∙105 Па. Чему равна относительная молекулярная масса этого газа?
Решение.
Из уравнения Менделеева-Клайперона
 , откуда
, откуда
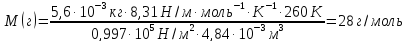
Так как числовое значение молярной массы, выраженной в г/моль, равно относительной молекулярной массе, т.е. {M}=Mr , то Mr = 28.
