
Биохимия растений
.pdf
живается рост цепи синтезируемой жирной кислоты и ее пере˝ход от одного фермента к другому в пределах мультиферментног˝о комплекса. Строение ацилпереносящего белка можно предст˝авить в виде следующей схемы:
Под действием фермента АПБ-ацетилтрансферазы (2.3.1.38) остаток уксусной кислоты от ацетил-КоА переносится на АПБ˝:
(2)
С участием другого фермента АПБ-малонилтрансферазы (2.3.1.39) на АПБ переносится также остаток малоновой кислоты
от малонил-КоА:
(3)
В следующей реакции, происходящей в мультиферментном ком˝- плексе синтетазы жирных кислот, под действием фермента 3-îêñî- ацил-АПБ-синтазы (3.3.1.41) из двууглеродного и трехуглеродного
радикалов ацетил-АПБ и малонил-АПБ происходит образовани˝е четырехуглеродного фрагмента, соединенного с АПБ. При этом в ходе реакции молекула малонил-КоА декарбоксилируется и в˝ ка- честве продукта данного превращения выделяется та же молекула
ÑÎ2, которая вошла в состав малонил-КоА в результате карбокси˝-
лирования ацетил-КоА:
(4)
391

Таким образом, карбоксилирование ацетил-КоА можно рассматривать как реакцию активирования ацетильного радик˝ала для переноса на соответствующий акцептор, который представл˝яет собой ацильный радикал, соединенный с АПБ в ферментном ко˝м-
плексе синтетазы жирных кислот.
Образовавшееся 3-оксоацилпроизводное далее подвергаетс˝я
восстановлению под действием фермента 3-оксоацил-АПБ-редук- òàçû (1.1.1.100), который использует в качестве донора электро-
нов и протонов восстановленные динуклеотиды НАДФ · Н. В р˝е-
зультате восстановительной реакции синтезируется 3-окси˝произ-
водное:
(5)
Как известно, источником образования восстановленных ди˝-
нуклеотидов НАДФ · Н служит фотосинтетическое фосфорилиро-
вание или реакции пентозофосфатного цикла.
В следующей реакции от 3-оксибутирил-АПБ отщепляется молекула воды с образованием α,β-ненасыщенного производного
кротонил-АПБ. Данное превращение катализирует фермент êðî- тонил-АПБ-гидратаза (4.2.1.58):
(6)
Ненасыщенное производное восстанавливается ферментом
еноил-АПБ-редуктазой (1.3.1.10), который использует в качестве
донора электронов и протонов восстановленные динуклеот˝иды НАДФ · Н:
(7)
392

На следующем этапе синтеза жирной кислоты бутирил-АПБ становится акцептором ацетильного радикала, переносимо˝го от малонил-АПБ, в результате осуществляется синтез уже шести˝углеродного 3-оксоацил-АПБ. Затем происходят реакции (5—7), в
ходе которых синтезируется восстановленное шестиуглеро˝дное производное гексаноил-АПБ. Оно также становится акцептор˝ом
ацетильного радикала, переносимого от малонил-АПБ, снова ˝повторяются реакции (5—7), дающие уже восьмиуглеродное восста-
новленное производное, связанное с АПБ. По аналогичной сх˝е-
ме указанные реакции повторяются до тех пор, пока полност˝ью
не синтезируется углеводородная цепь жирной кислоты, кот˝орая
далее вследствие ослабления связи с АПБ переносится на ко˝фермент А:
Длина синтезированной углеводородной цепи жирной кисло˝ты
определяется природой ферментного комплекса синтетазы ˝жир-
ных кислот, которая зависит от генотипа организма. Как вид˝но, в указанных ранее реакциях синтез жирной кислоты происход˝ит в
результате переноса на восстановленный акцептор двуугл˝еродного
фрагмента от малонил-АПБ, имеющего трехуглеродный радика˝л.
При этом каждый такой перенос сопровождается выделением˝
ÑÎ2. Вначале акцептором двууглеродного фрагмента служит аце- тил-АПБ, затем бутирил-АПБ, гексаноил-АПБ и т. д. В общем
виде ход удлинения углеродной цепи жирной кислоты в проце˝ссе
ее синтеза можно показать в виде следующей схемы:
Ñ2 + Ñ3 → Ñ4 + Ñ1 Ñ4 + Ñ3 → Ñ6 + Ñ1
Ñ6 + Ñ3 → Ñ8 + Ñ1 è ò. ä.
Согласно такой схеме синтеза в образующихся жирных кисло˝- тах всегда содержится четное число углеродных атомов.
Учитывая, что исходным веществом для синтеза жирных кис-
лот является ацетил-КоА и на отдельных этапах синтеза исп˝ользуются молекулы АТФ (при образовании малонил-КоА), восстанов˝- ленных динуклеотидов НАДФ · Н и воды, суммарное уравнени˝е синтеза насыщенной жирной кислоты на примере пальмитино˝вой кислоты можно записать следующим образом:
393
В ходе синтеза молекулы пальмитиновой кислоты 7 раз осуще˝- ствляется перенос на акцептор двууглеродного фрагмента˝ от мало- нил-АПБ, при образовании каждой молекулы которого происхо˝- дит гидролиз АТФ. При этом на каждом этапе процесса удлине˝-
ния углеводородной цепи жирной кислоты дважды повторяют˝ся реакции восстановления с участием восстановленных дину˝клеоти-
äîâ ÍÀÄÔ · Í.
У растений, животных и бактерий преобладают жирные кисло-˝
ты с четным числом углеродных атомов. Однако в клетках нек˝ото-
рых бактерий в значительном количестве синтезируются жи˝рные
кислоты с нечетным числом углеродных атомов. Это обусловл˝ено
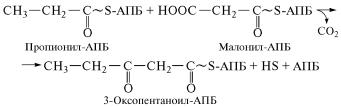
тем, что в клетках бактерий наряду с ацетилкоферментом А в˝ажным ключевым метаболитом является пропионилкофермент А˝,
который вместо ацетил-КоА может связываться с ацилперено˝ся-
щим белком и вступать во взаимодействие с малонил-АПБ, обра-
зуя пятиуглеродное 3-оксопроизводное:
Затем пятиуглеродное 3-оксопроизводное восстанавливает˝ся,
проходя такие же стадии превращений, которые представлен˝ы в
реакциях (5—6) синтеза жирных кислот с участием ферментног˝о
комплекса синтетазы жирных кислот. Восстановленный пяти˝угле-
родный фрагмент далее становится акцептором нового двуу˝глеродного фрагмента от малонил-АПБ, после чего снова проход˝ят
восстановительные реакции, приводящие к синтезу семиугл˝ерод-
ного восстановленного фрагмента, который снова становит˝ся акцептором следующего двууглеродного фрагмента и т. д. Из п˝редставленного механизма синтеза видно, что на конечном этап˝е образуется восстановленная углеводородная цепь жирной ки˝слоты с
нечетным числом углеродных атомов. Синтез жирной кислоты˝ с
нечетным числом углеродных атомов можно представить в ви˝де следующей схемы:
Ñ3 + Ñ3 → Ñ5 + Ñ1
Ñ5 + Ñ3 → Ñ7 + Ñ1
Ñ7 + Ñ3 → Ñ9 + Ñ1 è ò. ä.
В составе некоторых разновидностей липидов бактерий, пти˝ц и
растений найдены жирные кислоты, имеющие в углеродной цеп˝и
394

боковые ответвления. Как установлено, такие жирные кислот˝ы могут синтезироваться с участием в качестве акцептора дв˝ууглеродных фрагментов разветвленных ацильных производных, о˝бразующихся при распаде аминокислот с разветвленной углеро˝дной
цепью — валина, лейцина, изолейцина:
Универсальным донором разветвленных ацильных радикалов˝
при синтезе жирных кислот является пропионилкофермент А˝, ко-
торый, подвергаясь карбоксилированию, превращается в мет˝ил-
малонилкофермент А:
Затем ацильный радикал метилмалонил-КоА переносится на ацилпереносящий белок ферментного комплекса синтетазы ˝жирных кислот и участвует далее в синтезе жирных кислот в кач˝естве
донора разветвленного ацильного радикала:
395

После восстановления разветвленного оксопроизводного о˝бразуется восстановленный ацильный радикал, имеющий боково˝е метильное ответвление у второго углеродного атома. Он слу˝жит далее акцептором следующего двууглеродного фрагмента с˝ боко-
вым метильным радикалом, донор которого — метилмалонилАПБ. Таким образом, с участием метилмалонильного радикала˝
после каждого акта удлинения ацильного радикала углерод˝ная цепь синтезируемой жирной кислоты удлиняется на два угле˝род-
ных атома, а у каждого четного углеродного атома имеется б˝око-
вой метильный радикал.
Если к исходному акцептору с радикалом R происходит после˝-
довательное присоединение четырех двууглеродных фрагме˝нтов с боковым метильным радикалом и на каждом этапе их присоеди˝-
нения осуществляется восстановление полученных 3-оксопр˝оиз-
водных, строение синтезированной жирной кислоты можно за˝пи-
сать в виде следующей формулы:
В составе растительных жиров и липидов клеточных мембран˝
преобладают ненасыщенные жирные кислоты. Они синтезирую˝тся из насыщенных кислот путем их дегидрогенизации в аэробны˝х ус-
ловиях, т. е. с участием кислорода. В анаэробных условиях п˝роисхо-
дит синтез насыщенных кислот. Кроме кислорода важнейшими˝
соединениями, необходимыми для синтеза ненасыщенных жирных
кислот, являются восстановленные динуклеотиды НАДФ · Н˝. На
свету в образовании ненасыщенных кислот участвует ферре˝до-
êñèí.
Процесс дегидрогенизации насыщенных жирных кислот ката˝- лизируют ферменты оксигеназы, которые также называют десатуразами. Различают два вида десатураз — I и II. Десатуразы I имеются в клетках растений, животных, грибов, простейших орга˝низ-
мов. Они локализованы в цитозоле и способны инициировать ˝об-
разование олеиновой кислоты из стеариновой, образующей соединение с коферментом А — стеароил-КоА:
396
Синтез полиненасыщенных жирных кислот в клетках растени˝й осуществляют десатуразы II, локализованные в эндоплазмати˝ческом ретикулуме, они образуются с участием полирибосом, св˝язанных с мембранами эндоплазматической сети. В клетках челов˝ека и
животных превращения олеоил-КоА в линолеоил-КоА не проис-˝ ходит, поэтому полиненасыщенные жирные кислоты (линолева˝я,
линоленовая) являются для них незаменимыми компонентами˝ пищи.
Линолевая кислота, содержащая две двойные связи, образует˝ся
в результате дегидрогенизации олеоил-КоА по такому же мех˝аниз-
му, как и синтез олеоил-КоА из стеароил-КоА. Далее по указан˝-
ному механизму происходит дегидрогенизация линолеоил-К˝оА с образованием линоленоил-КоА. У животных в клетках печени ˝в
результате дегидрогенизации линолеоил-КоА синтезируетс˝я про-
изводное арахидоновой кислоты — арахидоноил-КоА.
Поскольку для синтеза ненасыщенных жирных кислот необхо˝-
димы кислород и восстановленные динуклеотиды НАДФ · Н, при недостатке последних образование данных кислот ослабля˝ется.
Так, например, происходит в условиях повышенных температу˝р,
когда снижается растворимость О2 в жидкой физиологической
среде. При избыточном азотном питании увеличивается доля˝ вос-
становленных динуклеотидов НАДФ · Н, затрачиваемых на восстановление нитритов и синтез аминокислот, и они меньше у˝ча-
ствуют в дегидрогенизации насыщенных жирных кислот, всле˝д-
ствие чего синтез ненасыщенных жирных кислот уменьшаетс˝я.
10.2. СИНТЕЗ АЦИЛГЛИЦЕРИНОВ
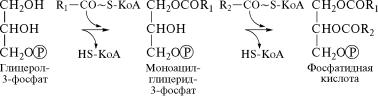
Исходные соединения для синтеза ацилглицеринов — глице˝-
рол-3-фосфат и активированные жирные кислоты, соединенные˝ с
коферментом А. В ходе синтеза ацилглицеринов последовате˝льно осуществляется перенос двух ацильных радикалов жирных к˝ислот на глицерол-3-фосфат под действием фермента глицеролфосфатацилтрансферазы (2.3.1.15) с образованием фосфатидной кислоты:
Фосфатидная кислота является важным промежуточным мета˝-
болитом в синтезе как ацилглицеринов, так и фосфолипидов ˝и
397
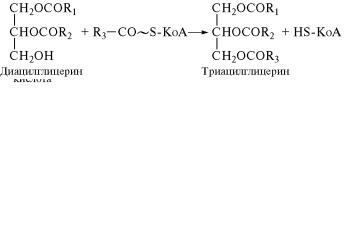
гликолипидов. В результате гидролиза фосфоэфирной связи˝ под действием фосфатидатфосфогидролазы (3.1.3.4) фосфатидная кислота превращается в диацилглицерин:
При переносе на диацилглицерин третьего ацильного остат˝ка
осуществляется синтез триацилглицерина — основного хи˝мического компонента жира:
Радикал R3 в этой реакции, как правило, представлен остатком ненасыщенной жирной кислоты. Учитывая, что радикалы R1, R2,
R3 представляют собой остатки разных жирных кислот, совершенно очевидно, что синтезируемый жир включает определенную˝ смесь ацилглицеринов, состав которой зависит от генотипа˝ и фазы развития растений, а также от условий окружающей сре˝ды.
Хорошими объектами для изучения процесса синтеза ненасы˝-
щенных жирных кислот и ацилглицеринов являются созреваю˝щие семена масличных растений. При их созревании усиливается˝ синтез ненасыщенных жирных кислот, о чем свидетельствует уве˝ли- чение иодного числа, и происходит превращение жирных кисл˝от в ацилглицерины жира, которое сопровождается уменьшением˝ кислотного числа.
10.3.СИНТЕЗ ФОСФОЛИПИДОВ
Âопытах с использованием меченых биохимических предше-
ственников показано, что молекулы фосфолипидов образуют˝ся из
фосфатидных кислот и других соединений, представленных э˝та-
ноламином, холином, серином, глицерином, миоинозитом. В ци-
топлазме растительных клеток фосфатидные кислоты превр˝аща-
398
ются в диацилглицерины, которые уже далее участвуют в син˝тезе фосфолипидов — фосфатидилэтаноламинов и фосфатидилхо˝линов. На первом этапе происходит активирование азотистых осно˝ваний в ходе реакций фосфорилирования с образованием этанолам˝ин-
фосфата и холинфосфата. Эти реакции катализируют фермент˝ы
этаноламинкиназа (2.7.1.31) è холинкиназа (2.7.1.32):
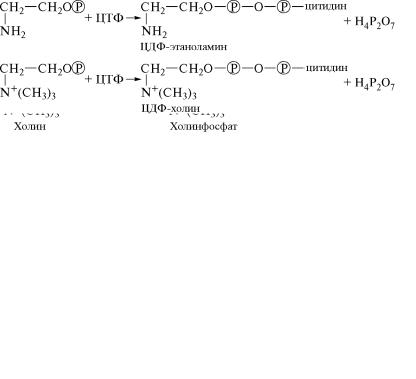
Этаноламинфосфат и холинфосфат подвергаются затем акти˝- вированию с участием макроэргического соединения цитид˝ин-
трифосфата (ЦТФ), в результате чего образуются цитидиндиф˝ос-
фатэтаноламин (ЦДФ-этаноламин) и цитидиндифосфатхолин (ЦДФ-холин):
Эти реакции катализируют ферменты этаноламинфосфатцитидилилтрансфераза (2.7.7.14) è холинфосфатцитидилилтрансфераза
(2.7.7.15).
Соединение диацилглицеринов с цитидиндифосфатпроизвод˝-
ными этаноламина и холина происходит с участием ферменто˝в
этаноламинфосфотрансферазы (2.7.8.1) è холинфосфотрансферазы
(2.7.8.2). В этих реакциях осуществляется синтез фосфатидилэта˝-
ноламина и фосфатидилхолина, а в качестве побочного проду˝кта высвобождается цитидиловая кислота (ЦМФ):
399
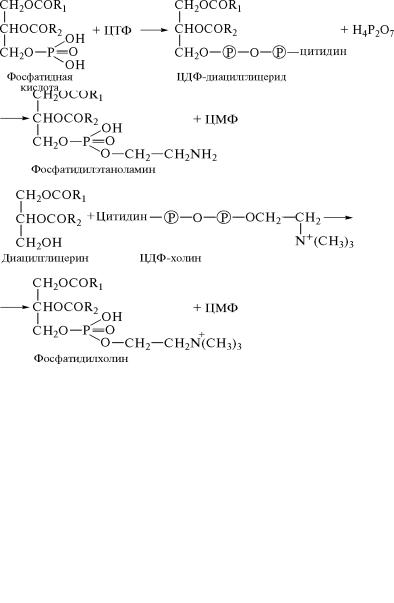
Следует отметить, что в процессе синтеза фосфолипидов реа˝-
лизуется такой механизм присоединения ацильных радикал˝ов к
глицерол-3-фосфату, при котором радикал R1 обычно представлен
остатком насыщенной жирной кислоты, а радикал R2 — ненасыщенной.
При синтезе фосфолипидов в хлоропластах и митохондриях а˝к- тивированию подвергается фосфатидная кислота в результ˝ате вза-
имодействия с ЦТФ:
В последующих реакциях остаток цитидиловой кислоты в мо-
лекуле ЦДФ-диацилглицерида может замещаться на серин или˝
400
