
Биохимия растений
.pdfзатрачивается на восстановление 1 моля СО2 до уровня гексозы, соответственно равно 91,8 + 439,6 = 531,4 кДж, которое составляет
≈38 % поглощенной энергии восьми квантов света. Определенно˝е
количество поглощенной энергии может затрачиваться так˝же на другие энергетические процессы, происходящие в листьях р˝астений (транспорт веществ и ионов через мембраны, синтез жирн˝ых
кислот, восстановление нитратов и др.).
Образовавшиеся в цикле Кальвина молекулы фруктозо-6-фос- фата и других фосфорнокислых эфиров моносахаридов, а такж˝е
фосфоглицериновой кислоты далее используются на синтез˝ раз-
личных органических веществ или подвергаются окислению˝ в ходе дыхательных реакций. На каждом этапе их превращений
только часть выделяющейся энергии может быть полезно исп˝оль-
зована, тогда как значительное ее количество рассеиваетс˝я в виде теплоты, флуоресценции, испарения и др. Поэтому в конечном˝
итоге на прирост биомассы растений расходуется всего лиш˝ь 1—
2 % всей поглощенной световой энергии, которую называют фотосинтетически активной радиацией (ÔÀÐ).
Перед учеными и специалистами, которые занимаются выра-
щиванием растений, стоит важная задача — повышение эффе˝к- тивности использования солнечной энергии в агроценозах˝. Осо-
бого внимания заслуживают селекционно-генетические и ге˝нно-
инженерные проекты, направленные на создание генотипов с˝ повышенной карбоксилирующей активностью фермента рибуло-
зодифосфаткарбоксилазы.
9.1.6. КОНЕЧНЫЕ ПРОДУКТЫ ФОТОСИНТЕЗА
Образовавшиеся в цикле Кальвина С3-продукты (3-фосфогли- цериновая кислота, 3-фосфоглицериновый альдегид и фосфоди˝- оксиацетон), а также фруктозо-6-фосфат не накапливаются в х˝лоропластах. Они участвуют в синтезе сахарозы, крахмала, ами˝нокислот, органических кислот, липидов и белков как непосре˝д- ственно в хлоропластах, так и в цитоплазме фотосинтезирую˝щих клеток. Фруктозо-6-фосфат в значительном количестве изоме˝ризуется в глюкозо-6-фосфат, который далее используется для с˝интеза крахмала. Содержание крахмала может достигать 90 % общ˝его объема хлоропластов.
Синтез сахарозы происходит в цитоплазме, в которую легко
диффундируют из хлоропластов фосфоглицериновая кислота˝,
фосфоглицериновый альдегид и фосфодиоксиацетон. Из трио˝з по известным механизмам образуются гексозы, а уже с их участ˝ием
синтезируются молекулы сахарозы (см. с. 376—378). Бó льшая
311
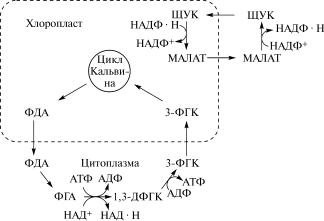
Рис. 9.6. Перенос энергетических (АТФ) и восстановительных п˝отенциалов (НАД · Н и НАДФ · Н) из хлоропласта в цитоплазму:
ФДА — фосфодиоксиацетон; ФГА — фосфоглицериновый альдегид; 1,3-ДФГК — 1,3-дифосфо- глицериновая кислота; ЩУК — шавелевоуксусная кислота; М˝АЛАТ — яблочная кислота
часть синтезированной в цитоплазме сахарозы транспорти˝руется в
акцепторные клетки по флоэме.
В ходе фотосинтеза в цитоплазме инициируются и другие про˝- цессы: синтез жирных кислот, восстановление нитратов и су˝льфа-
тов, образование липидов, белков и других веществ. Для их ос˝уще-
ствления необходимы биоэнергетические продукты в виде А˝ТФ и
восстановленных динуклеотидов НАДФ · Н и НАД · Н. Но они очень слабо проникают через оболочку хлоропластов. Поэто˝му для их переноса из хлоропластов в цитоплазму выработаны с˝пециальные механизмы.
Перенос в цитоплазму макроэргических связей АТФ осущест˝в-
ляется в результате взаимных превращений фосфоглицерин˝овой кислоты и фосфодиоксиацетона, при этом также происходит перенос восстановительного потенциала НАД · Н (рис. 9.6). Указанные С3-продукты легко диффундируют через оболочку хлоро-
пластов. В цитоплазме фосфодиоксиацетон изомеризуется в˝ 3-фос-
фоглицериновый альдегид, который далее под действием фер˝мента триозофосфатдегидрогеназы фосфорилируется с образованием 1,3-дифосфоглицериновой кислоты. В ходе реакции также образ˝у-
ются восстановленные динуклеотиды НАД · Н. Затем остато˝к ор-
тофосфорной кислоты с макроэргической связью переносит˝ся на
АДФ, и таким образом осуществляется синтез АТФ. Эту реакци˝ю
катализирует фермент фосфоглицераткиназа.
312

Образовавшаяся в цитоплазме фосфоглицериновая кислота ˝далее диффундирует в хлоропласты, включается там в реакции ˝цик-
ла Кальвина и снова превращается в фосфодиоксиацетон, спо˝соб-
ный вновь перемещаться в цитоплазму и т. д.
Одним из механизмов переноса восстановительного потенц˝иа-
ла НАДФ · Н из хлоропластов в цитоплазму является взаимное превращение яблочной и щавелевоуксусной кислот. Щавелев˝о-
уксусная кислота легко проникает через оболочку хлоропл˝астов
и подвергается в них превращению в яблочную кислоту с участи-
ем НАДФ · Н под действием фермента малатдегидрогеназы. Затем
яблочная кислота диффундирует в цитоплазму и там окисляе˝тся с участием дегидрогеназы в щавелевоуксусную кислоту. При э˝том
происходит образование НАДФ · Н:
После этого щавелевоуксусная кислота вновь диффундируе˝т в хлоропласты и там превращается в яблочную кислоту и т. д. В˝ результате каждого такого превращения в хлоропласте потре˝бляются восстановленные динуклеотиды НАДФ · Н, а в цитоплазме ре˝ге-
нерируются.
Выход продуктов фотосинтеза зависит от условий окружающ˝ей среды, которые могут стимулировать или ингибировать биох˝ими- ческие реакции при фотосинтезе. К важнейшим факторам, неп˝осредственно влияющим на процесс фотосинтеза, относятся ин˝тен-
сивность и состав солнечной радиации, концентрация в атмо˝сфе-
ðå ÑÎ2 è Î2, температура, обеспеченность влагой и элементами питания.
На световую стадию фотосинтеза решающее влияние оказыва˝ет
интенсивность солнечной радиации. Образование продукто˝в фо-
тосинтеза начинается при освещенности, составляющей 1 % п˝олного солнечного света, однако максимальная скорость фото˝синте-
за наблюдается у разных видов растений при освещенности 1˝0—
313
40 тыс. лк, тогда как в ясный солнечный день уровень освещенности может достигать 100 тыс. лк. Чрезмерно высокая интенсив-˝
ность солнечной радиации может повреждать пигментные си˝сте-
мы фотосинтезирующих клеток и ингибировать фотосинтез.
На образование конечных продуктов фотосинтеза существе˝н- ное влияние оказывает состав солнечной радиации. Если в н˝ей
увеличивается доля коротковолнового света (синих лучей)˝, то в
фотосинтезирующих органах уже при коротких экспозициях инициируется включение углерода СО2 в неуглеводные продук-
ты — аланин, аспарагиновую, яблочную, лимонную, глутамино˝-
вую кислоты, серин, а через несколько минут меченый углеро˝д СО2 обнаруживается в значительном количестве в составе бел-
ков. При увеличении доли длинноволнового света (красных л˝у-
чей) меченый углерод СО2 при коротких экспозициях более интенсивно включается в моносахариды и их фосфорнокислые
эфиры, а при 5-минутной и более длительных экспозициях — в˝
состав крахмала.
Кроме того, в опытах отмечено, что скорость фотосинтеза за˝-
метно возрастает при добавлении к красному свету небольшого
количества синего света (до 20 %), который действует в опреде˝- ленной степени как регулятор фотохимических реакций. Уве˝личе-
ние интенсивности синтеза азотистых веществ под действи˝ем си-
него света также связано с его регуляторным действием на ˝ферменты, катализирующие реакции обмена азотистых веществ. Вы-
яснено, что у этих ферментов роль хромофоров, поглощающих˝
синий свет, выполняют флавиновые группировки.
Темновая стадия фотосинтеза зависит от концентрации СО2,
оптимум которой для С3-растений составляет 0,1—0,3 %, тогда как среднее его содержание в атмосфере — 0,03 %. При такой конце˝н- трации СО2 интенсивность фотосинтеза у С3-растений достигает лишь 50 % максимальной. Поэтому для тепличных культур разра˝- батывают специальные технологии выращивания растений в˝ атмосфере с повышенной концентрацией СО2. Как было показано ранее, при пониженных концентрациях СО2 в атмосфере более эффективно осуществляют фотосинтез С4-растения, у которых первичное связывание СО2 катализирует фермент фосфопируваткарбоксилаза, обладающий более высокой карбоксилирующе˝й активностью и не способный инициировать процесс фотодыхан˝ия. У С3-растений интенсивность темновой стадии фотосинтеза
также в значительной степени определяется концентрацие˝й О.
2
При понижении ее в окружающей среде до 3—5 % увеличивается
выход продуктов фотосинтеза за счет ослабления оксигена˝зной реакции, которую катализирует фермент рибулозодифосфат˝кар-
боксилаза в условиях повышенной концентрации О2.
314
Все ферментативные реакции темновой и световой стадий фо˝- тосинтеза зависят от температуры окружающей среды, и при ˝ее
повышении их скорости возрастают как и при любом химическ˝ом
процессе. Однако при температурах свыше 35 °С наблюдаются˝ солнечные ожоги листьев, что приводит к повреждению пигме˝нтных и других фотосинтетических структур, в результате кот˝орого
интенсивность фотосинтеза понижается. Температурный оп˝тимум
Ñ3-растений наблюдается при 25 °С, а у С4-растений повышается до 35 °С.
Обеспеченность растений водой оказывает как прямое, так и˝
косвенное влияние на фотосинтез. Вода непосредственно по˝требляется в реакциях фотосинтеза и является источником кисл˝орода.
Кроме того, она служит основой жидкой физиологической сре˝ды
растительных клеток, включая и хлоропласты, и при ее недос˝татке нарушается функционирование мембранных структур и всле˝д-
ствие усиления вязкости этой среды понижаются скорости ф˝ер-
ментативных реакций. Водный режим растений также влияет н˝а работу устьиц, которые регулируют поступление во внутрен˝нюю
физиологическую среду СО2 из атмосферы. При дефиците и из-
бытке воды устьица закрываются.
Для формирования и функционирования фотосинтетических
структур растений также необходим довольно сложный комп˝лекс
различных химических элементов, которые должны содержат˝ься в фотосинтезирующих клетках в оптимальных концентрациях.˝ Не-
достаток или избыток питательных элементов понижает инт˝ен-
сивность фотосинтеза, оказывая влияние на его световую ил˝и темновую стадию, работу каталитических и мембранных структу˝р
хлоропластов, взаимодействие компонентов электронтранс˝портных цепей и т. д. Роль отдельных химических элементов в про˝цессе фотосинтеза показана в данной главе при изложении конк˝ретных механизмов фотохимических и других реакций.
Следует также отметить воздействие на фотосинтетически˝й аппарат растений различных химических загрязнителей окру˝жающей среды. Так, например, выяснено, что сернистый газ промыш˝- ленных выделений даже в малых концентрациях повреждает л˝истья многих растений, в результате чего понижается выход ф˝отосинтетических продуктов и происходит недобор урожая сельскохозяйственных культур.
Некоторые фотосинтезирующие организмы (одноклеточные
водоросли, некоторые бактерии) образуют в анаэробных усл˝овиях
в качестве основного продукта жизнедеятельности молеку˝лярный
водород, который может использоваться в энергетике стран˝ы как высокоэффективное топливо. В связи с этим проводятся иссл˝едо-
вания по созданию искусственных биологических систем, облада-
315

ющих способностью улавливать солнечную энергию и превра˝щать ее в химическую энергию молекул водорода.
Значительный интерес представляет процесс фотолиза вод˝ы, который катализируют реакционные центры фотосистемы II, л˝о-
кализованные в мембранах хлоропластов растений и водоро˝слей:
2Í2Î ¾¾¾¾¾¾®Ñâåò Î2 + 4Í+ + 4å
Хлоропласты
В фотохимических реакциях электроны и протоны, образую-
щиеся при фотолизе воды, затрачиваются на синтез восстано˝влен-
ных динуклеотидов НАДФ · Н. Однако с помощью гидрогеназной
ферментной системы они могут восстанавливаться до молек˝улярного водорода:
2å +2Í+ ¾¾¾¾¾®Гидрогеназа Í2
Созданная в 1973 г. первая искусственная биологическая сист˝е-
ма для фотосинтетического получения водорода включала и˝золированные хлоропласты высших растений, ферредоксин и ферм˝ент-
ный комплекс гидрогеназы, выделенный из бактерий.
9.1.7. ФОТОСИНТЕЗ У БАКТЕРИЙ
Клетки фотосинтезирующих бактерий отличаются по своей структуре от клеток растений и эукариотических водоросл˝ей. В них нет хлоропластов и пигменты локализованы в цитоплазм˝ати-
ческих мембранах. Главный пигмент большинства фотосинте˝зи-
рующих бактерий — бактериохлорофилл. У таких бактерий отсутствует белково-пигментный комплекс фотосистемы II, поэтом˝у не
происходит фотоокисления воды при фотосинтезе. В качеств˝е до-
норов электронов для реакций фотосинтеза они используют˝ не воду, а другие соединения: H2S, Í2, органические вещества. В свя-
зи с этим у них функционирует только фотосистема I.
Цианобактерии (синезеленые водоросли), как и другие фотосинтезирующие бактерии, не имеют хлоропластов, но главный˝
пигмент у них — хлорофилл, который входит в состав белков˝о- пигментных комплексов как фотосистемы I, так и фотосистем˝ы II. Поэтому у цианобактерий в качестве донора водорода для ф˝о- тосинтетических реакций, как и у растений, используются м˝олекулы воды, в результате фотолиза которых выделяется О2.
316

У галофильных бактерий (Íalobacterium halobium) роль светопоглощающего пигмента выполняет родопсиноподобный бело˝к с
молекулярной массой 26 000, входящий в состав поверхностной
мембраны, окружающей цитоплазму. Этот белок получил назва˝- ние бактериородопсина. В качестве активной группировки в нем содержится ретиналь — альдегидная форма витамина А. Пеп˝тид-
ные цепи бактериородопсина образуют спиралевидные стру˝ктуры,
вытянутые вдоль длинной оси их молекулы, но расположены о˝ни перпендикулярно по отношению к плоскости мембраны. На дол˝ю
бактериородопсина приходится до 75 % общей массы поверхно˝ст-
ной цитоплазматической мембраны.
При поглощении света бактериородопсин инициирует перен˝ос
электронов по электронтранспортной цепи, приводящей в де˝й-
ствие Н+-помпу, способную перемещать протоны через цитоплазматическую мембрану на ее внешнюю поверхность, созда˝вая
трансмембранный электрохимический потенциал. В дальней˝шем
энергия трансмембранного потенциала используется для о˝существления ионного транспорта и синтеза АТФ в клетках галоф˝иль-
ных бактерий, при этом фотолиза воды не происходит.
По способу питания фотосинтезирующие бактерии подразде˝- ляются на две группы — фотоавтотрофные è фотогетеротрофные.
Первые способны использовать в качестве источника углер˝ода для
синтеза органических веществ СО2 воздуха или другой окружающей среды, вторые — различные органические вещества.
К типичным фотоавтотрофным бактериям относятся зеленые˝ и
пурпурные серобактерии. В их клетках найдены ферментные с˝истемы, которые способны с участием восстановленного ферре˝док-
сина катализировать присоединение СО2 к ацетилили сукцинилкоферменту А:
317

Образующиеся в ходе этих реакций продукты могут включать˝ся
в различные биохимические превращения, связанные с обесп˝ече- нием жизнедеятельности рассматриваемых бактерий.
У некоторых пурпурных бактерий при фотосинтезе происход˝ит накопление аспарагиновой кислоты, которая синтезируетс˝я из 3-фосфоглицериновой кислоты, образующейся в результате пр˝исоединения СО2 к рибулозо-1,5-дифосфату. Фосфоглицериновая кислота превращается в фосфоенолпировиноградную кислот˝у, которая, подвергаясь карбоксилированию, образует щавелево˝уксус-
ную кислоту. Затем из щавелевоуксусной кислоты в результа˝те реакции переаминирования может синтезироваться аспарагин˝овая
кислота.
К фотогетеротрофным относятся галобактерии и некоторые˝
разновидности пурпурных несерных бактерий. Под действие˝м света они способны использовать в качестве субстрата пит˝ания для превращения в продукты жизнедеятельности уксусную, п˝ировиноградную кислоты и некоторые другие органические вещ˝ества.
9.2. АССИМИЛЯЦИЯ СО2 ЗА СЧЕТ ИСПОЛЬЗОВАНИЯ ЭНЕРГИИ ХИМИЧЕСКИХ РЕАКЦИЙ
Известна большая группа хемоавтотрофных бактерий, котор˝ые для синтеза органических веществ используют в качестве и˝сточ- ника углерода СО2, а энергию для этих процессов получают в результате окисления неорганических веществ: сероводород˝а, серы, аммиака, нитритов, водорода, восстановленных форм железа ˝и марганца и некоторых других неорганических соединений. С˝интез органических веществ из СО2 за счет энергии, полученной не от солнечных лучей, а с помощью химических реакций, получил н˝а-
звание хемосинтеза. Типичным примером хемоавтотрофных орга-
318

низмов являются бесцветные серобактерии (Òhiobàcillus), которые получают энергию для восстановления СО2 в органические вещества в результате окисления сероводорода или серы:
2H2S + O2 → 2H2O + S2 + G
S2 + 3O2 + 2H2O → 2H2SO4 + G
Высвобождающаяся при окислении указанных веществ энер-
гия используется для синтеза АТФ и других нуклеозидполиф˝осфатов, которые участвуют в синтезе органических веществ, об˝разуемых из СО2. Как было установлено в опытах с меченым углеродом, первичным акцептором СО2 у этих и других хемоавтотроф-
ных бактерий служит рибулозо-1,5-дифосфат и продуктом этой реакции, как и в хлоропластах растений, является 3-фосфогли˝це- риновая кислота.
Нитрофицирующие бактерии в качестве источника энергии и˝с- пользуют восстановленные формы азота в виде аммиака и нит˝ритов, которые они с помощью своих ферментов подвергают оки˝с-
лению кислородом:
2NH3 + 3Î2 → 2HNO2 + 2H2O + G (Nitrosomonàs) 2HNO2 + O2 → 2HNO3 + G (Nitrobàcter)
Эти бактерии играют важную роль в круговороте азота в био˝- сфере и формировании плодородия почвы, так как от их деяте˝ль-
ности зависит процесс нитрификации, обогащающий почву ни˝т- ратной формой азота.
Хемоавтотрофные бактерии, способные окислять восстанов˝- ленные формы железа и марганца, по-видимому, стали источни˝-
ком отложения железных и марганцевых руд. Они также спосо˝бны
использовать энергию химических реакций окисления для с˝инте-
за органических веществ путем ассимиляции СО2.
Частичное усвоение СО2 происходит даже в клетках гетеротрофных организмов. Выявлено несколько типов реакций, в к˝ото-
рых происходит связывание СО2 с органическими субстратами. Под действием соответствующих ферментов карбоксилирова˝нию
подвергаются некоторые кетокислоты, например пировиног˝рад-
ная кислота:
319

Хорошо известный путь гетеротрофного карбоксилирования˝ — присоединение СО2 к фосфоенолпировиноградной кислоте. Такие реакции изучены у растений и автотрофных бактерий. Ро˝ль катализатора в них выполняет фермент фосфопируваткарбоксилаза. Причем фиксация СО2 под действием данного фермента происходит в нефотосинтезирующих клетках.
В клетках растений, микроорганизмов и животных найден фер˝- мент фосфопируваткарбоксикиназа, который катализирует присое-
динение СО2 к фосфоенолпировиноградной кислоте с участием
ГДФ, при этом образуется щавелевоуксусная кислота и ГТФ:
К важным реакциям карбоксилирования следует отнести син˝- тез карбамоилфосфата, катализируемый ферментом карбамоилфосфатсинтетазой. Источником углерода в этой реакции служит
бикарбонат-ион (НСО3–):
Образовавшийся карбамоилфосфат далее используется в си˝нтезе пиримидиновых нуклеотидов, а также в реакциях орнитино˝вого
цикла (см. гл. 11 и 12).
С участием ферментов фосфопируваткарбоксилазы и фосфопируваткарбоксикиназы в клетках корней растений, по-види˝мо- му, осуществляется усвоение СО2, поступившего из почвы. Фос-
фоенолпировиноградная кислота образуется в них в ходе ды˝ха-
тельных реакций. Продукт реакций гетеротрофного карбокс˝или-
рования — щавелевоуксусная кислота может далее включат˝ься в
реакции цикла Кребса и вместе с другими продуктами этого ˝цикла
320
