
Биохимия растений
.pdf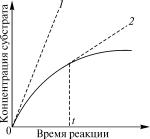
Рис. 8.4. Кинетическая кривая ферментативной реакции:
1 — касательная к кинетической кривой в нулевой момент времени; 2 — касательная к кинетической кривой в точке, соответствующей промежутку времени t
отдельный момент определяется наклоном касательной к ки˝нети-
ческой кривой (рис. 8.4).
Кинетическая кривая — это графическое выражение изменения
концентрации субстрата или продукта реакции в зависимос˝ти от
времени реакции. Чем больше наклон касательной к кинетиче˝с-
кой кривой, тем выше скорость реакции. Самая высокая скоро˝сть
превращения достигается в начальный момент времени, а зат˝ем скорость реакции уменьшается вследствие понижения конц˝ентра-
ции субстрата и одновременного накопления образующихся˝ про-
дуктов, увеличивающих скорость обратной реакции.
Исходя из указанных особенностей прохождения ферментат˝ив-
ной реакции, активность ферментов рекомендуется определ˝ять по начальной скорости реакции и за возможно короткий промеж˝уток
времени, чтобы получить практически линейную кинетическ˝ую
кривую.
По рекомендации Международного биохимического союза за˝
единицу каталитической активности фермента принят катал
(êàò). Один катал — это каталитическая активность, способная˝ катализировать превращение 1 моля субстрата за 1 с при опт˝и- мальных условиях и в заданной системе определения активн˝ости.
Очень часто для выражения активности ферментов использу˝ют так-
же производные от катала единицы: микрокатал (мккат) = 10–6 кат, нанокатал (нкат) = 10–9 кат, пикокатал (пкат) = 10–12 êàò.
В каталах и производных от него единицах измеряют общую активность фермента, которая зависит как от каталитическ˝их
свойств ферментного белка, так и количества фермента, уча˝ствую-
щего в реакции.
Для характеристики каталитической активности чистых фе˝р- ментных препаратов используют показатель удельная активность,
который выражается в каталах в расчете на 1 кг ферментного˝ пре-
парата (кат · кг–1) или в других производных от катала и килограм-
ма единицах. При определении удельной активности в тканях˝ жи-
вого организма данный показатель выражает содержание фе˝рмента в биологическом источнике.
201
Каталитическую активность фермента наиболее точно можн˝о выразить с помощью показателя, называемого молярной активностью, которая измеряется в каталах в расчете на 1 моль фермента (кат · мольô–1). Она показывает, какое число молекул субстрата
превращается за 1 с одной молекулой фермента. В отдельных˝ слу- чаях расчет активности фермента проводится с учетом числ˝а ак-
тивных центров в его молекуле и такой показатель называют˝числом оборотов èëè молекулярной активностью, он выражается в ка-
талах в расчете на 1 моль активных центров фермента.
Для многих ферментов показатель молярной активности име˝ет
очень высокие значения (до 106), поэтому скорости реакций, ката-
лизируемых ферментами, в десятки и даже сотни тысяч раз пр˝евышают скорости реакций, происходящих без участия ферменто˝в.
Вследствие того что в активном центре происходит активир˝ование
и сближение молекул реагирующих субстратов, ферментатив˝ные
реакции протекают с высокой скоростью даже при низкой кон˝-
центрации реагирующих веществ в физиологической среде. Так, например, фермент каталаза, участвующий в разложении˝ пе-
роксида водорода на воду и кислород, способен катализиров˝ать
превращение 2 · 105 молекул субстрата за 1 с в расчете на активный
центр фермента.
Âсвязи с тем что активный центр фермента должен структур˝но соответствовать субстрату, изменение его конформации мо˝жет
снижать каталитические свойства ферментной молекулы. По˝это-
му любые воздействия на фермент, вызывающие изменение
структуры активного центра, влияют на каталитическую спо˝соб-
ность фермента, тогда как изменение конформации молекулы˝, не затрагивающее активный центр, меньше влияет на каталитич˝еские свойства фермента.
Âфизиологической среде, в которой находятся молекулы ферментов, могут присутствовать химические компоненты, вызывающие инактивацию или даже разрушение молекул фермен˝- та. Поэтому каждый фермент может активно функционировать˝
лишь определенное время, после чего его молекулы становят˝ся
неактивными. Продолжительность жизни фермента определя˝ется его ролью в обмене веществ и генотипом организма. Для ха˝- рактеристики продолжительности жизни ферментов использ˝уют показатель — период полужизни ферментов, который для расти-
тельных объектов варьирует от нескольких часов до нескол˝ьких
суток.
Âсвязи с инактивацией и распадом ферментов в клетках жив˝о- го организма постоянно происходит процесс синтеза новых˝ моле-
кул ферментов. Такая особенность ферментов имеет важное био-
логическое значение для регуляции их синтеза и хода ферме˝нта-
тивных превращений. Если бы ферменты не инактивировались˝, то
202
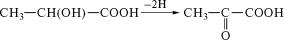
однажды синтезированный фермент длительное время не пре˝кращал бы своей деятельности и реакцию, катализируемую этим ˝ферментом, было бы трудно регулировать в соответствии с потр˝ебностями организма.
8.4. ИЗОФЕРМЕНТЫ
Большинство ферментов представлены в клетках организма˝ в
виде множественных молекулярных форм, называемых изофер˝- ментами или изоэнзимами. Изоферменты — это сходные по струк-
туре белковые молекулы, способные катализировать одну и т˝у же
биохимическую реакцию, но различающиеся по первичной стр˝ук-
туре входящих в их состав полипептидов. Они имеют одинако˝вую
структуру каталитического центра, вследствие чего облад˝ают одним типом субстратной специфичности. Изоферменты одного˝ и
того же фермента отличаются оптимумами рН, температуры, д˝ру-
гих условий внешней среды, их молярной активностью, но все˝
они катализируют одну и ту же реакцию. Когда из клеток орга˝низ-
ма выделяют какой-либо фермент и определяют его активност˝ь, всегда имеют дело с его конкретными изоферментами.
Молекулы ферментов чаще всего представляют собой олигом˝е-
ры, построенные из двух или нескольких полипептидов, кото˝рые
в той или иной степени различаются первичными структурам˝и, но
имеют однотипную третичную структуру и поэтому при взаим˝о- действии образуют функционально родственные белки. Как б˝ыло
показано ранее, различающиеся первичными структурами по˝ли-
пептиды в составе олигомерных молекул кодируются разным˝и ге-
нами, поэтому природа и набор изоферментов определяются г˝е- нотипом организма.
Впервые механизм образования изоферментов был выяснен при изучении множественных молекулярных форм фермента л˝ак-
татдегидрогеназы, катализирующего в клетках человека и ж˝ивот-
ных превращение молочной кислоты в пировиноградную:
В ходе исследований были выделены кристаллические препа˝- раты лактатдегидрогеназы из клеток печени, сердечной мыш˝цы и
скелетных мышц и подвергнуты разделению методом электро˝фореза в щелочной буферной системе (рН 8,8). В таких условиях мо˝-
лекулы фермента имеют отрицательный заряд и в зависимост˝и от величины заряда проявляют разную подвижность по направл˝ению
к аноду. В процессе электрофоретического разделения было˝ выде-
лено пять белковых фракций, каждая из которых представлял˝а со-
203
бой тетрамерные молекулы с молекулярной массой около 140 тыс., образованные из различных комбинаций двух типов полипептидов, обозначаемых Í è Ì. Полипептиды Í наиболее активно синтезируются в сердечной мышце и печени и содержат˝ в
своем составе больше остатков моноаминодикарбоновых ки˝слот. Полипептиды второго типа (Ì) синтезируются преимущественно
в скелетных мышцах и характеризуются меньшим содержание˝м дикарбоновых аминокислот. С участием указанных типов пол˝и-
пептидов образуется пять разновидностей ферментных мол˝екул,
являющихся изоферментами лактатдегидрогеназы: Í4, Í3Ì, Í2Ì2,
ÍÌ3, Ì4. Каждая молекула изофермента, как тетрамер, состоит из
четырех полипептидов, которые могут быть идентичными (Í4 è Ì4) или разными (Í3Ì, Í2Ì2, ÍÌ3). Количественное содержание
каждого изофермента в данной ткани зависит от концентрац˝ии в
ней полипептидов Í è Ì.
Вследствие того что полипептиды Í содержат в своем составе
больше остатков дикарбоновых аминокислот, тетрамер Í4 при рН 8,8 среды имеет наибольший отрицательный заряд, поэтому
быстрее движется к аноду в процессе электрофореза (рис. 8.5).
Тетрамер Ì4 характеризуется наименьшей подвижностью к
аноду, так как его молекулы построены из полипептидов с ме˝нь-
шим содержанием дикарбоновых аминокислот. Другие изофер˝- менты распределяются при электрофорезе между фракциями˝Í4 è
Ì4 в зависимости от числа полипептидов Í è Ì в их молекулах.
Из примера с лактатдегидрогеназой следует, что если молек˝ула
фермента — тетрамер, образованный из двух типов полипеп˝тидов,
то возникают пять изоферментов. Но если молекулы тетрамер˝ного фермента формируются из трех типов полипептидов, наприме˝рÀ, Á è Â, то возникают следующие комбинации полипептидов в мо-
|
лекуле: À4, Á4, Â4, À3Á, À3Â, À2Á2, À2Â2, |
|||
|
À2ÁÂ, ÀÁ3, ÀÂ3, ÀÁ2Â, |
ÀÁÂ2, Á3Â, |
Â3Á, |
|
|
Á2Â2. Из этого примера видно, что набор |
|||
|
изоферментов заметно |
возрастает |
ïðè |
|
|
увеличении числа разных полипептидов, |
|||
|
из которых строятся молекулы белка-фер- |
|||
|
мента. Набор изоферментов также увели- |
|||
|
чивается при возрастании степени олиго- |
|||
|
мерности молекулы фермента. Так, у |
|||
|
лактатдегидрогеназы из двух разных по- |
|||
|
липептидов строятся тетрамерные моле- |
|||
|
кулы и возникают пять изоферментов, а |
|||
Рис. 8.5. Электрофореграм- |
у гексамерного белка из двух типов поли- |
|||
ма изоферментов лактатде- |
пептидов образуются уже семь изофер- |
|||
гидрогеназы при разделении |
ментов, у октамерного белка — девять |
|||
в щелочной буферной сис- |
||||
è ò. ä. |
|
|
||
òåìå (ðÍ 8,8) |
|
|
||
204
Таким образом, общий набор изоферментов данного ферментного белка определяется степенью олигомерности его моле˝кулы и числом разных полипептидов, из которых образуются молеку˝лы белка. Следует отметить, что к изоферментам не относятся м˝оле-
кулы фермента, измененные в результате повреждения струк˝туры белка или модификации его молекул путем присоединения ак˝тив-
ных группировок (так называемая посттрансляционная моди˝фикация белков).
Поскольку изоферменты — это определенный набор белковы˝х
молекул, способных катализировать превращение одного и т˝ого
же субстрата, для их выявления используют методы разделен˝ия,
принятые для белков, с последующим определением каталити˝ческой активности. Наиболее часто для разделения изофермент˝ов ис-
пользуют метод электрофореза в полиакриламидном геле, ко˝то-
рый по сравнению с другими методами имеет наиболее высоку˝ю
разрешающую способность. При разделении этим методом мож˝но
выявить изоферменты, различающиеся по суммарному заряду˝ молекулы, который определяется содержанием в белке остатко˝в мо-
ноаминодикарбоновых кислот. Если же в составе организма и˝ме-
ются генетические варианты молекул фермента, у которых ра˝зли-
чия в аминокислотном составе не приводят к изменению заря˝да
молекулы, то для их разделения используют модификации эле˝ктрофореза, основанные на других принципах, например изоэле˝кт-
рофокусирование белков.
Особенно большое разнообразие множественных молекуляр-˝
ных форм наблюдается у растительных ферментов. Практически
каждый фермент представлен в растении в виде набора изофе˝р- ментов, каждый из которых проявляет каталитическую актив˝ность в строго определенных условиях, зависящих от параметров в˝нут-
ренней физиологической среды, что позволяет организму об˝еспе- чивать специфичность обмена веществ в данном органе, ткан˝и или внутриклеточном компартменте (межмембранном отсеке˝). Так, например, в листьях и корнях растений разная физиолог˝ичес-
кая среда, но в них может проходить одна и та же реакция за с˝чет
того, что ее катализируют разные изоферменты данного ферм˝ента. При изучении у растений картофеля изоферментов фосфорил˝азы, катализирующей расщепление крахмала, было выявлено, что в˝се органы картофеля (корни, листья, клубни) имеют специфическ˝ий
набор изоферментов этого фермента, который определяли эл˝ект-
рофорезом в кислой буферной системе (рис. 8.6). При таких усл˝о- виях разделения ферментные белки имеют положительный за˝ряд, обусловленный наличием в белках диаминомонокарбоновых ˝кис-
лот, вследствие чего белки проявляют подвижность к катоду˝.
В процессе роста и развития растений постоянно изменяютс˝я
внутренняя физиологическая среда и внешние условия, в соо˝твет-
205

Рис. 8.6. Электрофореграммы изоферментов фосфорилазы картофеля:
1 — клубни; 2 — листья; 3 — корни
ствии с этим изменяется и набор изоферментов каждого фермента. Наиболее четко проявляют-
ся качественные и количественные изменения
состава изоферментов при созревании и прорастании семян.
На рисунке 8.7 показаны электрофореграм-
мы изоферментов α-амилазы созревающего,
зрелого и прорастающего зерна пшеницы, раз-
личающихся по их подвижности к аноду. При сравнении элект˝рофореграмм видно, что в созревающем зерне пшеницы амилолит˝и-
ческой активностью обладают пять изоферментов с низкой п˝од-
вижностью к аноду, в прорастающем зерне также пять, но уже
других по электрофоретической подвижности изоферментов˝.
Вследствие того что при созревании зерна происходит связ˝ывание амилаз белковыми ингибиторами в неактивный комплекс, в по˝л-
ностью созревшем зерне при благоприятных погодных услов˝иях
выявляется слабая амилолитическая активность только од˝ного
изофермента α-амилазы. Однако в зерновках, сформировавшихся
при влажной погоде, активность большинства изоферментов˝α-ами- лаз, выявленных в созревающем зерне, сохраняется.
Специфичность обмена веществ у больных и здоровых расте-
ний также осуществляется за счет синтеза определенного н˝абора
изоферментов, обеспечивающих ход жизненно важных биохим˝и-
ческих реакций. Как установлено в опытах по изучению особ˝ен-
ностей функционирования ферментных систем при различны˝х заболеваниях большого набора растений, в листьях и других о˝рганах больных растений очень часто возрастает число изоформ ок˝исли- тельно-восстановительных ферментов. Полу-
ченные данные свидетельствуют о том, что при
анализе сведений об изоферментах необходимо учитывать возраст и физиологическое состояние растений, а также обязательно знать, из какого органа, ткани или внутриклеточного ком-
партмента они выделены.
Рис. 8.7. Электрофореграммы изоферментов α-амилазы
пшеницы:
1 — созревающее зерно в фазе молочно-восковой спелости; 2 — зрелое зерно, сформировавшееся при сухой погоде; 3 — зрелое зерно, сформировавшееся при влажной погоде; 4 — зерно трехсуточных проростков. Стрелкой показано направление движения моле˝кул изоферментов при электрофорезе, справа дана шкала относи˝тельной электрофоретической подвижности белковых компонент˝ов
206
Наличие в клетках организма множественных молекулярных˝ форм одного и того же фермента, проявляющих каталитическу˝ю активность при разных физиологических условиях, позволя˝ет организму осуществлять с необходимой интенсивностью би˝охи-
мические процессы при изменении условий внешней среды.
При изменении внешних условий они становятся неблагопри˝-
ятными для проявления каталитической активности опреде˝ленных изоферментов, но биохимическая реакция не прекращает˝ся,
так как вступают в действие другие изоферменты, которые с˝по-
собны катализировать данное превращение в изменившихся˝ усло-
виях. Если появляется новый изофермент, то он расширяет ди˝апа-
зон выживаемости организма. Чем больше набор изоферменто˝в, тем шире диапазон их действия и лабильнее адаптация орган˝изма
к неблагоприятным факторам внешней среды.
Так, у гетерозисных растений выявлены «гибридные» изофер-
менты, которых нет у родительских генотипов, именно с появ˝ле-
нием этих новых изоферментов связывают увеличение мощно˝сти и жизнеспособности гетерозисных растений, что в конечном˝ ито-
ге приводит к повышению их продуктивности.
Изучение ферментных систем растений показывает, что спец˝и-
фичность обмена веществ у разных генотипов обеспечивает˝ся ха-
рактерным для каждого генотипа набором изоферментов. Чем˝ ближе генотипы растений в систематическом отношении, тем˝
меньше различается у них изоферментный состав ферментов˝. В
связи с этим изоферментный анализ довольно успешно приме˝ня-
ется для уточнения систематики живых организмов, выявлен˝ия
филогенетического родства между видами и сортами растен˝ий, а также проверки генетической чистоты или, наоборот, генети˝ческого разнообразия растительной популяции.
8.5.ИЗМЕНЕНИЕ АКТИВНОСТИ ФЕРМЕНТОВ
ÂЗАВИСИМОСТИ ОТ УСЛОВИЙ СРЕДЫ
На каталитические свойства ферментных белков влияют мно˝-
гие химические и физические факторы, способные воздейств˝овать
на структуру активного центра, скорость образования и рас˝пада фермент-субстратного комплекса, состояние ионизации мол˝екул субстрата и определенных группировок фермента (температ˝ура, рН и ионный состав среды, присутствие активаторов и ингиб˝иторов, окислительно-восстановительный потенциал среды, кон˝цен-
трация субстрата и фермента, влияние внешнего электричес˝кого
поля и др.). Действие этих факторов оказывается возможным б˝ла-
годаря тому, что ферменты являются белками, которые довол˝ьно
легко перестраивают пространственную структуру молекул˝ы под
207
влиянием условий внешней среды и, следовательно, проявляю˝т высокую лабильность в изменении своих физико-химических˝
свойств. При оценке влияния факторов внешней среды на кат˝али-
тические свойства ферментов следует также учитывать, что˝ в каждом конкретном случае определяется активность того набо˝ра изоферментов, которые определяют специфичность обмена веще˝ств в
исследуемом биологическом объекте.
Влияние температуры. Ферментативные реакции могут происходить в интервале температур от 0 °С (точка замерзания воды) до
70...80 °С (тепловая денатурация белков высших организмов). Пр˝и
повышении температуры увеличиваются скорости химически˝х реакций, в том числе и скорость образования фермент-субстра˝тных
комплексов, поэтому активность ферментов возрастает, вслед-
ствие чего происходит интенсификация процессов жизнеде˝ятельности растений.
Ускорение реакций под воздействием повышенной температ˝у-
ры обусловлено тем, что снижается энергия активации как с˝убстрата, так и фермента. В интервале температур 0...40 °С повыше˝-
ние температуры на 10 °С увеличивает скорость ферментативных
реакций в 1,4...2 раза. Наиболее высокая активность ферментов наблюдается при температурах 40...50 °С. При температурах свы˝ше
50 °С активность ферментов понижается, так как начинается˝ про-
цесс тепловой денатурации ферментных белков, вызывающий˝ необратимое изменение четвертичной, третичной и вторичн˝ой
структур белковых молекул. Полная денатурация растительных
белков в растворе, как указывалось ранее, происходит при т˝емпературах 70...80 °С.
Однако в негидратированном (сухом) состоянии белки спосо˝б- ны сохранять нативные свойства и при более высокой темпер˝атуре, что используется в технологиях быстрого высушивания з˝ерна и семян без снижения их всхожести. Не происходит необратимо˝й инактивации ферментов также и при замораживании растите˝льных тканей. При понижении температуры ниже точки замерзан˝ия физиологической среды прекращается действие ферментов,˝ однако при повышении температуры их каталитическая активнос˝ть восстанавливается.
Влияние рН среды. Каждая молекулярная форма фермента (изофермент) проявляет каталитическую активность в узко˝м интервале рН среды, поскольку от концентрации водородных ио˝нов
зависит состояние ионизации молекулы субстрата и группи˝ровок
в активном центре ферментного белка, которое обеспечивае˝т ка-
талитическое действие фермента. Кроме того, концентрация˝ ионов водорода влияет на конформацию активного центра. По˝-
этому даже небольшой сдвиг реакции среды от оптимального зна-
208

чения изменяет заряд кислотных и основных групп фермента и субстрата
и конформацию активного центра
фермента, вследствие чего резко понижается каталитическая активность молекулы фермента. Однако фермен-
ты в клетках растений представлены
наборами изоферментов, каждый из которых проявляет каталитическую
активность при разных значениях рН
среды, поэтому в результате действия всего набора изоферментов обеспечи-
вается ход катализируемой реакции в
широком диапазоне изменения рН
Рис. 8.8. Каталитическая активность аспартатдегидрогеназы бактероидов из клубеньков желтого люпина в зависимости от рН
среды. Зависимость активности фермента от рН среды показа˝на на рисунке 8.8.
Влияние концентрации фермента и субстрата. Если в физиоло-
гической среде содержится много субстрата и мало фермент˝ного белка, то скорость превращения субстрата в продукты реакц˝ии
будет низкой, так как каждая молекула фермента способна к˝ата-
лизировать превращение определенного количества субстр˝ата в единицу времени. При увеличении числа ферментных молекул
(т. е. концентрации фермента) в среде скорость ферментати˝вной
реакции будет возрастать до тех пор, пока достаточно субс˝трата для полной реализации молярной активности фермента. При
дальнейшем увеличении концентрации фермента скорость р˝еак-
ции уже не возрастает. Следовательно, скорость ферментати˝вной реакции пропорциональна количеству фермента в среде тол˝ько при высокой концентрации субстрата.
Скорость реакции, катализируемой ферментом, зависит такж˝е от концентрации субстрата в физиологической среде при ус˝ловии, что количество фермента остается неизменным. Если в среде˝ находится определенное количество фермента и в нее добавля˝ется субстрат, то вначале скорость ферментативной реакции буд˝ет возрастать пропорционально увеличению концентрации субстрата. Однако в дальнейшем по мере увеличения концентрации с˝убстрата темпы нарастания скорости реакции замедляются, и при определенном количестве субстрата в среде скорость реак˝ции достигает максимального уровня, при котором полностью реал˝изу-
ется молярная активность фермента (рис. 8.9). С этого момента˝ скорость реакции уже не будет возрастать при увеличении к˝оли-
чества субстрата в среде, так как лимитирующим фактором, опре-
деляющим дальнейший ход реакции, становится концентраци˝я фермента.
209
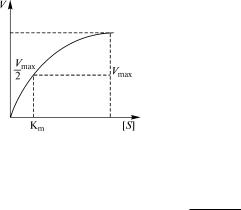
Рис. 8.9. Зависимость скорости ферментативной реакции от концентрации субстрата:
V — скорость ферментативной реакции; [S] — концентрация субстрата; Vmax — максимальная скорость ферментативной реакции при данном количестве фермента; Кm — константа Михаэлиса фермента
Зависимость скорости ферментативной реакции (V) от концент-
рации субстрата может быть выражена уравнением
[S ]
V+ [S ],=Vmax Km
ãäå Vmax — максимальная скорость реакции при высокой концентра˝ции субстрата, когда в каждый момент времени все молекулы фермента наход˝ятся в соединении с субстратом (насыщение фермента субстратом); [S] — концентрация субстрата; Km — константа Михаэлиса, названная именем Л. Михаэлиса, ко˝торый внес большой вклад в разработку теории ферментативной кинетики.
Константа Михаэлиса выражает сродство фермента к субстр˝ату и служит важной характеристикой ферментного белка. Чем ме˝нь-
ше константа Михаэлиса, тем выше молярная активность ферм˝ен-
та и тем интенсивнее происходит ферментативный катализ. И˝з приведенного выше уравнения можно определить значение к˝он-
станты Михаэлиса:
Km =[S]æ |
Vmax |
– 1 |
ö |
; |
ïðè V = |
Vmax |
Km = [S]. |
÷ |
|
||||||
|
|
||||||
ç |
V |
|
2 |
|
|||
è |
ø |
|
|
||||
Следовательно, константа Михаэлиса численно равна конце˝нт-
рации субстрата, при которой скорость реакции, катализиру˝емой
ферментом, достигает 1/2 максимальной.
Для определения константы Михаэлиса экспериментальным путем с использованием чистого фермента находят скорост˝ь катализируемой реакции, включая максимальную при разных знач˝е- ниях концентрации субстрата. Затем изменение скорости фе˝рментативной реакции в зависимости от концентрации субстрат˝а выра-
жают в виде графика, как показано на рисунке 8.9. Если на этом
графике отметить скорость, равную половине максимальной˝, и опустить перпендикуляр на ось абсцисс, то он укажет конце˝нтрацию субстрата, численно равную константе Михаэлиса.
Активаторы ферментов. Для поддержания молекулы фермента в активном состоянии необходимо наличие в среде определен˝ных
210
