
Биохимия растений
.pdfполипептидов с известными молекулярными массами и опред˝еляют их электрофоретическую подвижность, а затем с помощью ˝специальных расчетов или графически производят оценку моле˝кулярной массы исследуемых полипептидов.
5.4.СВОЙСТВА И МЕТОДЫ ИЗУЧЕНИЯ БЕЛКОВ
Âзависимости от состава аминокислотных группировок бел˝ковые молекулы, находясь в растворенном состоянии, могут вс˝ту-
пать в различные химические реакции, с помощью которых мо˝ж-
но проводить качественные тесты на наличие тех или иных г˝руп-
пировок в молекуле белка, а также качественные реакции дл˝я об-
наружения белков. Так, например, при взаимодействии белко˝в с крепкой азотной кислотой образуется желтое окрашивание˝, кото-
рое свидетельствует о наличии радикалов ароматических а˝мино-
кислот. Такая качественная реакция на белки получила назв˝ание
ксантопротеиновой реакции.
При добавлении к щелочному раствору белка небольшого ко-
личества медного купороса происходит образование компл˝екс-
ного соединения катионов меди (Cu2+) с пептидными группи-
ровками белка, окрашивающего раствор в сине-фиолетовый
цвет. Эту реакцию называют биуретовой, так как такое же окра-
шивание с катионами меди дает биурет, имеющий группировку˝ —CО—NН—.
Поскольку аминокислоты обладают оптической активностью˝,
оптические свойства также характерны для пептидов и белк˝ов, од-
нако величина удельного вращения плоскости поляризации˝ света
óбелковой молекулы не является простой суммой удельных в˝ращений аминокислот, образующих данный белок. В полипептида˝х имеются два фактора асимметрии, влияющих на оптические св˝ой-
ства, — наличие асимметрических атомов углерода в радик˝алах
аминокислот и особенности пространственного строения в˝торич-
ной и третичной структуры молекулы. Так, если в молекуле пр˝и- сутствует много α-спиральных структур, то возрастает угол правого вращения плоскости поляризации света.
Âмолекулах белков в составе аминокислотных радикалов им˝е-
ются аминные и карбоксильные группы, которые, как и в амино˝- кислотах, в зависимости от реакции среды могут образовыва˝ть анионы или катионы, способные двигаться в электрическом п˝оле
соответственно к аноду или катоду. При определенном значе˝нии pH, индивидуальном для каждого типа белков, устанавливаетс˝я равенство положительных и отрицательных зарядов и сумма˝рный
заряд молекулы становится равным нулю. Такое состояние бе˝лко-
вой молекулы называют изоэлектрической точкой.
101
При pH физиологической среды ниже pH изоэлектрической точки белка белковая молекула заряжена положительно за с˝чет заряда аминных групп, присоединяющих катионы водорода. Если˝ же pH среды выше pH изоэлектрической точки белка, белковая
молекула заряжена отрицательно вследствие диссоциации ˝карбоксильных групп. И в том и в другом случае все молекулы данно˝го
белка имеют одинаковый по величине заряд, который обуслов˝ливает взаимное отталкивание молекул, вследствие чего они л˝егче
удерживаются в растворе.
В изоэлектрической точке между молекулами белка нет элек˝т-
ростатического отталкивания, и они легко переходят в осад˝ок.
Вследствие того что белки в изоэлектрической точке имеют˝ минимальную растворимость, для их выделения применяют специа˝ль-
ный прием, называемый изоэлектрическим осаждением.
Значение pH изоэлектрической точки белков зависит от их
аминокислотного состава, определяющего число свободных˝
аминных и карбоксильных групп в молекуле. При увеличении ˝в белке содержания остатков дикарбоновых кислот pH изоэлект˝-
рической точки смещается в кислую сторону, а при возраста˝нии
количества остатков диаминомонокарбоновых кислот — в щ˝е-
лочную сторону.
Растворимость белков зависит от степени гидратации белк˝овой молекулы, которая определяется наличием на ее поверхност˝и гид-
рофильных группировок, способных образовывать с молекул˝ами
воды водородные связи или вступать в электростатические взаи-
модействия. В результате таких взаимодействий вокруг белковой
молекулы формируется гидратная оболочка, включающая несколько слоев молекул воды и удерживающая белковую молек˝улу в растворенном состоянии. Если путем воздействия каких-ли˝бо
факторов удалить гидратную оболочку вокруг белковых мол˝екул, то они вступают в межмолекулярные взаимодействия между с˝о- бой, образуя более крупные агрегаты, способные осаждаться˝ из раствора.
При насыщении белкового раствора некоторыми органическ˝и-
ми растворителями (спирт, ацетон) или солями, которые связ˝ывают молекулы воды сильнее, чем белки, происходит обезвожив˝ание белковых молекул, вследствие чего они в результате агрега˝ции образуют более крупные частицы и выпадают в осадок. Для пред˝отв-
ращения денатурации осаждение белков органическими рас˝твори-
телями проводят при пониженной температуре (–5 °C). Выделе˝н- ные таким способом белки после удаления органического ра˝створителя снова можно растворить в воде или слабом растворе соли,
при этом белки сохраняют свои нативные свойства.
Процесс осаждения белков в насыщенных растворах нейт-
ральных солей называют высаливанием. Его очень часто приме-
102
няют для выделения и очистки ферментов и других белковых препаратов.
Сухие препараты белков или сухая растительная масса, соде˝р-
жащая белки, способны впитывать воду, при этом происходит˝ увеличение объема и может создаваться очень сильное давл˝ение. Такие свойства белков называют набуханием. Процессы набухания
белков играют важную роль при прорастании семян и учитыва˝ют-
ся при разработке технологий хранения и переработки раст˝ительной продукции (набухание белков при созревании теста, при˝го-
товлении кондитерских изделий; набухание зерна при его за˝мачи-
вании и др.).
Белковые молекулы вследствие крупных размеров не способ˝-
ны диффундировать через биологические мембраны, через ко˝то-
рые свободно проходят молекулы воды и низкомолекулярных˝ незаряженных веществ. Благодаря этому свойству белков во˝з-
можна локализация ферментов и катализируемых ими реакци˝й в
замкнутых межмембранных отсеках растительной клетки — ˝компартментах.
Для очистки белков от низкомолекулярных примесей исполь˝-
зуют целлофановые мембраны. Из белкового раствора, помеще˝н- ного в пространство, ограниченное целлофановой мембрано˝й,
низкомолекулярные вещества под влиянием градиента конц˝ент-
рации легко диффундируют во внешний омывающий раствор, а для белковых молекул целлофановая мембрана непроницаем˝а. Та-
кой процесс очистки белков называют диализом.
Свойства белков учитывают при выборе методов их выделени˝я. Главная цель выделения белков — предотвращение их денатура-
ции и сохранение нативной структуры. Исходя из этих требо˝ваний подбирают растворители, защитные добавки, а также спо˝собы и условия экстракции, осаждения и очистки белков. Кроме то˝го, необходимо учитывать, что в любом растительном материале˝ поч- ти всегда содержатся протеолитические ферменты, катализ˝ирующие гидролиз белков, который приводит к их деградации. В це˝лях защиты от протеолиза необходимо при выделении белков при˝менять специальные приемы удаления протеолитических ферм˝ентов или добавлять в белковый раствор ингибиторы протеаз.
Для подавления жизнедеятельности микроорганизмов, кото˝- рые также могут стать источником протеолитических ферме˝нтов или причиной денатурации белковых молекул, все этапы выде˝ле-
ния и очистки белков проводятся при пониженной температу˝ре
(чаще всего 4 °C), а в отдельных случаях применяют и антисепт˝и-
ки. При использовании органических растворителей во избе˝жание денатурации белков температуру понижают до –5 °C, а в услов˝иях
вакуума применяют и более низкие температуры.
103
Вследствие того что в сильнокислой или сильнощелочной ср˝е- де белковые молекулы подвергаются денатурации, для выдел˝ения белков применяют растворители или буферные системы с pH ср˝е- ды, близким к нейтральной или равным pH изоэлектрической
точки выделяемых белков.
Выделению белков предшествует процесс измельчения раст˝и-
тельного материала и его гомогенизации, затем проводят эк˝стракцию белков соответствующим растворителем или буферным р˝а-
створом, который должен в максимальной степени обеспечив˝ать
избирательность растворения. При выделении белков, прочн˝о
связанных с клеточными структурами, применяют специальн˝ые
детергенты, способные разрушать связи выделяемых белков˝ с другими органическими компонентами.
Из полученного экстракта белки осаждают насыщенными ра-
створами солей, спиртом, ацетоном или в виде нерастворимы˝х
продуктов. Если необходимо, проводят изоэлектрическое ос˝ажде-
ние. Полученные после осаждения белковые препараты очища˝ют путем промывания и переосаждения, а затем высушивают. Для˝
сушки белковых препаратов применяют специальную методи˝ку
высушивания, называемую лиофилизацией, которая обеспечивает
сохранение нативных свойств белковых молекул. В процессе˝ лио-
фильного высушивания вода удаляется из белкового препар˝ата или растительной массы в замороженном состоянии при созд˝ании
глубокого вакуума.
Для достижения особой чистоты выделяемых из растительны˝х
тканей белков применяют специальные методы очистки (диал˝из,
иммуносорбцию, ультрафильтрацию, различные виды хромато˝- графии), которые позволяют получать белки в кристалличес˝ком состоянии. Современными методами установлено, что белков˝ые
кристаллы практически не содержат примесей других вещес˝тв, но в то же время и не являются индивидуальными белками, так ка˝к состоят из смеси близких по свойствам белковых молекул, о˝бразующих кристаллы одинаковой формы.
Для выделения индивидуальных белков или конкретных белк˝о-
вых фракций применяют большой набор методов, основанных н˝а использовании различий их физико-химических свойств. В за˝висимости от размеров и форм молекул белки разделяют методами гельхроматографии, ультрацентрифугирования и электрофо˝реза в
гелях. На различиях зарядов белковых молекул основано их ˝разде-
ление методами ионообменной хроматографии, электрофоре˝за и изоэлектрофокусирования.
При разделении белков методом гельхроматографии белков˝ый
раствор пропускают через колонку, заполненную гидратиро˝ван-
ным гелем, который состоит из пористых гранул, образованн˝ых из
высокомолекулярного полисахарида декстрана и его произ˝водных
104
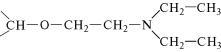
(сефадекс, сефароза), полиакриламида (биогели) или другого˝ полимерного материала. В процессе протекания белкового рас˝твора через гель молекулы небольших размеров способны проника˝ть в мелкие поры отдельных гранул геля и задерживаться в нем, а˝ бо-
лее крупные молекулы с потоком движущегося раствора прох˝одят
âпоры большего размера между гранулами геля и поэтому бы˝ст-
рее выходят из колонки.
Методы ультрацентрифугирования и электрофореза уже рас-
сматривались ранее (см. с. 98—101). Метод изоэлектрофокусиро-
вания представляет собой разновидность электрофореза в˝ геле, в
котором создается градиент pH в направлении движения заря˝жен-
ных частиц. Как только в процессе электрофореза белки дос˝тигают участка геля с pH, равным pH изоэлектрической точки белка,
белковые молекулы становятся электронейтральными и пре˝кра-
щают движение в электрическом поле. Этим методом удается раз-
делять белковые молекулы, изоэлектрические точки которы˝х раз-
личаются на сотые доли pH.
Для разделения белков методом ионообменной хроматограф˝ии
âкачестве катионитов чаще всего используют производные˝ цел-
люлозы и сефадекса, имеющие присоединенные к ним карбокси˝-
метильные группировки =CH—O—CH2—COOH. В качестве анио-
нитов обычно используют производные целлюлозы, сефадекс˝а и сефарозы с присоединенными к ним диэтиламиноэтильными
группировками:
После связывания белков катионитом или анионитом провод˝ят их десорбцию путем элюирования раствором с возрастающей˝ ионной силой. При увеличении концентрации соли в протекающем˝
через колонку растворе вначале подвергаются десорбции б˝елки,
имеющие мало заряженных группировок и поэтому слабее свя˝занные с ионитом, затем происходит элюирование более прочно ˝связанных белков.
С использованием в качестве ионообменников более прочны˝х
органических полимеров разработаны методы быстрой жидк˝о-
стной хроматографии белков (система FPLC), позволяющие проводить разделение белковых молекул при высокой скорости˝ протекания растворов через колонки под давлением 2 МПа.
Для разделения белков, различающихся гидрофобными свой-
ствами, используют метод гидрофобной хроматографии. В это˝м
случае для связывания белков применяют сорбенты с присое˝ди-
105
ненными гидрофобными радикалами (например, фенилсефароз˝а) и высокую концентрацию соли в растворе. В дальнейшем путем постепенного понижения концентрации соли в элюирующем р˝астворе проводят десорбцию белков по степени их гидрофобно˝сти.
Путем присоединения гидрофобных углеводородных радикал˝ов к молекулам пористого кремнезема получены гидрофобные со˝рбен-
ты с повышенной механической прочностью, которые использ˝уют для высокоэффективной жидкостной хроматографии белков ˝при
высоком давлении (система HPLC).
Особенно высокой эффективностью отличаются методы разд˝е-
ления белков, основанные на строго избирательном связыва˝нии
белковых молекул биоспецифическим сорбентом, частицы ко˝торого по своей пространственной конфигурации структурно˝ совме-
стимы с одним из участков молекулы белка. Такой способ выд˝еле-
ния функционально однотипных белков получил название афинной хроматографии. Разновидностью афинной хроматографии яв-
ляется иммуносорбция, основанная на весьма специфическо˝м взаимодействии белков с антителами — иммуноглобинами, ˝кото-
рые присоединяют к матрице биоспецифического сорбента.
5.5. КЛАССИФИКАЦИЯ БЕЛКОВ
Огромное разнообразие белков по составу и строению молек˝ул, физико-химическим свойствам и выполняемым функциям не по˝-
зволяет создать единой классификации белковых веществ. П˝о со-
ставу молекул белки подразделяют на два больших класса —˝ про-
теины и протеиды. Протеины — это типичные полипептиды, образованные только из аминокислот. Протеиды состоят из полипептидных группировок, с которыми прочно связаны другие соединения неаминокислотной (небелковой) природы.
Протеины. Молекулы протеинов заметно различаются по физи-
ко-химическим свойствам, и это положено в основу их класси˝фикации по группам растворимости или выполняемым функциям˝.
Растворимые в воде протеины называют а л ь б у м и н а м и. Типичными представителями альбуминов являются белок ку˝ри-
íîãî ÿéöà — овальбумин, водорастворимые белки зерна пшеницы,
ржи, ячменя — лейкозины, легумелин из зерна гороха и других зернобобовых культур.
Альбумины содержатся во всех тканях растений и обладают в˝ы-
сокой биологической активностью, так как к ним относятся ˝мно-
гие белки-ферменты, белковые ингибиторы ферментов, белки-˝ан- тивитамины, многие регуляторные белки. В зерне злаковых и зер-
нобобовых культур содержание альбуминов составляет 5—10 %˝, а
в семенах масличных культур, клубнях картофеля, корнеплод˝ах,
106
овощах, плодах и вегетативной массе растений концентраци˝я этих белков может достигать 20—30 % общей массы белков.
Белки, растворимые в растворах нейтральных солей, называю˝т г л о б у л и н а м и. Чаще всего для извлечения глобулинов ис-
пользуют 5—10%-е растворы NaCl или KCl.
Глобулины содержатся во всех клетках и тканях живых орга-˝
низмов и выполняют жизненно важные функции. К глобулинам относятся многие ферментные и регуляторные белки, а также˝ за-
пасные белки растений. Многие растительные глобулины выд˝еле-
ны в кристаллическом виде и хорошо изучены. Так, из семян со˝и
выделен глицинин, из фасоли — фазеолин, из гороха — легумин, èç
конопли — эдестин, из люпина — конглютин, из картофеля — туберин.
Особенно много глобулинов накапливается в зерне зернобо˝бо-
вых культур (60—70 % общей массы белков), семенах масличных
растений, клубнях картофеля и корнеплодах, овощах и плода˝х
(40—60 %). В зерновках злаковых культур концентрация глобули-˝ нов составляет 10—20 %, в вегетативных органах растений — 40—˝
50 % общей массы белков.
В семенах злаковых растений накапливается очень много за˝-
пасных белков, растворяющихся в 70%-м водном растворе этано-
ла, их называют п р о л а м и н а м и. Синтез в семенах проламинов — генетическая особенность злаковых растений, тогда˝ как в
растениях других семейств эти белки не образуются. Они та˝кже не
синтезируются в вегетативных органах растений (в том чис˝ле и
злаковых). Название «проламины» этой группе белков было ˝дано
вследствие того, что при их гидролизе образуется много ам˝инокислоты пролина и аммиачного азота.
Проламины — основные белки клейковины пшеницы и других˝
злаковых растений. Проламин пшеницы называют глиадином, кукурузы — зеином, îâñà — авенином, ячменя — гордеином, ðæè — секалином. Особенно много проламинов содержится в зерновках кукурузы и проса (35—55 % общей массы белков), пшеницы, ячме-
ня, овса (25—35 %) и значительно меньше в зерне ржи (10—20 %).
Белки, нерастворимые в воде, водных растворах солей и спир˝- та, но хорошо растворяющиеся в щелочных растворах (0,1—0,2%-й раствор NaOH), называют г л ю т е л и н а м и. Они содержатся в любых растительных клетках, но особенно их много в семена˝х зла-
ковых растений. Глютелины входят в состав клейковины. В се˝ме-
нах эти белки выполняют роль запасных веществ, а в листьях˝ глютелины, по-видимому, являются структурными белками. Наибо˝- лее хорошо изучены глютелины пшеницы — глютенины и глюте-
ëèíû ðèñà — оризенины.
Содержание глютелинов в зерне злаковых растений — 25—
40 %, в зерне риса — 60—70, в семенах масличных культур, клуб-
107
нях картофеля, корнеплодах, овощах, плодах — 10—20, в вегетативной массе растений — 20—30 % общей массы белков.
Альбумины, глобулины, проламины и глютелины растений состоят из большого набора индивидуальных белков. Методом э˝лек-
трофореза каждая из этих групп белков может быть разделен˝а на 20—30 компонентов, различающихся по электрофоретической
подвижности, а методом изоэлектрофокусирования — на не˝сколько десятков белковых компонентов.
В хромосомах клеточных ядер содержатся водорастворимые˝
белки — г и с т о н ы, играющие важную роль в образовании
структуры хроматина, так как связаны с ДНК. Они имеют высо-
кую концентрацию основных аминокислот — лизина и аргин˝ина (25—30 %), поэтому относятся к щелочным белкам, у которых
очень сильно выражены свойства оснований. Эти белки имеют˝
молекулярные массы 11—21 тыс. и разделяются на пять фракций,
обозначаемых как H1, H2a, H2б, H3, H4.
Основная функция гистонов — упаковка молекул ДНК в ядра˝х клеток высших организмов. Гистоны H2а, H2б, H3 и H4, взаимо-
действуя с ДНК, образуют упорядоченные ядерные структуры˝ —
нуклеосомы, связь между которыми обеспечивают гистоны H1.
Гистоны, богатые аргинином (H3 и H4), у разных организмов
очень мало различаются по аминокислотным последователь˝ностям, а богатый лизином гистон H1 по составу аминокислот проя˝в-
ляет довольно высокую видовую специфичность.
К протеинам также относятся с к л е р о п р о т е и н ы, пред-
ставляющие белки, которые нерастворимы в воде и большинст˝ве
других растворителей. Они выполняют структурную функцию˝, образуя длинные параллельные полипептидные цепи, соединен˝ные поперечными связями в прочные структуры. К этой группе белков
относятся коллаген сухожилий, миозин мышц, кератин волос,˝ эластин кровеносных сосудов, фиброин шелка.
Протеиды. В зависимости от химической природы небелковой части протеиды разделяют на несколько групп: гликопротеи˝ды,
хромопротеиды, липопротеиды, флавопротеиды, металлопрот˝еи-
ды, нуклеопротеиды и др.
Гликопротеиды. В составе молекул гликопротеидов к белку че- рез аминокислотные остатки присоединены моносахариды и˝ли их производные — манноза, галактоза, глюкозамин, глюкуроно˝вая
кислота и др. К гликопротеидам относятся многие ферменты,˝
мембранные белки, защитные белки (иммуноглобины и лектин˝ы), некоторые запасные белки (вицилин семян фасоли), белок вне˝- клеточного матрикса (ламинин), некоторые ядовитые белки (˝ри-
цин клещевины).
Чаще всего образуются гликопротеиды двух типов — N-гли-
копротеиды и O-гликопротеиды. В N-гликопротеидах к амидному˝
108
азоту аспарагина в составе белка присоединяется N-ацетилг˝люко- замин, к которому далее последовательно — остатки манно˝зы и некоторых других моносахаридных производных, образующи˝е разветвленный олигосахарид. В молекулах O-гликопротеидов˝
N-ацетилглюкозамин присоединяется O-гликозидной связью к остаткам серина или треонина белка. Как правило, углеводн˝ый
компонент гликопротеидов мало влияет на функциональные˝ свойства белка, но обеспечивает их связь с другими внутри˝клеточ-
ными компонентами. Известны также гликопротеиды, в которы˝х
содержится много олигосахаридных звеньев, и такие молеку˝лы по
структуре очень похожи на разветвленные полисахариды.
Липопротеиды. Они образуются при соединении белков с липидами и являются основными компонентами цитоплазматичес˝ких,
хлоропластных и митохондриальных мембран. При образован˝ии
мембранных липопротеидов к C- или N-концам полипептидных
цепей белка присоединяется гликолипидная или липидная г˝руп-
пировка, которая делает эту часть молекулы белка гидрофоб˝ной и поэтому способной к взаимодействию с липидными компонен˝та-
ми мембраны. Липидная часть липопротеида обычно представ˝ле-
на фосфатидилинозитом и диацилглицерином.
Нуклеопротеиды. Соединения белков с нуклеиновыми кислота-
ми играют важную роль в процессах жизнедеятельности орга˝низмов, связанных с передачей наследственной информации. Они˝ яв-
ляются главным веществом хромосом, рибосом и пластидных
факторов наследственности.
Фосфопротеиды. Это белки, в которых к остаткам серина, трео-
нина, тирозина, имеющим HO-группы, сложноэфирной связью присоединяются остатки ортофосфорной кислоты. Фосфорил˝ирование белков играет важную роль в регулировании активнос˝ти
ряда ферментов: гликогенфосфорилаз (катализирующих фосф˝оролиз гликогена), гликогенсинтетаз (катализирующих синтез˝ гликогена), синтетаз жирных кислот, пируватдегидрогеназы, мног˝их ферментов, образующих систему клеточного деления. Фосфор˝и-
лированию могут подвергаться также и другие белки — регулятор-
ные, защитные, транспортные, запасные.
Металлопротеиды. Имеют в своем составе группировки, содержащие атомы металлов. К ним относятся белки, обладающие ка˝- талитическими свойствами: цитохромы, пероксидаза, катала˝за,
глобины (осуществляющие связывание и перенос кислорода)˝, в
состав которых входит железо; аскорбинатоксидаза, феноло˝ксидазы, тирозиноксидаза, пластоцианин, содержащие медь; нитра˝тредуктаза, в состав которой входит молибден; нитрогеназа, вк˝люча-
ющая молибден и железо; многие другие ферменты.
Известны белки-ферменты, имеющие в своем составе произ-
водные витаминов и нуклеотидные группировки, в связи с че˝м та-
109
кие белки можно назвать витаминопротеидами и нуклеотидо˝протеидами. Более подробно они будут рассмотрены в главе 8.
К нуклеотидопротеидам относятся также G-белки, которые
выполняют важную функцию передачи сигнала другим белкам˝. Такие белки способны нековалентно связывать молекулы ГТ˝Ф и переходить в активную форму. К G-белкам относятся многие бе˝л-
ковые факторы в генетических системах синтеза белков, а т˝акже
белок трансдуцин, участвующий в передаче светового сигна˝ла у фотосинтезирующих клеток.
5.6. АМИНОКИСЛОТНЫЙ СОСТАВ БЕЛКОВ
Систематические исследования аминокислотного состава б˝елков были начаты во второй половине XIX в., когда были разрабо˝-
таны химические методы определения аминокислот в белков˝ых
гидролизатах. Однако значительные успехи в аминокислотн˝ом анализе полипептидов были достигнуты после разработки х˝рома-
тографических методов изучения органических веществ. В с˝овре-
менных исследованиях для определения аминокислотного с˝остава белков применяется метод ионообменной хроматографии с и˝с-
пользованием аминокислотных анализаторов, которые в авт˝ома-
тическом режиме разделяют смесь аминокислот, полученных˝ в результате гидролиза белков, на ионообменнике, производят и˝х ок-
рашивание и измерение оптической плотности окрашенного˝ ра-
створа, после чего данные спектрофотометрических измере˝ний выводятся на регистрирующее устройство.
Гидролиз белков проводят в кислой или щелочной среде, а та˝к- же с помощью протеолитических ферментов. В ходе гидролиза˝ пептидные связи, соединяющие аминокислотные остатки в бе˝лке, расщепляются и образуется смесь свободных аминокислот.
При кислотном гидролизе белки в течение определенного вр˝е- мени нагревают в ампулах при температуре 100...105 °C с крепкой соляной кислотой, при щелочном гидролизе нагревание прои˝зводят с разбавленным раствором щелочи.
В ходе кислотного гидролиза цистеин превращается в цисти˝н, а глутамин и аспарагин — в соответствующие аминокислоты.˝ В сильнокислой среде происходит практически полное разру˝шение триптофана и наблюдаются значительные потери цистина и м˝ети-
онина.
При щелочном гидролизе белков также происходит разруше-
ние некоторых аминокислот, но обеспечивается достаточно˝ высокий выход триптофана. Наименьшие потери аминокислот набл˝ю-
даются при ферментативном гидролизе.
110
