
Биохимия растений
.pdfВ биохимических системах в процессе переноса электронов˝ при осуществлении окислительно-восстановительных реакц˝ий происходит значительное изменение свободной энергии, св˝язанной со значением стандартных окислительно-восстановите˝льных
потенциалов донора и акцептора электронов следующим ура˝внением:
G°′ = –nF Å°′,
ãäå G°′— изменение свободной энергии в джоулях при стандартных˝ условиях (рН 7); n — число переносимых электронов от молекулы-донора на молекулу-ак- цептора; F — постоянная Фарадея (96 406 Дж · В–1); Å°′ — разность стандартных окислительно-восстановительных потенциалов акцептора и˝ донора электронов
ïðè ðÍ 7 (Å°′àêö – Å°′äîí).
Так, например, в реакциях обмена азотистых веществ происх˝о-
дит окислительно-восстановительная реакция превращения˝ окисленной формы глютатиона в восстановленную с участием вос˝ста-
новленных динуклеотидов НАДФ · Н:
Глютатион—S—S—глютатион +
+ÍÀÄÔ · Í + Í+ → 2 Глютатион—SH + НАДФ+
Âходе реакции происходит перенос двух электронов и двух
протонов от НАДФ · Н + Н+ на окисленный глютатион. Стандартный окислительно-восстановительный потенциал системы в˝ос-
становленный/окисленный глютатион при рН 7 равен –0,23 В, а
для системы НАДФ+/НАДФ · Н –0,32 В. Разность стандартных
окислительно-восстановительных потенциалов акцептора и˝ донора электронов будет равна:
Å°′ = Å°′àêö – Å°′äîí = Å°′глют. окисл – Å°′ÍÀÄÔ · Í = –0,23 Â –
–(–0,32) = –0,23 + 0,32 Â = 0,09 Â.
Изменение свободной энергии в этой реакции в расчете на
1 моль окисленного глютатиона при стандартных условиях рас-
считывают по указанной ранее формуле:
G°′ = –nF Å°′ = –2 · 96 406 · 0,09 = –17 353 Äæ ≈ –17,35 êÄæ.
В связи с тем что изменение свободной энергии в рассматри˝-
ваемой реакции отрицательно, она осуществляется самопро˝из-
вольно.
Мы рассмотрели основные способы определения изменения
свободной энергии в биохимических системах при стандарт˝ных
161
условиях. Однако условия физиологической среды в клетках˝ организмов очень сильно отличаются от стандартных условий, ос˝обенно по температуре и концентрации веществ. Стандартная тем˝пература 25 °С, а температура физиологической среды у разных˝ орга-
низмов изменяется в довольно широких пределах, у растений˝, например, от 0 до 50 °С. Концентрация веществ в физиологическо˝й
среде также очень сильно отличается от стандартной (1 моль˝/л), обычно она составляет сотые и даже тысячные доли моля на 1 л˝.
Изменение свободной энергии вещества в зависимости от те˝мпе-
ратуры и его концентрации в физиологической среде выража˝ется
следующим уравнением:
Gфизиол = G°′ + RTln C,
ãäå G°′ — стандартное изменение свободной энергии при рН 7; R — у˝ниверсальная газовая постоянная (8,31 Дж · моль–1 · Ê–1); Т — температура физиологической среды в единицах шкалы абсолютных температур (в кельв˝инах);Ñ — концентрация реагирующего вещества или продукта реакции в физи˝ологической среде
(ìîëü/ë).
Используя данное уравнение, в ходе реакции можно опреде-
лить изменение свободной энергии для каждого компонента˝ биохимической системы, находящегося в физиологической сред˝е.
Поскольку концентрации веществ в физиологической среде˝
меньше стандартной концентрации (1 моль/л) и выражаются
дробными числами, показатель lnC в указанном выше уравнении
будет иметь отрицательные значения, поэтому Gфизиол всегда будет меньше G°′, определенного при стандартных условиях. В слу-
чае экзергонической реакции в разбавленных физиологиче˝ских
растворах вероятность ее самопроизвольного осуществлен˝ия су-
щественно возрастает.
7.4. СОПРЯЖЕННЫЙ СИНТЕЗ ВЕЩЕСТВ
Для поддержания жизнедеятельности клеток организма в ни˝х постоянно происходят эндергонические реакции синтеза с˝ложных
веществ из простых, в ходе которых свободная энергия сист˝емы
возрастает. Источником свободной энергии для их осуществ˝ления служат экзергонические реакции, в которых энергия выделя˝ется, или окружающая среда, как, например, свет в реакциях фотоси˝н- теза. Если эндергоническая реакция осуществляется за сче˝т энергии, выделяющейся в сопряженной с ней экзергонической реа˝к-
ции, то такие две реакции называют сопряженными реакциями синтеза того или иного вещества, а происходящий в этих реакциях биохимический процесс получил название сопряженного синтеза веществ. Обе реакции катализирует, как правило, один фермент,
162
который объединяет их в одну термодинамическую систему. С˝у- ществует целый класс таких ферментов, называемых лигазам˝и или синтетазами, с участием которых осуществляется сопряжен˝ный синтез веществ.
Для того чтобы реакции сопряженного синтеза веществ могл˝и проходить самопроизвольно, согласно второму закону терм˝одина-
мики в экзергонической реакции должно выделяться энерги˝и больше, чем потребляется в эндергонической реакции, так к˝ак ко-
эффициент использования энергии в биохимических систем˝ах со-
ставляет 40—60 %. Кроме того, основное термодинамическое ус-
ловие самопроизвольного осуществления любых реакций в б˝иохи-
мической системе заключается в том, что общее количество ˝в ней свободной энергии в ходе реакции уменьшается. Поэтому сум˝мар-
ное изменение свободной энергии при сопряженном синтезе˝ бу-
дет оставаться величиной отрицательной, т. е. можно запи˝сать:
Gñîïð = Gýêç + Gýíä < 0.
Таким образом, оценивая процесс сопряженного синтеза ве-
ществ количественно, следует отметить, что в экзергоничес˝кой
реакции должно высвобождаться почти в 2 раза больше свобо˝д-
ной энергии, чем ее требуется для прохождения эндергониче˝с-
кой реакции. Однако в большинстве экзергонических и эндер˝гонических реакций, осуществляемых в организмах, изменение˝
свободной энергии характеризуется сопоставимыми величи˝нами
и обычно не превышает 20 кДж/моль. Поэтому большинство
биохимических реакций не способны высвобождать необход˝и-
мое количество свободной энергии для сопряженного синте˝за веществ. Для осуществления такого синтеза в организмах ис˝-
пользуются специальные реакции, в ходе которых происходи˝т
большое изменение свободной энергии, при стандартных услови-
ях оно составляет –30...–60 кДж/моль. В этих реакциях превраще-˝ нию подвергаются специализированные формы органических˝ веществ, называемые макроэргическими соединениями.
В составе макроэргического соединения имеется группиро˝вка,
которая присоединяется сильно поляризованной связью. Эт˝у
связь принято называть макроэргической и обозначать короткой волнистой линией (~). При взаимодействии макроэргического˝ соединения с определенным акцептором группировка, присоед˝и- ненная макроэргической связью, переносится ферментом на˝ мо-
лекулу акцептора, при этом в ходе реакции высвобождается ˝боль-
шое количество энергии. Схематически ход такой реакции мо˝жно
записать следующим образом:
Ì ~ õ + À → Ì + À – x, G°′ = –30...–60 êÄæ · ìîëü–1.
163
Поскольку в ходе превращений макроэргических соединени˝й происходит перенос группировки и высвобождается большо˝е количество свободной энергии, их также называют соединениями с высоким потенциалом переноса групп.
Макроэргические соединения подразделяют на три класса: фосфаты, тиоэфиры è имидазолы. Все они содержат в молекулах
сильно поляризованные макроэргические связи, которые со˝единяют разные группировки атомов.
Фосфаты. Соединения этого класса включают остатки фосфор-
ной кислоты, присоединенные макроэргической связью к нук˝лео-
тидной, ацильной, енольной или аминной группировке, в резу˝ль-
тате образуются четыре группы макроэргических фосфатов˝: нуклеозидполифосфаты, ацилфосфаты, енолфосфаты, амидинфосф˝а-
ты. В молекулах макроэргичесих фосфатов остаток фосфорно˝й
кислоты с макроэргической связью очень часто сокращенно˝ запи-
сывают ~ Ð .
Н у к л е о з и д п о л и ф о с ф а т ы (пирофосфаты) представляют собой производные нуклеотидов, к фосфатным группиро˝в-
кам которых макроэргическими связями присоединяются ещ˝е
один или два остатка фосфорной кислоты с образованием соо˝твет-
ствующих нуклеозиддифосфатов и нуклеозидтрифосфатов (с˝м.
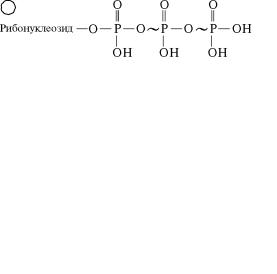
гл. 4). Наиболее важное биохимическое значение как макроэр˝ги- ческие соединения имеют следующие нуклиозидполифосфаты˝:
аденозинтрифосфат (АТФ), гуанозинтрифосфат (ГТФ), уридин-
трифосфат (УТФ), цитидинтрифосфат (ЦТФ), инозинтрифосфат
(ИТФ). Все они содержат пирофосфатную группировку с макро-˝
эргическими связями, присоединенную к рибонуклеотидном˝у остатку. Схематически строение указанных рибонуклеозидтр˝ифосфатов можно показать в виде следующей формулы:
В молекулах дезоксирибонуклеозидтрифосфатов также соде˝р- жатся пирофосфатные группировки с макроэргическими свя˝зями,
поэтому они являются макроэргическими соединениями. Одн˝ако
их биологическая роль заключается лишь в том, что они учас˝твуют в синтезе молекул ДНК, но не могут служить источником энер˝гии для сопряженного синтеза других веществ. Кроме участия в ˝со-
пряженном синтезе веществ рибонуклеозидтрифосфаты служ˝ат
источниками фосфатных групп для различных реакций фосфо˝рилирования, источниками энергии для биохимических процес˝сов
поглощения и транспорта веществ, являются исходными соед˝ине-
164
ниями в синтезе молекул РНК и коферментных группировок (НАД, НАДФ, ФАД, КоА).
А ц и л ф о с ф а т ы являются макроэргическими фосфатами карбоновых кислот. У них остаток фосфорной кислоты соедин˝я-
ется макроэргической связью с кислородом карбоксильной˝ группы кислоты. Строение ацилфосфатов выражается формулой
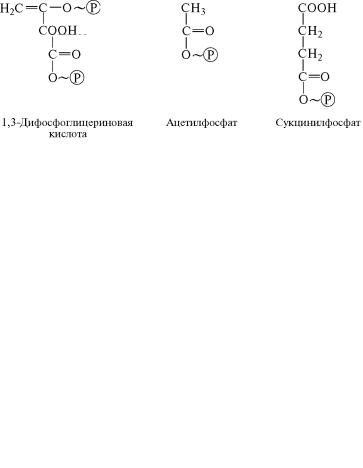
Важнейшие представители ацилфосфатов — 1,3-дифосфогли-
цериновая кислота, ацетилфосфат, сукцинилфосфат и др. Как˝ бу-
дет указано в дальнейшем, 1,3-дифосфоглицериновая кислота о˝б-
разуется в качестве промежуточного продукта в реакциях ц˝икла
Кальвина и анаэробной стадии дыхания, где этот макроэргич˝еский фосфат участвует в синтезе АТФ. Ацетилфосфат является˝
промежуточным продуктом в синтезе ацетилкофермента А, пр˝и-
нимающего участие во многих биосинтетических реакциях, а˝ сук-
цинилфосфат — промежуточным метаболитом при фосфороли˝зе
сукцинилкофермента А. Этот процесс происходит в цикле Кре˝бса и служит источником образования АТФ (у растений) или ГТФ (у˝
человека и животных).
Е н о л ф о с ф а т ы включают фосфоенолпировиноградную кислоту, которая является наиболее типичным представите˝лем этой группы макроэргических соединений. Ее формула
В молекуле фосфоенолпировиноградной кислоты остаток фо˝с-
форной кислоты соединен макроэргической связью с кислор˝одом
енольного гидроксила. Это соединение образуется в анаэро˝бной
стадии дыхания, а также при декарбоксилировании щавелево˝ук-
сусной кислоты с участием ГТФ. Это макроэргическое соедин˝е-
165

ние может служить источником фосфатной группы в процессе˝ синтеза АТФ и акцептором СО2 в реакциях карбоксилирования.
Àм и д и н ф о с ф а т ы имеют макроэргическую >N ~ P-связь
èиграют важную роль в реакциях обмена азотистых веществ ˝в ка-
честве промежуточных соединений. Одним из таких соединен˝ий
является аргининфосфат, образующийся как продукт фосфор˝или-
рования аминокислоты аргинина:
Тиоэфиры. У тиоэфиров макроэргическая связь возникает меж-
ду углеродом карбоксильной группы и атомом серы тиоловой˝ группировки (—SH). Среди них наиболее распространенные со-
единения — ацилтиоэфиры, которые представляют собой пр˝оиз-
водные карбоновых кислот и кофермента А:
Кофермент А включает остатки адениловой, пантотеновой и фосфорной кислот, а также тиоэтаноламина, имеющего тиолов˝ую
группу (см. с. 195). Сокращенно молекулу кофермента А записы-
вают как HS-КоА. Важными представителями ацилтиоэфиров яв-
ляются ацетилкофермент А и пропионилкофермент А:
Ацетилкофермент А — промежуточный продукт реакций дыха˝- ния, служит исходным соединением для синтеза жирных кисло˝т, фенольных и терпеноидных соединений, стероидных липидов˝.
Пропионилкофермент А — важный промежуточный продукт в обмене веществ микроорганизмов.
Имидазолы. Наиболее известным из макроэргических производных имидазола является ацетилимидазол:
166
В зависимости от типа макроэргической связи и природы ак-˝ цептора, на который переносится группировка макроэргиче˝ского соединения, изменение свободной энергии в результате его˝ превращения может варьировать в широком интервале. Для сравн˝е-
ния потенциалов переноса групп различных макроэргическ˝их соединений обычно определяют изменение свободной энергии˝ в ре-
акциях гидролиза макроэргических связей, в которых акцеп˝тора-
ми для переноса групп служат молекулы воды. Сопоставление˝ этих показателей проводят в стандартных условиях при рН 7˝.
Стандартные свободные энергии гидролиза (ΔG°′) важнейших мак-
роэргических соединений приведены далее.
Макроэргическое соединение |
G°′, |
|
êÄæ · ìîëü–1 |
||
|
||
Аденозинтрифосфат (при переносе фосфата) |
–30,6 |
|
Аденозинтрифосфат (при переносе пирофосфата) |
–42 |
|
1,3-Дифосфоглицериновая кислота |
–49 |
|
Ацетилфосфат |
–42 |
|
Фосфоенолпировиноградная кислота |
–62 |
|
Ацетилкофермент А |
–37 |
|
Аргининфосфат |
–32 |
|
Ацетилимидазол |
–50 |
Рассмотрим конкретный пример сопряженного синтеза ве-
ществ с участием макроэргического соединения. В процессе˝ син-
теза аминокислот довольно активно происходит образован˝ие амида глутаминовой кислоты глутамина из глутаминовой кисло˝ты и
аммиака под действием фермента глутаминсинтетазы. Это эн˝-
дергоническая реакция, в ходе которой поглощается свобод˝ная энергия в количестве G°′ = 14 кДж на 1 моль синтезируемого
глутамина.
Для осуществления эндергонической реакции синтеза глут˝амина проходит сопряженная экзергоническая реакция гидрол˝иза АТФ с высвобождением свободной энергии –30,6 кДж в расчете на 1 моль АТФ. Суммарное изменение свободной энергии в ука˝- занных сопряженных реакциях при синтезе 1 моля глутамина ˝рав-
íî G°′ñîïð = G°′ýêç + G°′ýíä = –30,6 + 14 = –16,6 кДж. Как следует из приведенных данных, общее количество свободной энер˝гии
при прохождении указанных реакций уменьшается, поэтому с˝ин-
тез глутамина за счет энергии гидролиза АТФ происходит са˝мопроизвольно.
Сопряженные реакции синтеза глутамина из глутаминовой
кислоты и аммиака с участием АТФ можно записать в виде сле˝-
167
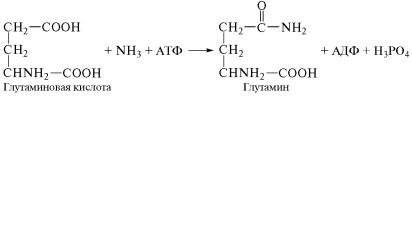
дующей схемы с учетом того, что в экзергонической реакции
свободная энергия уменьшается, а в эндергонической — увели-
чивается:
Суммарное уравнение сопряженного синтеза глутамина с уч˝ас-
тием АТФ под действием фермента глутаминсинтетазы можно˝ за-
писать следующим образом:
Среди всех макроэргических соединений центральное поло˝же-
ние занимает аденозинтрифосфат, или, как часто его называ˝ют, аденозинтрифосфорная кислота. Это макроэргическое соед˝ине-
ние служит источником энергии для большинства реакций со˝пряженного синтеза различных веществ, участвует в активации˝ молекул путем их фосфорилирования, трансмембранном транспор˝те
катионов водорода и органических веществ, служит источни˝ком
фосфатных групп для синтеза других макроэргических соед˝ине-
ний. В виде АТФ аккумулируется энергия в процессах фотоси˝н- теза и дыхания, а также осуществляется дальний транспорт ˝энергии по флоэмной системе растений и кровеносной системе че˝ловека и животных, тогда как большинство других макроэргиче˝с- ких соединений дальнему транспорту не подвергаются. АТФ содержится во всех живых клетках в количестве 0,5—20 ммоль/л
жидкой физиологической среды, и его концентрация поддержи-
вается на оптимальном уровне с помощью специальных регул˝я- торных систем.
Остатки фосфорной кислоты в молекулах АТФ обладают силь-
но выраженной способностью к ионизации, превращаясь в ани˝о- ны АТФ4–, которые в физиологической среде активно взаимодей-
ствуют с катионами магния Mg2+, образуя устойчивые комплексы
MgÀÒÔ2–.
168

Именно в виде таких комплексов АТФ взаимодействует с фер-˝
ментами в различных реакциях фосфорилирования и активац˝ии
органических веществ.
В реакциях сопряженного синтеза веществ молекулы АТФ мо-
гут гидролизоваться по одной из двух макроэргических свя˝зей с
образованием АДФ или адениловой кислоты (АМФ). При гидро-
лизе АТФ по первой макроэргической связи с образованием в˝ ка-
честве продуктов АДФ и неорганического фосфата высвобож˝дается 30,6 кДж свободной энергии в расчете на 1 моль АТФ (при
стандартных условиях):
ÀÒÔ + Í2Î → ÀÄÔ + H3PO4, G°′ = –30,6 êÄæ/ìîëü.
Гидролиз АТФ по такому механизму происходит в реакциях со˝-
пряженного синтеза аспарагина, глутамина, малонилкоферм˝ен-
та А, щавелевоуксусной кислоты и других соединений.
В сопряженных реакциях, где требуются большие энергетиче˝с- кие затраты, осуществляется гидролиз АТФ по второй (внутр˝енней) макроэргической связи с образованием пирофосфата, к˝оторый приводит к высвобождению в стандартных условиях 42 кДж˝ свободной энергии в расчете на 1 моль гидролизуемой АТФ:
ÀÒÔ + Í2Î → ÀÌÔ + Í4Ð2Î7, G°′ = –42 êÄæ/ìîëü.
Указанная реакция гидролиза АТФ инициируется при активации жирных кислот и аминокислот. Так, например, процессу˝
β-окисления жирных кислот в митохондриях предшествует их с˝вя-
зывание с коферментом А, на которое затрачивается энергия˝ гидролиза АТФ с образованием пирофосфата:
169

На биосинтетические процессы в организмах затрачиваетс˝я большое количество АТФ, которое восполняется за счет его ˝постоянного синтеза. В растениях и других организмах вырабо˝таны специальные механизмы образования АТФ, находящиеся, как м˝ы
увидим далее, под контролем регуляторных систем. В ходе си˝нтеза АТФ под действием ферментов инициируется образование ма˝кро-
эргической связи и присоединение к ней неорганического ф˝осфата, а затем осуществляется перенос остатка фосфорной кисл˝оты с
макроэргической связью на АДФ. В качестве продуктов в так˝их
реакциях синтезируются молекулы АТФ.
Образование макроэргической связи — эндергонический п˝ро-
цесс, на который затрачивается энергия, высвобождающаяся˝ в сопряженной экзергонической реакции или в результате напр˝авлен-
ного переноса протонов через хлоропластные и митохондриальные
мембраны под действием трансмембранного электрохимичес˝кого
потенциала, индуцируемого переносом электронов по элект˝рон-
траспортной системе этих клеточных органелл. Согласно пе˝рвому закону термодинамики на синтез АТФ из АДФ и неорганическо˝го
фосфата затрачивается такое же количество энергии, котор˝ое выс-
вобождается при гидролизе АТФ, однако изменение свободно˝й
энергии в ходе реакции будет уже с противоположным знаком˝:
ÀÄÔ + Í3ÐÎ4 → ÀÒÔ + Í2Î, G°′ = +30,6 êÄæ/ìîëü.
У большинства организмов происходит интенсивное образо˝ва-
ние АТФ за счет энергии окисления органических веществ в ˝анаэ-
робной стадии дыхания и реакциях цикла Кребса. Эти реакци˝и
получили название субстратного фосфорилирования, так ка˝к в них окисление дыхательных продуктов и образование макро˝эрги-
ческих связей сопряжено с фосфорилированием субстратов˝ дыха-
ния путем включения в состав органических веществ неорга˝ни-
ческого фосфата. Схематически процесс субстратного фосф˝орилирования можно представить в виде следующих превращени˝й:
Ñ+ Ô → Ñ : Ô
Органический |
Фермент |
Фермент-субстратный |
субстрат |
|
|
|
комплекс |
Ñ : Ô + Í3 ÐÎ4 → Ñ : Ð + Ô
Макроэргический
фосфат
Вначале фермент реагирует с органическим субстратом и ин˝и-
циирует образование макроэргической связи в фермент-субстрат-
ном комплексе. Затем ферментная группировка замещается о˝стат-
ком фосфорной кислоты неорганического фосфата, в результ˝ате
170
