
Биохимия растений
.pdf
ком, инициируя или замедляя процесс транскрипции соответ˝- ствующего гена. В опытах по изучению действия фиторегулят˝о- ров выяснено, что ауксины, цитокинины и гиббереллины усил˝и- вают синтез многих белков и всех форм РНК в цитоплазме, тог˝да
как абсцизовая кислота оказывает на указанные процессы п˝ротивоположное действие. В других экспериментах также показа˝но,
что ауксины могут активировать в цитоплазме синтез кислы˝х гидролаз, цитокинины — фермента нитратредуктазы, гиббе˝рел-
лины — образование в прорастающих зерновках злаков α-àìè-
лаз, катализирующих гидролитическое расщепление молеку˝л
крахмала.
Регуляция светом. В растениях как фототрофных организмах многие биохимические процессы регулируются светом, кото˝рый
воспринимают в качестве регуляторного сигнала рецептор˝ные
белки — фитохром è флавопротеиды, способные при поглощении
света определенной длины волны переходить в активную кон˝фор-
мацию и вызывать активацию или даже синтез ферментов. Фитохром представляет собой белок с молекулярной массой˝
~120 тыс., состоящий из двух полипептидных субъединиц и вклю˝-
чающий светочувствительную группировку — хромофор, который
образуется из четырех линейно соединенных пиррольных гр˝уппи-
ровок с определенным набором боковых радикалов:
При поглощении красного света (660 нм) в структуре одной из
пиррольных группировок происходит изомеризация двойных˝ свя-
зей, вызывающая конформационную перестройку молекулы бе˝лка:
231
Активированный светом белок связывается с клеточной мем˝б- раной и вызывает регуляторное действие примерно по таком˝у же механизму, как и гормоны. Если же активная форма фитохрома˝ поглощает свет с длиной волны 730 нм, то инициируется фотоиз˝о-
меризация хромофора в обратном направлении, вследствие ч˝его фитохром превращается в неактивную форму. В ряде опытов у˝ста-
новлено, что фитохром регулирует активность ферментов, ка˝тализирующих реакции фотосинтеза (фруктозо-1,6-дифосфатаза, гли˝-
церальдегидфосфатдегидрогеназа), проницаемость клеточ˝ных
мембран в листьях, синтез гормонов.
Другая группа фотосенсорных белков представлена флавоп˝ро-
теидами. У них хромофором служит флавиновая группировка, способная подвергаться фотохимическому превращению под˝ воз-
действием синего света.
8.8.КЛАССИФИКАЦИЯ ФЕРМЕНТОВ И ИХ УЧАСТИЕ
ÂМЕТАБОЛИЗМЕ РАСТЕНИЙ
Âсоответствии с принятой номенклатурой классификация
ферментов проводится в зависимости от типа катализируем˝ых
ими реакций, кроме того, учитывается природа субстратов, а˝кцеп-
торов и расщепляемых связей, а также особенности строения˝ от-
щепляемых, присоединяемых или переносимых групп. По типу катализируемых реакций все ферменты подразделяют на шес˝ть
классов:
1) î ê ñ è ä î ð å ä ó ê ò à ç û — окислительно-восстановительные
ферменты;
2) ò ð à í ñ ô å ð à ç û — катализируют реакции переноса атом-
ных группировок от молекулы донора к молекуле акцептора; 3) ã è ä ð î ë à ç û — катализируют гидролитическое расщепле-
ние веществ с участием молекул воды;
4) ë è à ç û — катализируют отщепление групп от органических субстратов с образованием двойных связей или присоедине˝ние определенных группировок за счет разрыва двойных связей˝;
5) è ç î ì å ð à ç û — ферменты изомеризации;
6) ë è ã à ç û (синтетазы) — катализируют реакции синтеза ве-
ществ, которые сопряжены с гидролизом АТФ или превращения˝- ми других макроэргических соединений.
Âкаждом из шести классов ферментов проводится их разделе˝- ние на ï î ä ê ë à ñ ñ û, а в подклассе выделяют группы ферментов, называемые ï î ä ï î ä ê ë à ñ ñ à ì è. В каждом подподклассе
отдельные ферменты записываются в определенной нумерац˝ии.
Согласно такой группировке каждый фермент имеет классиф˝ика-
ционный номер, который записывается в виде четырех чисел,˝ раз-
деленных точками. Первое число (записанное слева) указыва˝ет
232
принадлежность фермента к одному из шести классов, следую˝щее за ним число обозначает подкласс, третье число — подподк˝ласс, а четвертое — порядковый номер фермента в конкретном под˝подклассе. Так, например, фермент малатдегидрогеназа, катали˝зиру-
ющий превращение яблочной кислоты в щавелевоуксусную, им˝е- ет классификационный номер 1.1.1.37, который показывает, что
этот фермент относится к первому подклассу оксидоредукт˝аз, катализирующих окисление спиртовых групп, на что указывают˝
первые два числа (1.1). Третье число (1) выражает принадлежнос˝ть
данного фермента к первому подподклассу, который объедин˝яет
группу каталитически активных белков, имеющих в качестве˝ ко-
фермента НАД. Четвертое число (37) определяет порядковый но˝- мер фермента в указанном подподклассе.
8.8.1. ОКСИДОРЕДУКТАЗЫ
Ферменты, относящиеся к классу оксидоредуктаз, катализир˝у- ют реакции окисления и восстановления, происходящие в про˝-
цессе жизнедеятельности организмов. В зависимости от при˝роды
окисляемой группы в молекуле субстрата они подразделяют˝ся на
подклассы, а по типу акцептора электронов проводится разд˝еле-
ние подклассов на подподклассы.
Многие реакции биологического окисления происходят пут˝ем
отщепления от субстратов водорода, который присоединяет˝ся к
активному центру фермента и далее с участием фермента пер˝еда-
ется на акцептор. Ферменты, катализирующие такие реакции,˝ по-
лучили название дегидрогеназ. В ходе реакции субстрат, от которого отщепляется водород, окисляется, а акцептор, присоедин˝яю-
щий водород, восстанавливается. Фермент дегидрогеназа в п˝ро-
цессе каталитического действия, присоединяя водород, пер˝еходит
из окисленной формы в восстановленную, а затем, передавая˝ водород акцептору, снова превращается в окисленную форму и может катализировать окисление новой молекулы субстрата.
Âсамом общем виде действие дегидрогеназ можно представи˝ть
âвиде следующей схемы:
Субстрат—Н2 + Фермент → Окисленный субстрат + Фермент—Н2 Фермент—Н2 + Акцептор → Фермент + Акцептор—Н2
Если в ферментативных реакциях акцептором водорода служ˝ит кислород, то катализирующие их оксидоредуктазы называют˝
аэробными дегидрогеназами èëè оксидазами. Однако чаще всего де-
гидрогеназы передают отщепляемый от субстратов водород˝ дру-
гим акцепторам, в связи с чем такие ферменты называют анаэробными дегидрогеназами.
233
Анаэробные дегидрогеназы. Представлены большой группой ферментных белков, у которых в качестве коферментов служа˝т
НАД, НАДФ, ФАД, ФМН. Специфичность действия этих фер-
ментов зависит как от типа кофермента, так и от структуры ф˝ерментного белка. Чаще всего анаэробные дегидрогеназы обра˝зуют олигомерные структуры, включающие 2, 4, 6, а иногда и более по-
липептидных субъединиц.
НАД-зависимые дегидрогеназы катализируют окисление мно˝- гих субстратов в ходе реакций дыхания и распада различных˝ орга-
нических веществ: яблочной, изолимонной, глутаминовой кис˝лот,
глицерол-3-фосфата, глицеринового альдегида, оксипроизвод˝ных жирных кислот и др. Образующиеся в этих реакциях восстано˝в-
ленные формы дегидрогеназ чаще всего передают водород фл˝ави-
новым ферментам, имеющим коферменты в виде ФАД и ФМН, или участвуют в реакциях восстановления, в ходе которых п˝роис-
ходит синтез аминокислот из кетокислот, образование глиц˝ерол-
3-фосфата из фосфодиоксиацетона, превращение 3-фосфоглице˝- риновой кислоты в 3-фосфоглицериновый альдегид.
Рассмотрим примеры некоторых реакций, катализируемых
НАД-специфичными дегидрогеназами.
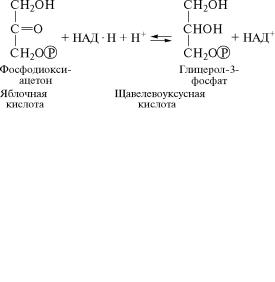
Малатдегидрогеназа (1.1.1.37) катализирует окислительное пре-
вращение яблочной кислоты в щавелевоуксусную в цикле ди- и
трикарбоновых кислот:
Глицерол-3-фосфатдегидрогеназа (1.1.1.8) катализирует реакции обратимого превращения фосфодиоксиацетона и глицерол-3-ф˝ос- фата в процессе синтеза и распада жиров:
234
3-Оксоацил-КоА-дегидрогеназа (1.1.1.35) катализирует окислительное превращение 3-оксиацилпроизводных жирных кислот˝ в кетопроизводные:
2 |
¾¾® |
2 |
RCHOHCH CO :S-ÊîÀ +ÍÀÄ+ |
|
RCOCH CO: S-ÊîÀ + |
3-Оксиацил-КоА |
|
3-Оксоацил-КоА |
+ ÍÀÄ·Í+Í+
НАДФ-зависимые дегидрогеназы катализируют многие восст˝а-
новительные реакции, происходящие в процессе фотосинтез˝а и
биосинтеза жирных кислот, а также окислительные превраще˝ния в ходе реакций пентозофосфатного цикла и окисления янтар˝ной
кислоты. Очень часто НАДФ-зависимые дегидрогеназы, катали˝-
зирующие восстановительные реакции, называют редуктазами.
Еноил-АПБ*-редуктаза (1.3.1.10) катализирует в ходе синтеза
жирных кислот восстановление ненасыщенных производных жирных кислот, связанных с АПБ:
R—CH=CH—CO :S-ÀÏÁ+ÍÀÄÔ·Í +Í ¾¾®
α,β-Ненасыщенное производное
¾¾® R—CH2—CH2—CO :S-ÀÏÁ+ÍÀÄÔ+
Насыщенное производное
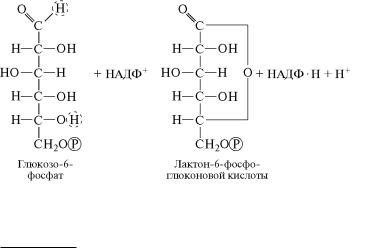
Глюкозо-6-фосфатдегидрогеназа (1.1.1.49) катализирует окисле-
ние глюкозо-6-фосфата в пентозофосфатном цикле:
По такому же механизму происходят и другие реакции, катал˝и-
зируемые НАДФ-зависимыми дегидрогеназами. ФАД-зависимые˝
дегидрогеназы катализируют отщепление водорода от карб˝ониль-
* Ацилпереносящий белок.
235

ных соединений и карбоновых кислот с образованием a,b-нена- сыщенных карбонильных соединений. Они участвуют также в р˝е- акциях превращения восстановленной формы липоевой кисл˝оты в окисленную, восстановления окисленных тиоловых соедине˝ний.
Сукцинатдегидрогеназа (1.3.99.1) катализирует в цикле ди- и трикарбоновых кислот окисление янтарной кислоты:
Ацил-КоА-дегидрогеназа (1.3.99.3) катализирует образование a,b-ненасыщенных производных в процессе b-окисления жирных
кислот:
R—CH2 —CH2 —CO :S-ÊîÀ + ÔÀÄ ¾¾®
Àöèë-ÊîÀ
¾¾® R—CH=CH—CO :S-ÊîÀ + ÔÀÄ ·Í2
α,β-Ненасыщенное производное
Глютатионредуктаза (1.6.4.2) катализирует восстановление окисленного глютатиона с участием НАДФ · Н:
G—S—S—G+ ÍÀÄÔ ·Í + Í+ ¾¾® 2G—SH + ÍÀÄÔ+
Окисленный |
Восстановленный |
|
глютатион |
||
глютатион |
||
|
Флавиновые дегидрогеназы, имеющие коферменты в виде ФАД и ФМН, способны окислять восстановленные формы НАД-
и НАДФ-зависимых дегидрогеназ, а также свободные восстановленные динуклеотиды НАД · Н и НАДФ · Н:
ÍÀÄ · Í + Í+ + ÔÌÍ ® ÍÀÄ+ + ÔÌÍ · Í2
ÍÀÄÔ · Í + Í+ + ÔÀÄ ® ÍÀÄÔ+ + ÔÀÄ · Í2
Восстановленные формы флавиновых дегидрогеназ могут пе˝редавать водород на хиноны и цитохромы. Так, в процессе окисл˝и- тельного фосфорилирования в митохондриях акцептором во˝дорода для восстановленных флавиновых дегидрогеназ служит у˝бихи-
нон, который называют коферментом Q:
236

В составе убихинона изопреновая группировка, заключенна˝я в
скобки, может повторяться в линейной структуре этого ради˝кала
6—10 ðàç.
При взаимодействии восстановленного флавинового фермен˝та с цитохромами осуществляется перенос электронов, а водор˝одные
атомы превращаются в ионы водорода:
ÔÀÄ ·Í2 + 2 öèò(Fe3+ ) ¾¾® ÔÀÄ + 2 öèò(Fe2+ )+ 2H+
Окисленный |
Восстановленный |
цитохром |
цитохром |
Аэробные дегидрогеназы (оксидазы). В процессе каталитическо-
го действия эти ферменты отщепляют водород от субстратов˝ и передают его на кислород с образованием молекул воды или пе˝рок-
сида водорода.
Аскорбатоксидаза (1.10.3.3) относится к группе ферментов,
способных переносить водород на кислород с образованием˝ воды.
В каталитическом центре этого фермента содержатся атомы˝ меди, которые участвуют в передаче электронов кислороду. В резу˝льтате
окисления в растительных тканях аскорбиновая кислота по˝д дей-
ствием аскорбатоксидазы превращается в дегидроаскорбин˝овую
кислоту:
Такие превращения особенно активно проходят в перезревш˝их
плодах и овощах, а также при нарушении режимов хранения ра˝с-
тительной продукции.
237

Полифенолоксидаза (1.10.3.1) è тирозиназа (1.14.18.1) также относятся к медьсодержащим оксидазам. Полифенолоксидаза к˝атализирует окисление фенольных соединений и дубильных вещ˝еств в тканях растений с образованием хинонов и воды:
Тирозиназа участвует в окислении аминокислоты тирозина˝ с
образованием темноокрашенных продуктов — меланинов (с˝м.
с. 555—556). При высокой активности полифенолоксидазы и тирозиназы происходит потемнение на воздухе разрезанных п˝лодов,
овощей и других растительных продуктов.
Гликолатоксидаза (1.1.3.1) принадлежит к ферментам, катали-
зирующим перенос водорода на кислород с образованием пер˝ок-
сида водорода. Под действием гликолатоксидазы происходи˝т окисление гликолевой кислоты в глиоксиловую в процессе ф˝ото-
дыхания у растений:
Коферментом в составе каталитического центра этого ферм˝ен-
та служит флавинмононуклеотид (ФМН).
Альдегидоксидаза (1.2.3.1) осуществляет окисление в живых клетках альдегидов в кислоты с участием молекул воды и ки˝слорода:
Роль кофермента также выполняет флавиновая группировка˝, но уже в виде ФАД.
Известны и другие оксидазы, катализирующие биохимически˝е
превращения в ходе окисления углеводов, нуклеотидов, амин˝о-
кислот и т. д. К ним можно отнести ксантиноксидазу, уратокс˝ида-
зу, глюкозооксидазу, оксидазы аминокислот, аминооксидазы˝ и др.
238

Оксигеназы. Известно довольно много биохимических реакций окисления, в ходе которых инициируется присоединение к су˝б- страту одного или двух атомов кислорода. Такие ферменты п˝ринято называть оксигеназами. Они играют важную роль в липидном
обмене растений и превращениях фенольных соединений. Липоксигеназа (липоксидаза) (1.13.11.12) — растительный фер-
мент, катализирующий окисление кислородом полиненасыще˝н- ных жирных кислот (линолевой, линоленовой), находящихся ка˝к
в несвязанном состоянии, так и в составе липидов. В ходе оки˝сле-
ния происходит образование гидропероксида и смещение дв˝ой-
ной связи, которое сопровождается ее переходом из öèñ- â транс-
конфигурацию:
Наиболее хорошо изучена оксигеназа сои, представляющая с˝о-
бой глобулин с молекулярной массой ~100 000. Она содержит в
каталитическом центре атомы железа. Образующиеся под дей˝- ствием липоксигеназы гидропероксиды обладают высокой о˝кис-
лительной способностью и подвергают дальнейшему окисле˝нию
другие молекулы ненасыщенных жирных кислот, а также разли˝ч-
ные соединения: аскорбиновую кислоту, аминокислоты, карот˝ин и другие пигменты. Поскольку в результате окисления гидро˝пероксидами пигментов происходит исчезновение окраски, пр˝едполагается, что действие липоксигеназы можно использовать˝ для от-
беливания теста и осветления мякиша хлеба. Повышенная акт˝ив-
ность липоксигеназы в растительных продуктах может вызы˝вать разрушение каротина при их сушке и хранении, а также иници˝и- ровать процесс прогоркания муки и крупы.
Примерно по такому же механизму, как действует липоксиге-˝
наза на ненасыщенные жирные кислоты, в организме животных˝ с участием специфической оксигеназы осуществляется превр˝аще-
ние каротина в витамин А.
Образование ненасыщенных жирных кислот также катализир˝у-
ют специфические оксигеназы с участием в качестве кофакт˝оров
восстановленных динуклеотидов НАДФ · Н. Предшественник˝ами
239

для синтеза ненасыщенных жирных кислот служат насыщенны˝е кислоты, связанные с коферментом А. В ходе этих реакций вна˝ча- ле происходит присоединение кислорода к субстрату, а зате˝м образование двойной связи:
R —CH —CH —R —CO :S-ÊîÀ +ÍÀÄÔ·Í +Í +Î ¾¾®
1 2 2 2 2 Насыщенная жирная кислота
¾¾® R1—CH=CH—R2—CO :S-ÊîÀ +ÍÀÄÔ+ +2Í2 Î
Ненасыщенная жирная кислота
Оксигеназы, катализирующие окисление кислородом стерои˝д-
ных соединений, содержат в активном центре группировку в ˝виде
гема, в связи с чем они получили наименование цитохрома Ð-450. Источником электронов для этого фермента служат восстан˝овлен-
ные нуклеотиды НАД · Н или НАДФ · Н. Под действием цитохр˝о-
ìà Ð-450 один из атомов молекулы кислорода присоединяется к
атому углерода в стероидной структуре, образуя гидроксил˝ьную
группу, а второй атом кислорода соединяется с водородом восстановленного динуклеотида и дает молекулу воды:
Многие оксигеназы из группы цитохрома Ð-450 связаны с мембранами эндоплазматического ретикулума, и для их функцио˝ни-
рования необходимы промежуточные переносчики, способны˝е
передавать электроны от НАДФ · Н на цитохром. Очень часто такими переносчиками электронов служат флавиновые фермен˝ты и ферредоксин.
Катализаторы пероксидного окисления. При окислении в орга-
низмах кислородом органических субстратов во многих слу˝чаях в
качестве одного из продуктов выделяются пероксид водоро˝да (Н2Î2) или органические пероксиды, которые могут окислять различные соединения. Одним из хорошо известных ферментов, с˝пособных катализировать реакции пероксидного окисления х˝ими-
ческих веществ в живых клетках, является пероксидаза (1.11.1.7), которая образует с пероксидом водорода комплексное соед˝ине-
ние, в результате чего пероксид переходит в активированно˝е состояние, превращаясь в акцептор водорода.
Растительные пероксидазы — двухкомпонентные ферменты˝,
локализованные главным образом в пероксисомах. В состав к˝ата-
240
