
- •Оглавление
- •Введение
- •1. Интерференция света
- •1.1. Электромагнитная волна на границе раздела сред
- •1.2. Интерференция света и условия её наблюдения. Когерентные источники света
- •1.2. Интерференция света в тонких пленках
- •2. Дифракция
- •2.1. Явление дифракции света. Условия ее наблюдения. Принцип Гюйгенса – Френеля
- •2.2. Метод зон Френеля. Прямолинейность распространения света
- •2.3. Дифракция на простейших преградах
- •Дифракция на круглом диске
- •Дифракция Фраунгофера
- •Дифракция на одной щели
- •Дифракция на дифракционной решетке
- •3. Поляризация
- •3.1. Естественный и поляризованный свет
- •3.2. Методы получения поляризованного света. Закон Брюстера
- •3.3. Анализ поляризованного света. Закон Малюса
- •3.4. Интерференция поляризованного света
- •3.5.Применение поляризованного света
- •4. Квантовые свойства света
- •4.1. Тепловое излучение и его характеристики
- •4.2. Законы теплового излучения
- •4.3. Оптическая пирометрия
- •4.4. Законы фотоэлектрического эффекта. Уравнение Эйнштейна
- •4.5. Практическое применение фотоэффекта
- •4.6. Фотоны. Масса и импульс фотона
- •4.7. Давление света
- •4.8. Эффект Комптона
- •4.9. Двойственная корпускулярно-волновая природа света
- •5. Атомная физика. Элементы квантовой физики
- •5.1. Модели атома. Спектры излучения атомов водорода
- •5.2. Постулаты Бора
- •Решая совместно уравнение второго закона Ньютона для электрона
- •5.3. Волновые свойства вещества. Гипотеза де Бройля. Принцип неопределенности
- •5.4. Волновая функция и уравнение Шредингера
- •Функция будет принимать то или иное значение в зависимости от внешних условий. Внешние условия – это силы, действующие на микрочастицу, представлены потенциальной функцией u ( X, y, z, t ).
- •5.5.Квантовомеханическое описание состояния электрона в атоме. Принцип Паули. Структура электронных оболочек атома
- •5.6.Вынужденное излучение. Лазеры
- •6.Атомное ядро. Элементарные частицы
- •6.1.Характеристики атомного ядра. Размер, состав и заряд атомного ядра
- •6.2. Дефект массы и энергия связи ядра
- •6.3. Ядерные силы
- •6.4. Радиоактивность. Закон радиоактивного распада
- •6.5. Элементарные частицы
- •6.6. Элементы космологии
- •Литература
6.Атомное ядро. Элементарные частицы
6.1.Характеристики атомного ядра. Размер, состав и заряд атомного ядра
Атом состоит из положительно заряженного ядра и окружающих его электронов. Атомные ядра имеют размеры примерно 10 -14… 10 -15м (линейные размеры атома – 10-10м).
Атомное ядро состоит из элементарных частиц протонов и нейтронов. Протонно-нейтронная модель ядра была предложена российским физиком Д. Д. Иваненко, а впоследствии развита В. Гейзенбергом.
Протон (р) имеет положительный заряд,
равный заряду электрона, и массу покоятp=1,6726∙10-27кг
![]() 1836me, гдеmeмасса электрона.
Нейтрон (n)нейтральная частица с массой покояmn=
1,6749∙10-27кг
1836me, гдеmeмасса электрона.
Нейтрон (n)нейтральная частица с массой покояmn=
1,6749∙10-27кг
![]() 1839тe,.Массу протонов и
нейтронов часто выражают в других
единицах – в атомных единицах массы
(а.е.м., единица массы, равная 1/12 массы
атома углерода
1839тe,.Массу протонов и
нейтронов часто выражают в других
единицах – в атомных единицах массы
(а.е.м., единица массы, равная 1/12 массы
атома углерода![]() ).
Массы протона и нейтрона равны
приблизительно одной атомной единице
массы. Протоны и нейтроны называются
нуклонами(от лат.nucleusядро). Общее число нуклонов в атомном
ядре называется массовым числомА).
).
Массы протона и нейтрона равны
приблизительно одной атомной единице
массы. Протоны и нейтроны называются
нуклонами(от лат.nucleusядро). Общее число нуклонов в атомном
ядре называется массовым числомА).
Радиусы ядер возрастают с увеличением массового числа в соответствии с соотношением R = 1,4А1/310-13 см.
Эксперименты показывают, что ядра не имеют резких границ. В центре ядра существует определенная плотность ядерного вещества, и она постепенно уменьшается до нуля с увеличением расстояния от центра. Из-за отсутствия четко определенной границы ядра его «радиус» определяется как расстояние от центра, на котором плотность ядерного вещества уменьшается в два раза. Среднее распределение плотности материи для большинства ядер оказывается не просто сферическим. Большинство ядер деформировано. Часто ядра имеют форму вытянутых или сплющенных эллипсоидов
Атомное ядро характеризуется зарядомZe,где Z зарядовое числоядра, равное числу протонов в ядре и совпадающее с порядковым номером химического элемента в Периодической системе элементов Менделеева.
Ядро обозначается тем же символом, что
и нейтральный атом:
![]() ,
гдеX символ
химического элемента,Zатомный номер (число протонов в ядре),А массовое
число (число нуклонов в ядре). Массовое
числоАприблизительно равно массе
ядра в атомных единицах массы.
,
гдеX символ
химического элемента,Zатомный номер (число протонов в ядре),А массовое
число (число нуклонов в ядре). Массовое
числоАприблизительно равно массе
ядра в атомных единицах массы.
Так как атом нейтрален, то заряд ядра Z определяет и число электронов в атоме. От числа электронов зависит их распределение по состояниям в атоме. Заряд ядра определяет специфику данного химического элемента, т. е. определяет число электронов в атоме, конфигурацию их электронных оболочек, величину и характер внутриатомного электрического поля.
Ядра с одинаковыми зарядовыми числами
Z, но с разными массовыми числамиА
(т. е. с разными числами нейтронов
N = A – Z), называются изотопами, а ядра
с одинаковымиА,но разнымиZ –изобарами. Например, водород (Z = l)
имеет три изотопа:
![]() Н
– протий (Z= l,N = 0),
Н
– протий (Z= l,N = 0),
![]() Н
– дейтерий (Z = l,N= 1),
Н
– дейтерий (Z = l,N= 1),
![]() Н
– тритий (Z = l,N = 2), олово –
десять изотопов и т. д. В подавляющем
большинстве случаев изотопы одного и
того же химического элемента обладают
одинаковыми химическими и почти
одинаковыми физическими свойствами.
Н
– тритий (Z = l,N = 2), олово –
десять изотопов и т. д. В подавляющем
большинстве случаев изотопы одного и
того же химического элемента обладают
одинаковыми химическими и почти
одинаковыми физическими свойствами.
Е,
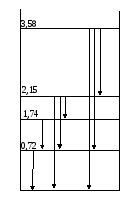
МэВ Рис.
6.1. Уровни
энергии и
наблюдаемые переходы для ядра атома
бора
Когда электрон переходит из более
высокого в более низкое энергетическое
состояние, разность энергий излучается
в виде фотона. Энергия этих фотонов
имеет порядок нескольких электронвольт.
Для ядер энергии уровней лежат в интервале
примерно от 1 до 10 МэВ. При переходах
между этими уровнями испускаются фотоны
очень больших энергий (γ–кванты). Для
иллюстрации таких переходов на рис. 6.1
приведены пять первых уровней энергии
ядра
![]() .Вертикальными линиями указаны наблюдаемые
переходы. Например, γквант
с энергией 1,43 МэВ испускается при
переходе ядра из состояния с энергией
3,58 МэВ в состояние с энергией 2,15 МэВ.
.Вертикальными линиями указаны наблюдаемые
переходы. Например, γквант
с энергией 1,43 МэВ испускается при
переходе ядра из состояния с энергией
3,58 МэВ в состояние с энергией 2,15 МэВ.
