
МЕТОДИЧЕСКОЕ ПОСОБИЕ- Орг. химия-Часть 1
.pdf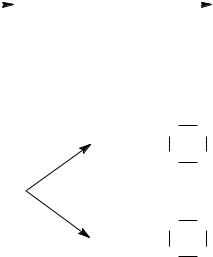
H2C |
|
|
|
|
C |
|
|
|
|
|
CH2 |
пропадиен; аллен |
|||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
H3C |
|
|
|
|
CH |
|
|
|
C |
|
|
|
|
CH2 |
бутадиен-1,2; метилаллен |
||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
H2C |
|
|
|
CH |
|
|
|
CH |
|
|
|
CH2 |
бутадиен-1,3; дивинил |
||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
H2C |
|
|
|
C |
|
|
CH |
|
|
CH2 |
2-метилбутадиен-1,3; изопрен |
||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
CH3 |
|
|||||||||||||||||||||||||||
H3C |
|
|
CH |
|
|
CH |
|
|
CH |
|
|
CH2 |
пентадиен-1,3; пиперилен |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||
H3C |
|
CH |
|
CH |
|
CH2 |
|
CH |
|
CH2 |
гексадиен-1,4 и т.д. |
||||||||||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||
Для диенов с изолированными двойными связями характерны обычные реакции олефиновых углеводородов, только в них принимает участие не одна, а две двойные практически независимые друг от друга связи.
Диены с кумулированными и сопряженными двойными связями проявляют своеобразные свойства.
Углеродный атом в алленах, несущий две двойные связи, находится в sp-гибридном состоянии, поэтому все три углеродных атома в аллене лежат на одной прямой. Аллены легко гидратируются с образованием кетонов.
R |
|
CH |
|
C |
|
CH2 |
HOH |
R |
|
CH |
|
C |
|
CH3 |
|
R |
|
CH2 |
|
C |
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
O |
|||||||
Они способны полимеризоваться с образованием четырехчленных циклов. Это свойство алленов используется для синтеза производных циклобутана.
H2C  C CH2
C CH2
H2C C  CH2
CH2
H2C  C
C  CH2
CH2
H2C  C CH2
C CH2
H2C  C CH2
C CH2
Сопряженные диеновые углеводороды вызывают наибольший теоретический и практический интерес. Они способны к полимеризации и получающиеся при этом полимеры обладают ценными техническими свойствами. Рассмотрим методы получения и свойства сопряженных диеновых углеводородов детальнее.
Способы получения
– Наиболее распространѐнным промышленным методом получе-
ния дивинила является дегидрирование бутан-бутиленовой фракции,
51

полученной пиролизом нефтяных дистиллятов. Процесс проводится в одну или в две стадии в присутствии катализатора (Cr2O3 + Al2O3 + Cu+2).
H3C |
|
CH2 |
|
CH2 |
|
CH3 |
|
H3C |
|
CH2 |
|
CH |
|
CH2 + H2 |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
H3C CH2 CH CH2
CH2  H2C
H2C  CH CH
CH CH CH2 + H2
CH2 + H2
Таким же способом получают изопрен из изопентан-амиленовой смеси, предварительно подвергая еѐ изомеризации.
– Другой, применяемый с 1932 года, промышленный синтез бутадиена-1,3 по С.В. Лебедеву заключается в пропускании паров этилового спирта при температуре 400 °C…500 °С над катализатором из оксидов магния и цинка
2C2H5OH → C4H6 + 2H2O + H2
Дивинил с хорошим выходом получается за один проход через катализатор. Реакция протекает через несколько стадий с промежуточным образованием альдегидов и двухатомных спиртов.
– Дивинил и изопрен получают также дегидратацией гликолей (двухатомных спиртов):
HOH2C |
|
|
|
CH2 |
|
|
CHOH |
|
CH3 |
Al2O3 |
|
C4H6 |
||||||||||
|
|
|
|
|
|
-2H O |
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
HOH C |
|
CH |
|
|
COH |
|
|
CH |
|
|
H2C |
|
CH |
|
C |
|
CH2 |
|||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|||||||||||||||||||
2 |
2 |
|
|
|
|
|
|
3 |
-2H2O |
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
– Изопрен получают также конденсацией изобутилена с муравьиным альдегидом. Процесс протекает в присутствии 25 %-ной Н2SO4 через стадию образования диметилизодиоксана
|
|
|
|
|
|
|
O |
|
H2C |
|
CH2 CH |
H3C |
|
C |
|
CH2 + 2 H |
|
|
|
|
3 |
||
|
|
|
C |
|
O |
|
C |
||||
|
|
||||||||||
|
|
|
|
||||||||
|
|
||||||||||
|
|
|
|
|
|
H |
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH3 |
|
H C |
|
O |
|||||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
2 |
|
|
|
который дегидратируется в изопрен
H4P2O7 |
|
|
|
|
|
|
|
|
|
|
O |
H2C |
|
CH |
|
C |
|
CH2 |
+ 2H2O + H |
|
C |
||
|
|
|
|
|
|||||||
на SiO2 |
|
|
|
|
|||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
H |
||||
|
|
|
|
|
CH3 |
|
|
||||
|
|
|
|
|
|
|
|
||||
Помимо этих промышленных синтезов дивинила и изопрена существует целый ряд методов их получения в лабораторных условиях. Описание этих методов можно найти в учебных пособиях и монографиях.
|
Физические свойства |
|
Дивинил при комнатных условиях – газ (tкип= – 3,00 °С; tплав = |
= – |
108,9 °С). Изопрен и другие простейшие диены – жидкости |
(tкип |
изопрена = 34 °С; tплав = –145 °С). Закономерности в изменении |
|
52 |
физических свойств, присущие гомологическим рядам углеводородов, действуют таким же образом и в ряду сопряженных диенов. Однако существование сопряжения систематически изменяет физические свойства диенов. Например, для дивинила и его гомологов свойственно завышение значений молекулярной рефракции на 1–2 единицы против расчѐта без учѐта сопряжения.
Химические свойства
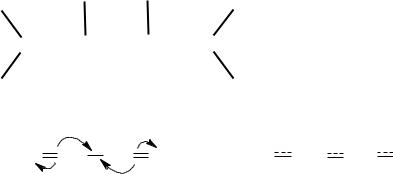
Во введении упоминалось, что в углеводородах типа дивинила возникает так называемое сопряжение за счѐт перекрывания р-электронных облаков атомов углерода, находящихся в состоянии sp2-гибридизации, приводящее к выравниванию электронной плотности. При этом возникает единая для всех четырѐх атомов молекулярная электронная орбита (система сопряжения). Результатом образования системы сопряжения является энергетическая стабилизация молекул сопряженных диенов (примерно на 15 кДж∙моль-1) и выравнивание длин углерод-углеродных связей в сопряженном фрагменте. В результате двойные связи в бутадиене-1,3 отклоняются к одинарной, а одинарная приближается к двойной, что иллюстрируется указанным на схеме порядком связей С–С в дивиниле (под порядком связей подразумевается число обобществленных поделенных электронных пар между двумя связанными атомами). Порядок связи С–С в этане равен единице, в этилене – двум.
H |
H |
H |
|
|
|
H |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
H3C |
|
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||
C |
|
C |
|
C |
|
|
C |
|
|
1 |
|
|
||
|
|
1,894 |
|
|
|
|
|
|
|
|
||||
1,894 |
1,447 |
|
|
|
|
|
H2C |
|
|
CH2 |
||||
H |
|
|
|
|
|
|
H |
|
|
|
||||
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
2 |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||
Молекулу дивинила иногда упрощѐнно изображают таким образом:
H C CH |
CH |
CH |
или СН |
СН СН |
СН |
2 |
|
2 |
2 |
|
2 |
Особенность химического поведения сопряженных систем как раз и состоит в способности этих систем реагировать как единое целое. Благодаря этому они могут присоединять различные вещества не только по двойным связям (1,2-присоединение), но и к крайним атомам углерода системы сопряжения (1,4- присоединение).
– Присоединение водорода в присутствии катализатора.
53
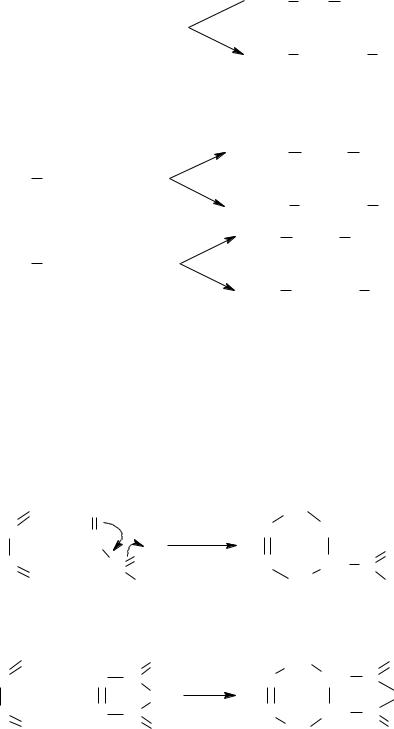
1,2 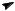
H3C CH2 CH CH2
CH2
H2C |
|
CH |
|
CH |
|
CH2 |
+ H2 |
|
|
|
|||||
|
|
||||||
|
|
|
|||||
|
|
|
|
|
|
|
1,4 |
–Таким же образом идѐт
галоидоводородов.
H3C CH CH CH3
CH CH3
присоединение галоидов и
H2C  CH CH
CH CH CH2
CH2
H2C  CH CH
CH CH CH2
CH2
+Cl2
+HCl
1,2 1,4 1,2 1,4
ClH2C CHCl CH CH2
CH2
ClH2C CH CH CH2Cl
CH CH2Cl
H3C CHCl CH CH2
CH2
H3C CH CH CH2Cl
CH CH2Cl
- Диеновый синтез, или реакция Дильса–Альдера
Диеновый синтез – это реакция присоединения сопряженного диена по типу 1,4 по двойной активированной связи диенофила.
Особенно легко эта реакция протекает тогда, когда двойная связь в диенофиле активизирована электроноакцепторным заместителем.
Реакция может идти только с сопряженными диенами:
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
|
|
CH |
CH |
|
|
|
|
HC |
2 |
2 |
|
HC |
CH2 |
|
+ CH |
|
O |
||||
|
|
|
|
|
|
|
HC |
CH2 |
C O |
HC |
CH C |
||
|
|
H |
CH2 |
H |
||
|
|
акролеин |
|
|
|
|
HC |
CH2 |
HC |
O |
H2C |
CH |
O |
|
C |
HC |
C |
|||
|
+ |
|
O |
|
|
O |
HC |
CH2 |
HC |
C |
HC |
CH |
C |
|
|
O |
H2C |
|
O |
|
малеиновый
ангидрид
Присоединение идѐт при лѐгком нагревании. Эта реакция используется для количественного определения сопряженных диенов и образования соединений с шестичленными циклами.
- Полимеризация
Этот процесс представляет огромный промышленный интерес, поскольку в результате полимеризации получаются каучукоподобные
54
продукты. Полимеризация может протекать под действием катализаторов и инициаторов. Катализаторы (металлоорганические соединения) ускоряют ионные реакции соединения в 1,4-положения. Инициаторы (пероксиды) ускоряют радикальную полимеризацию смешанного типа в 1,2- и 1,4-положения. Щелочные металлы также катализируют 1,2- и 1,4-полимеризацию.
nC4H6
1,4
1,2
1,2 1,4
H2C CH  CH CH2 CH2 CH
CH CH2 CH2 CH  CH CH2
CH CH2
H2C |
|
|
|
|
|
CH |
|
|
CH2 |
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH |
|
|
CH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
CH2 |
|
|
CH2 |
||||||||||||||||||||||
H2C |
|
|
CH |
|
CH2 |
|
|
CH |
|
CH |
|
CH2 |
|
CH2 |
|
|
CH |
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
||||||||||
Особенно ценные продукты получаются при стереорегулярной полимеризации по типу 1,4 с образованием цис-конфигурации каждого остатка. Такой процесс идѐт на металлоорганических катализаторах
... H |
CH |
|
|
CH |
|
|
CH |
|
|
CH |
|
CH |
|
CH |
|
.... |
||||||
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
||||||||||||||||||
C |
CH |
|
|
CH |
|
|
CH |
|
|
|
CH |
|
CH |
2 |
||||||||
|
|
|
||||||||||||||||||||
2 |
|
|
|
|
|
2 |
2 |
|
2 |
|
|
2 |
|
|
|
|
||||||
|
|
|
|
|
|
|
цис-полибутадиен |
|
|
|
|
|
|
|
||||||||
H3C |
H H3C |
|
|
H H3C |
|
H |
|
|
||||||||||||||
|
C |
|
C |
|
|
|
C |
|
|
|
C |
|
C |
|
|
C |
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
... H |
C |
CH |
|
|
CH |
|
|
CH |
|
|
CH |
|
CH2 .... |
|||||||||
|
|
|
|
|
|
|||||||||||||||||
2 |
|
|
|
|
|
2 |
2 |
|
2 |
|
|
2 |
|
|
|
|
|
|||||
цис-полиизопрен
Большое техническое применение имеют сополимеры диеновых углеводородов со стиролом, акрилонитрилом и другими продуктами.
Каучук
Натуральный каучук получают обработкой сока растений каучуконосов: гевеи, гваюлы, кок-сагыза, тау-сагыза и других. Это липкое мягкое вещество, имеющее малую прочность, набухающее во многих органических растворителях и непосредственно не имеющее технического применения. Лишь после открытия процесса вулканизации каучук нашѐл широкое применение в виде резины.
Строение натурального каучука в настоящее время известно во всех деталях. Он на 95 % состоит из стереорегулярного цис-полимера изопрена. Кстати, транс-полиизопрен тоже встречается в природе в виде
55
гуттаперчи. Молекулярная масса натурального каучука колеблется в пределах 150000–500000. Макромолекула каучука имеет спиральное строение и содержит более 1000 изопреновых остатков. Такое строение макромолекулы каучука обеспечивает его высокую эластичность и способность обратимо растягиваться до 900 % первоначальной длины. Отсутствие в большинстве стран рентабельных источников натурального каучука, стремление получить материалы, превосходящие по ряду свойств (масло- и морозостойкость, прочность к истиранию) натуральный каучук, стимулировали исследования по получению синтетического каучука (далее – СК). В 1932 году впервые в мире в
СССР осуществлѐн промышленный синтез СК по методу С.В.Лебедева. Мономерами для СК служат, в основном, диены: дивинил, изопрен, хлоропрен (2-хлорбутадиен-1,3). Для улучшения технических свойств СК диены часто полимеризуют совместно с мономерами, имеющими активный винильный остаток
Изопрен в присутствии металлоорганических комплексов даѐт СК, повторяющий по свойствам натуральный каучук.
Бутадиен-стирольный каучук является лучшей маркой СК для автомобильных покрышек.
Бутадиен-нитрильный каучук обладает вязкостью натурального и превышает его по устойчивости к истиранию, масло- и бензостойкости.
Бутилкаучук – сополимер изобутилена с дивинилом обладает высокой химической стойкостью и газонепроницаемостью, хороший изолятор для проводов и кабелей.
Важнейшим процессом превращения каучука в технический продукт – резину – является вулканизация, в результате которой повышается прочность, термостойкость, устойчивость к действию растворителей. При вулканизации к каучукам иногда добавляют наполнители (например, сажу) и красящие вещества. Вулканизация заключается в образовании новых поперечных связей между полимерными цепями.
При вулканизации серой образуются дисульфидные мостики:
... |
|
|
H3C |
S |
|
|
|
|
|
... |
|||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
H2C |
C |
CH |
|
CH2 |
|
|
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
||
... |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
C |
CH |
|
CH2 ... |
|||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
H3C |
S |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
56 |
|
|
|
|
|
|
|
|
||

Радикальная полимеризация приводит к образованию поперечных связей:
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||
... |
|
|
|
|
|
CH |
|
|
C |
|
|
CH |
|
CH2 |
|
... |
||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
... |
|
H2C |
|
C |
|
|
CH |
|
|
CH2 |
|
|
... |
|||||||||
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
H3C ... |
|
|
|
|
|
|
|
|
|
|||||||||||
1.4 Алкины (ацетиленовые углеводороды)
Ацетиленовые углеводороды – это большая группа органических соединений, которая характеризуется присутствием двух атомов углерода, связанных тройной связью. Общая формула ацетиленов СnН2n-2. Первым членом ряда является ацетилен
H C C H
C H
Ранее уже говорилось, что атомы углерода при тройной связи находятся в sр-гибридном состоянии и молекула ацетилена линейна.
Изомерия и номенклатура
Изомерия ацетиленов определяется положением тройной связи и строением углеродного скелета. Называют ацетиленовые углеводороды по номенклатуре ИЮПАК и по так называемой «ацетиленовой» номенклатуре. По «ацетиленовой» номенклатуре названия гомологов ацетилена строятся прибавлением к ацетилену названий радикалов, замещающих в нѐм атомы водорода. В случае номенклатур ИЮПАК пользуются теми же правилами, что и при названии олефинов, только окончание -ен заменяется на -ин.
HC |
|
|
CH |
|
|
этин, ацетилен |
||||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|||||||||||||||
|
|
|
|
|
||||||||||||||
HC |
|
|
|
C |
|
|
|
CH3 |
|
|
пропин, метилацетилен |
|||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
||||||||||||||
HC |
|
|
|
C CH2 |
|
CH3 |
бутин-1, этилацетилен |
|||||||||||
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||
H3C |
|
C |
|
|
|
C |
|
|
CH3 |
бутин-2, диметилацетилен |
||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
||||||||||||||||
HC |
|
C |
|
CH2 |
|
CH2 CH3 |
пентин-1, пропилацетилен |
|||||||||||
|
|
|
||||||||||||||||
|
|
|||||||||||||||||
|
|
|
||||||||||||||||
HC |
|
C |
|
|
CH |
|
CH3 |
3-метилбутин-1, изопропилацетилен |
||||||||||
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3
и т.д.
57

Способы получения
Рассмотрим вначале методы промышленного получения ацетилена.
– До недавнего времени основным источником ацетилена служил карбид кальция СаС2. Ацетилен получается при разложении карбида кальция водой:
CaC2 + 2H2O  Ca(OH)2 + HC
Ca(OH)2 + HC CH
CH
Метод найден Вѐлером ещѐ в 1862 г., но сохранил свое значение до сих пор. Однако он энергоѐмок при получении карбида кальция.
– Пиролиз углеводородов
Пиролиз метана осуществляется нагреванием природного газа до температуры 1400 °C. Он приводит к образованию ацетилено-водо- родной смеси.
2CH4 
 HC
HC  CH + 3H2
CH + 3H2
Метод также энергоѐмок.
– При окислительном пиролизе с добавкой кислорода часть метана расходуется на раскаливание аппарата, а остальной метан подвергается пиролизу.
4CH4 + 4O2 |
|
|
HC |
|
CH + CO2 + CO + 5H2O + 2H2 |
|
|
|
|||
|
|
|
|||
|
|
|
|||
Пиролиз метана ведется в крупном промышленном масштабе и |
|||||
является вторым после карбидного способа производства ацетилена. |
|||||
– Пиролиз |
жидких |
углеводородов при температурах |
|||
1200 °C…1500 °C приводит к образованию ацетилена легче, чем пиролиз метана. Этот метод широко используется в промышленности.
Ацетилен и его гомологи могут быть получены также следующими способами.
– Действием спиртовой щѐлочи на дигалогеналканы и галогеналкены.
H3C |
|
CHCl2 |
2KOH |
C2H2 + 2KCl + 2H2O |
||||||||||
|
спирт |
|||||||||||||
ClH2C |
|
CH2Cl |
KOH |
H2C |
|
CHCl |
KOH |
HC |
|
CH |
||||
|
|
|
|
|
|
|||||||||
|
спирт |
|
спирт |
|
||||||||||
|
|
|
||||||||||||
– Алкилированием металлических производных ацетилена.
HC |
|
CH |
CH3MgI |
CH4 |
+ HC |
|
CMgI |
|
RI |
HC |
|
C |
|
R + MgI2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
HC |
|
CNa + RBr |
|
|
|
HC |
|
C |
|
|
R + NaBr |
|||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
58 |
|
|
||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Физические свойства
Общие закономерности в температурах кипения и плотностях ацетиленов аналогичны закономерностям в рядах алканов и алкенов. Тройная связь повышает температуры кипения и плотности углеводородов.
Ацетилен: |
tкип = – 83,6 |
°C; |
tплав= – 81,8 |
°C ; d420 = 0,62 |
Пропин: |
tкип = – 23,3 °C; |
tплав= – 104,7 °C; |
||
Бутин-1: |
tкип = – 8,3 |
°C; |
tплав= – 130,0 |
°C. |
Химические свойства
При sр-гибридизации углеродных атомов, участвующих в образовании тройной связи, электроны, образующие тройную связь, оказываются втянутыми внутрь молекулы и менее реакционноспособны.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
C |
C |
|
|
H |
||||
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
При этом атомы углерода приобретают небольшой положительный заряд, что протонизирует водороды и они приобретают повышенную подвижность и слабокислый характер. Поэтому, несмотря на большую ненасыщенность, ацетилены менее активны в реакциях электрофильного присоединения с разрывом -связи (например, присоединение галогенов), чем олефины. И наоборот, они более склонны к реакциям с нуклеофильными реагентами (H2O, спирты, амины). Для ацетиленов с
концевой тройной связью характерен также второй тип реакций,
обусловленый подвижностью водородов при углеродах с тройной связью. Это реакции замещения этих водородов на металлы и присоединения самих ацетиленов с диссоциацией по связи ≡С Н.
Реакции присоединения по тройной связи
– Гидрирование ацетиленов протекает в тех же условиях, что и гидрирование олефинов. При этом реакция идет медленнее. Однако в смеси олефинов и ацетиленов в первую очередь гидрируются алкины, так как на поверхности катализатора они сорбируются прочнее и не допускают контакта с ней молекул алкенов. Это позволяет селективно удалять ацетилены из смесей их с олефинами.
59

HC |
|
CH |
H2 |
H2C |
|
CH2 |
H2 |
H3C |
|
CH3 |
|
|
|||||||||
|
|
|
|
|
||||||
|
Pt |
|
Pt |
|
||||||
|
|
|||||||||
|
– Присоединение к ацетиленам хлора, брома и йода также идѐт медленнее, чем к алкенам.
HC  CH Cl2
CH Cl2  ClHC CHCl Cl2
ClHC CHCl Cl2  Cl2HC CHCl2
Cl2HC CHCl2
1,2-дихлорэтен тетрахлорэтан
В промышленности от тетрахлорэтана под действием щелочей отщепляют HCl и получают важный растворитель – трихлорэтилен:
ClHC CCl2
CCl2
Гидролиз трихлорэтена даѐт другой ценный продукт – монохлоруксусную кислоту:
|
|
|
H2O |
|
|
O |
ClHC |
|
CCl2 |
CH2Cl |
|
C |
|
|
|
|
||||
|
|
|
||||
|
|
|||||
|
|
|
|
|
|
OH |
– Галогеноводороды присоединяются к ацетилену с
образованием этиленовых моногалогенидов, а затем и дигалогеналканов.
HC |
|
CH |
HCl |
H2C |
|
CHCl |
HCl |
H3C |
|
CHCl2 |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|||||||
|
|
по Марковникову |
|
||||||||
|
|
|
|||||||||
|
|
||||||||||
|
|
|
|
хлористый |
|
|
|
|
|
||
|
|
|
|
винил |
|
|
|
|
|
||
Это один из технических способов получения хлористого винила.
– Присоединение воды
В промышленности эту реакцию ведут по Кучерову в присутствии сульфата ртути или гетерогенных катализаторов.
Из ацетилена получают уксусный альдегид из его гомологов – кетоны.
O HC  CH + H2O HgSO4 H3C C
CH + H2O HgSO4 H3C C  H
H
R |
|
C |
|
CH + H2O |
|
R |
|
C |
|
CH3 |
||
|
||||||||||||
|
|
HgSO4 |
|
|
||||||||
|
||||||||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
O |
|
|
||
Присоединение идет по правилу Марковникова.
– Спирты присоединяются к ацетиленам по правилу Марковникова в присутствии алкоголятов (RONa). Получаются простые виниловые эфиры, которые используют как мономеры.
HC CH ROH H2C CH O R
RONa
60
