
МЕТОДИЧЕСКОЕ ПОСОБИЕ- Орг. химия-Часть 1
.pdf
Органические перекиси и гидроперекиси
Органические перекиси и гидроперекиси можно рассматривать как производные перекиси водорода, в которой соответственно один или оба водорода заменены на углеродные радикалы или ацильные группы
O
H3C C 
Гидроперекиси алкилов и ацилов имеют формулы R–О–О–H и
R C O O H
O
перекиси – соответственно R–О–О–R и
R |
|
C |
|
O |
|
O |
|
C |
|
R |
||||
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
O |
. |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
|
|
|
O |
|
|
O |
|
|
H |
гидроперекись метила |
||||
|
|
|
|
|
|
|
|||||||||
H3C |
|
C |
|
|
O |
|
OH |
гидроперекись ацетила |
|||||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(надуксусная кислота) |
|
|
|
O |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|||||
H3C O O C2H5 перекись метилэтила
Перекиси и гидроперекиси алкилов можно получить действием спиртов на гидропероксид водорода. Устойчивость их значительно возрастает при переходе от первичных к третичным алкильным заместителям.
Гидроперекиси и перекиси первичных алкилов при перегреве взрываются.
При нагревании перекиси и гидроперекиси сравнительно легко разлагаются с образованием свободных радикалов.
(CH3)3С |
|
O |
|
O |
|
H |
|
(CH3)3С |
|
O + H |
|
O |
|
|
|
|
|
|
(CH3)2С  O + H3C
O + H3C
В промышленности перекиси и гидроперекиси используют как инициаторы реакций полимеризации и сильные окислители.
121

4 КАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ (альдегиды и кетоны, оксосоединения )
4.1 Насыщенные карбонильные соединения
Как следует из реакций и способов получения, оксосоединения можно рассматривать как алканы, в которых два атома водорода при одном углероде замещены на двухвалентный атом кислорода. Функциональной группой оксосоединений является карбонильная
группа
 C
C  O
O
В зависимости от числа углеводородных радикалов, присоединенных к карбонильной группе, различают два вида оксосоединений:
альдегиды
O
R C 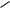
H
и кетоны
R C R
O ,
в реакциях которых проявляется много общего, но имеются и различия.
Номенклатура и изомерия
Номенклатура этих двух групп соединений строится по-
разному. Тривиальные названия альдегидов связывают их с тривиальными названиями кислот, в которые они переходят при окислении
O |
O |
O |
|
R C |
R C |
||
|
|||
H |
|
OH |
Из кетонов лишь немногие имеют тривиальные названия (например, ацетон). Для них широко используется радикальнофункциональная номенклатура, в которой названия кетонов даются с использованием названий радикалов, связанных с карбонильной группой. По номенклатуре ИЮПАК названия альдегидов
производятся от названия углеводорода с тем же числом атомов углерода
122

путѐм добавления окончания –аль. Для кетонов эта номенклатура требует окончания –он. Цифрой обозначается положение функциональной группы в цепи кетона (табл. 6).
Таблица 6 – Названия некоторых карбонильных соединений
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Названия по триви- |
Названия по |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альной и радикально- |
|
|
|
|
|
|
|
Соединение |
|
|
номенклатуре |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
функциональной |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ИЮПАК |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
номенклатурам |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
муравьиный |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
C |
H |
|
|
|
|
|
|
|
альдегид; |
метаналь |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
формальдегид |
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
уксусный альдегид; |
|
||||
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
этаналь |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
ацетальдегид |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
пропионовый |
|
||||||||
|
|
|
|
|
|
|
|
H5C2 C |
|
|
|
|
|
|
|
пропиональ |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
H3C |
|
|
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
|
C |
|
H |
масляный альдегид |
бутаналь |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
изомасляный |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
|
|
|
CH |
|
|
|
C |
|
|
|
|
|
|
|
метилпропаналь |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
альдегид |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
валериановый |
|
H3C |
|
|
CH2 |
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
C |
пентаналь |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
альдегид |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
изовалериановый |
|
|
H3C |
|
|
|
|
|
|
|
|
CH |
|
|
|
|
CH2 |
|
|
|
|
C |
|
|
3-метилбутаналь |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
альдегид |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
H3C |
|
|
|
|
C |
|
|
|
|
|
CH3 |
|
|
ацетон; |
пропанон |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
диметилкетон |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
H3C |
|
|
|
|
C |
|
|
|
|
C2H5 |
|
|
метилэтилкетон |
бутанон |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
H3C |
|
|
C |
|
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
CH3 |
метилпропилкетон |
пентанон-2 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
H3C |
|
|
|
|
|
C |
|
|
|
|
CH |
|
|
CH3 |
метилизопропилкетон |
3-метилбутанон-2 |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
CH3 |
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
123
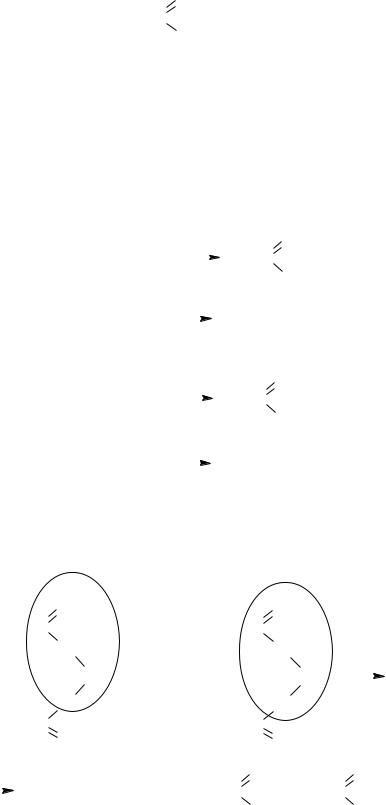
Изомерия альдегидов и кетонов полностью отражается номенклатурой и комментарий не требует. Альдегиды и кетоны с одинаковым числом атомов углерода являются изомерами.
Например:
|
|
|
|
|
O |
|
|
|
|
|
|
|
H3C |
|
CH2 |
|
C |
H |
H3C |
|
C |
|
CH3 |
||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
O |
|||||
|
|
|
|
|
|
|
|
|||||
пропаналь |
|
пропанон |
||||||||||
|
|
C3H6O |
|
C3H6O |
||||||||
Способы получения
– Окисление или каталитическое дегидрирование первичных спиртов до альдегидов, вторичных – до кетонов. Реакции эти уже упоминались при рассмотрении химических свойств спиртов.
|
|
|
|
|
|
|
|
|
|
|
|
|
Cu |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||
R |
|
|
CH2OH |
|
R |
|
|
|
|
|
C |
|
+ H2 |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
R |
|
|
|
|
CH |
|
|
R' |
Cu |
R |
|
|
|
C |
|
|
R' + H2 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
R |
|
|
CH2OH |
O |
|
|
|
R |
|
|
|
C |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
+ H2O |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
R |
|
|
|
|
CH |
|
|
R' |
|
O |
|
R |
|
|
|
|
C |
|
|
R' + H2O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
||||||||||
– Пиролиз кальциевых или бариевых солей карбоновых кислот, одна из которых – соль муравьиной кислоты, даѐт альдегиды.
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|||||||
H3C |
|
C |
O |
|
H |
|
C |
O |
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
Ca |
+ |
|
|
|
|
Ca |
|
t ° |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|||||||
H3C |
|
C |
O |
|
H |
|
C |
O |
|
|
|
||||||||||
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
t ° |
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
|||
|
H3C |
|
C |
|
CH3 |
+ H3C |
|
C |
|
+ H |
|
C + CaCO3 |
|||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
пропанон |
этаналь |
метаналь |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
124 |
|
|
|
|
|
|
|
||
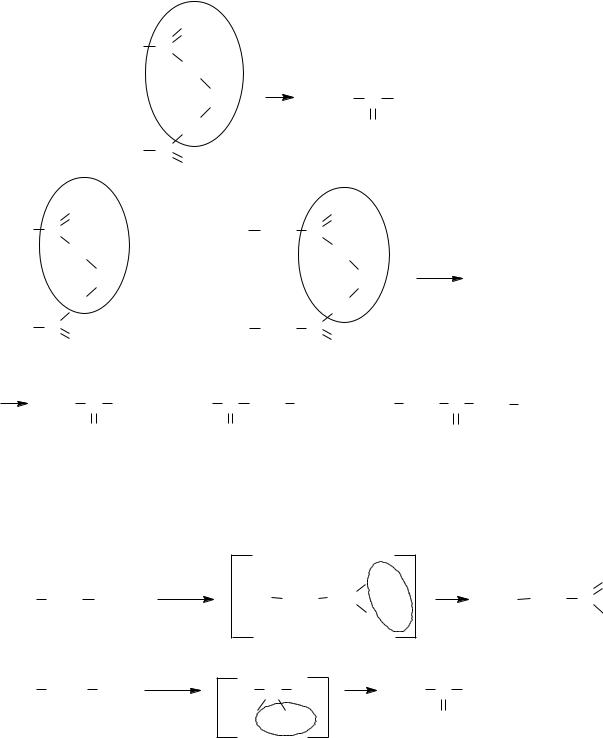
Во всех других случаях образуются кетоны.
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Ca |
t ° |
H3C |
C |
|
CH3 |
+ CaCO3 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
H3C |
|
C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
H3C |
C |
|
|
|
|
|
H3C CH2 |
C |
|
|
|
|
|
|
|
||
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
Ca |
|
|
+ |
|
|
|
|
|
Ca |
|
t ° |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
O |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
H3C |
C |
O |
|
|
|
|
H3C |
CH2 |
C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
t ° |
H3C C CH3 |
+ H3C |
C CH2 CH3 + H3C CH2 C CH2 |
CH3 + CaCO3 |
|||||||||||||
|
|||||||||||||||||
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
ацетон |
|
|
метилэтилкетон |
|
|
|
диэтилкетон |
|
|||||||
|
– Гидролиз геминальных (заместители у одного углерода) |
||||||||||||||||
дигалогеналканов |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
2H2O |
|
|
|
|
|
OH |
|
-H2O |
|
O |
||
H3C |
CH2 |
CHCl2 |
H3C |
CH2 HC |
|
|
|
H3C |
CH2 C |
||||||||
- 2HCl |
OH |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропаналь H |
|||
H3C |
CCl2 |
CH3 |
|
2H2O |
H3C |
C |
CH3 |
-H2O |
H3C |
C CH3 |
|
||||||
- 2HCl |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
O |
|
|
||
пропанон
– Гидратация ацетилена и его гомологов протекает в присутствии сульфата ртути (реакция Кучерова) или над гетерогенным катализатором. В соответствии с правилом Марковникова из ацетилена получается уксусный альдегид из его гомологов – кетоны (смотри свойства ацетиленовых углеводородов).
125
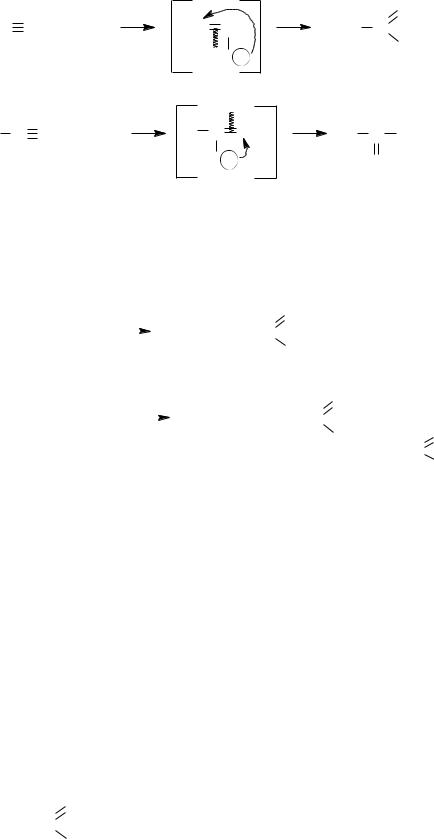
|
|
|
O |
HC CH + H2O |
H2C CH |
H3C C |
|
|
|
OH |
H |
|
|
|
|
R C CH + H |
O |
R C CH2 |
R C CH |
2 |
|
|
3 |
|
|
OH |
O |
– Оксосинтез. Эта реакция синтеза альдегидов из алкенов и смеси оксида углерода (II) с водородом открыта в 1938 году Реппе и является основным промышленным методом синтеза альдегидов С3 и выше. Процесс проводят при температуре 100 °C…200 °C и 100…200 атмосферах в присутствии кобальтового или никелевого катализатора.
|
|
|
|
|
|
|
Co |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||||
H2C |
|
CH2 + CO + H2 |
H3C |
|
|
CH2 |
|
|
C |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
Co |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
R |
|
CH |
|
CH2 + CO + H2 |
|
R |
|
|
CH2 |
|
|
|
CH2 |
|
C + R |
|
|
CH |
|
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
||||
Физические свойства
Муравьиный альдегид – газ. Остальные низшие альдегиды и кетоны – жидкости, плохо растворимые в воде. Альдегиды имеют удушливый запах. Кетоны пахнут обычно приятно. Температуры кипения оксосоединений растут с увеличением молекулярной массы. Кетоны кипят выше изомерных альдегидов. В противоположность спиртам альдегиды и кетоны – слабо ассоциированные жидкости. Поэтому они кипят значительно ниже соответствующих спиртов.
Структурная формула |
tкип, °C |
Структурная формула tкип, °C |
|||||||||||||||||
H3C |
|
CH2 |
|
CH2OH |
97,4 |
H3C |
|
|
|
|
CH |
|
CH3 |
82,4 |
|||||
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
CH2 |
|
|
H3C C CH3 |
|
|||||||||||||
|
|
C |
48,8 |
56,1 |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
O |
||||||||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
В то же время, карбонильные соединения кипят выше углеводородов с той же молекулярной массой. Плотность их ниже единицы.
126

Химические свойства
Альдегиды и кетоны – соединения весьма активные. Высокую реакционную способность сообщает им карбонильная группа. По своей природе двойная связь С=О в карбонильной группе сходна с двойной связью между атомами углерода. Она образуется из - и π-связей (как у алкенов). Однако кислород более электроотрицателен по сравнению с углеродом. Поэтому электронная плотность у кислорода выше, чем у углерода при двойной связи. Вследствие этого связь С=О сильно поляризуется и реакционная способность ее возрастает. Углеродный атом обладает электрофильными свойствами и способен присоединять нуклеофильные реагенты. Кислород имеет дробный отрицательный заряд и легко атакуется электрофильными реагентами.
C O
В то же время, карбонильная группа, связанная в альдегидах с одним алкильным радикалом, а в кетонах – с двумя, оказывает влияние на них, смещая электронную плотность с радикалов к положительно заряженному углероду карбонила.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
R |
CH2 |
|
|
C |
|
|
CH2 R |
R CH2 C |
|
|
3 3 |
3 |
3 |
||||
|
|
|
|
CH |
H C |
CH |
H C |
|
|
|
H |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
При этом степень поляризации связи С=О несколько понижается: у альдегидов в меньшей степени (за счет одного радикала), у кетонов – в большей (за счет двух радикалов), а подвижность водородов при - углеродах радикалов возрастает: у альдегидов в большей степени у кетонов – в меньшей.
Таким образом, для карбонильных соединений наиболее характерны два типа реакций: 1) реакции присоединения по карбонильной группе и 2) реакции, обусловленные высокой подвижностью водородных атомов при -углеродах радикалов по отношению к карбонилу. Причем в обоих типах реакций альдегиды
активнее кетонов.
Реакции присоединения
– Восстановление. Присоединение водорода к оксосоединениям происходит в присутствии катализаторов гидрирования (Ni, Pt, Pd, Cu и другие). Альдегиды при этом дают первичные, а кетоны – вторичные спирты.
127
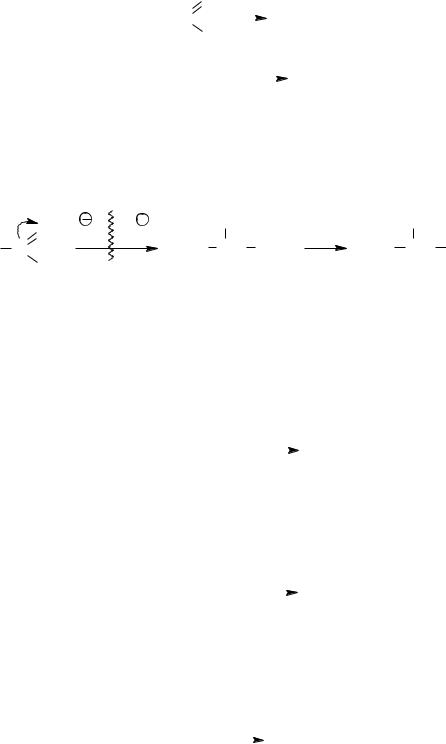
|
|
|
|
|
|
|
O |
H2 |
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
|
|
|
C |
|
|
|
|
H3C |
|
CH2OH |
||||||||||
|
|
|
H |
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
|
|
C |
|
CH3 |
|
H2 |
|
H3C |
|
|
CH |
|
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||
– Присоединение магнийорганических соединений. Эта типичная и важная реакция была рассмотрена в разделе спиртов.
|
|
|
|
|
|
OMgBr |
|
OH |
|
|
|
|
|
|
|
||||
|
|
O |
CH3 |
MgBr |
|
|
H2O |
|
|
H C |
C |
|
H C CH CH |
H C CH |
CH + MgBr(OH) |
||||
|
|
|
|
||||||
3 |
|
|
|
|
3 |
3 |
|
3 |
3 |
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
После гидролиза аддуктов из формальдегида получаются первичные спирты, из всех остальных альдегидов – вторичные, и из кетонов – третичные спирты.
– Присоединение синильной кислоты приводит к образованию
α-оксинитрилов. Гидролизом из них получают α-гидроксикислоты.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
H3C |
|
|
|
C |
|
|
|
O |
|
+ HCN |
|
|
|
|
|
H3C |
|
|
C |
|
CN |
||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нитрил -гидрокси- |
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
пропионовой кислоты |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
H3C |
|
|
C |
|
|
O |
|
+ HCN |
|
|
|
|
|
H3C |
|
|
|
C |
|
|
CN |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
нитрил -гидрокси- |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
изомасляной кислоты |
||||||||||||||||
|
|
|
|
|
|
OH |
|
|
|
H2O |
|
|
|
|
OH |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H3C |
|
|
|
|
C |
|
|
|
C |
|
H3C |
|
C |
|
|
|
COOH + NH3 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
H |
|||||||||||||||||||
нитрил -гидрокси- |
|
|
|
|
|
|
-гидрокси- |
||||||||||||||||||||||||||||||
пропионовой |
|
|
|
|
|
|
пропионовая |
||||||||||||||||||||||||||||||
кислоты |
|
|
|
|
|
|
|
кислота |
|||||||||||||||||||||||||||||
– Присоединение кислой соли бисульфита (гидросульфита) натрия даѐт кристаллические вещества – бисульфитные производные альдегидов и кетонов. Из кетонов в реакцию вступают только метилкетоны R–CO–CH3.
128
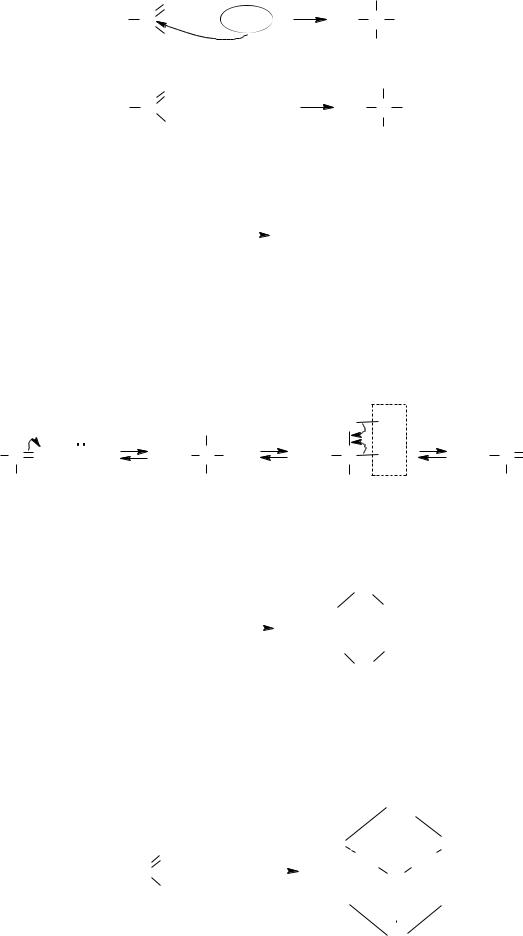
|
O |
|
|
|
|
OH |
|
|
|
|
|
|
|
||
R |
C |
+ HSO3Na |
|
R |
C |
SO3Na |
|
|
H |
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
R |
C |
+ HSO3Na |
R |
C |
SO3Na |
||
|
CH3 |
|
|
|
CH3 |
||
|
|
|
|
|
|
||
При нагревании с раствором соды бисульфитные производные разлагаются с выделением свободного альдегида или кетона.
|
|
OH |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
2R |
|
C |
|
O + Na2SO3 + CO2 + H2O |
|
2R |
|
C |
|
SO3Na + Na2CO3 |
|
|
|
|||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|||||||||
|
|
CH |
|
|
|
CH3 |
||||||
3 |
|
|
|
|
|
|
|
|||||
Реакция с бисульфитом натрия используется для качественного определения альдегидов и кетонов, а также для их выделения и очистки.
– Присоединение аммиака. Взаимодействие с аммиаком позволяет различить альдегиды и кетоны. Альдегиды образуют с аммиаком
альдимины.
|
|
|
|
|
HN |
H |
|
|
|
|
|
|
NH3 |
|
|
|
|||
|
|
|
|
|
|
|
|
||
H C C |
O + NH |
3 |
H C C |
O |
H C C |
OH |
H C C |
NH + H |
O |
3 |
|
3 |
|
3 |
|
3 |
2 |
|
|
H |
|
|
H |
|
H |
|
H |
|
|
|
|
|
|
|
|
|
ацетальдимин |
|
|
Альдимины легко циклизуются в альдегидаммиаки.
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
||||
|
|
|
|
|
|
|
NH |
|
NH |
||||||
3H3C |
|
C |
|
NH |
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
CH |
|
CH |
|
CH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
H |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
NH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
ацетальдегидаммиак
Кетоны реагируют с аммиаком очень медленно и сложно. Совершенно своеобразна реакция формальдегида с аммиаком,
приводящая к гексаметилентетрамину или уротропину.
|
|
|
|
|
|
|
|
CH2 |
||
|
|
|
O |
|
|
N |
|
N |
||
|
|
|
|
|
|
H2C |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
||
6 H C |
|
+ 4NH3 |
||||||||
H |
|
N |
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
CH2 |
|||
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
CH2 |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
||
|
|
|
|
129 |
|
|
|
|
|
|
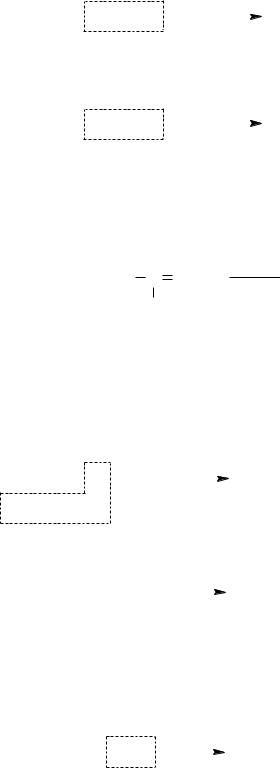
Уротропин и его комплекс с CaCl2 (кальцекс) применяется в медицине (мочегонное, противогриппозное средство). Нитрованием уротропина получают сильное взрывчатое вещество – гексоген.
– С гидроксиламином альдегиды и кетоны дают альдоксимы и кетоксимы (реакция идет по схеме, показанной выше для реакции с аммиаком). Суммарно:
H3C |
|
C |
|
O + H2NOH |
|
H3C |
|
C |
|
NOH + H2O |
||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||
|
|
H |
|
|
|
H |
||||||
|
|
|
|
|
|
|
ацетальдоксим |
|||||
H3C |
|
C |
|
O + H2NOH |
|
H3C |
|
C |
|
NOH + H2O |
||
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
CH3 |
|
|
|
CH3 |
||||||
|
|
|
|
|
|
|
ацетоноксим |
|||||
Под действием водоотнимающих средств (P2O5) альдоксимы (но не кетоксимы) переходят в нитрилы кислот. Это один из методов синтеза нитрилов.
H3C C NOH - H2O CH3C
CH3C N H
N H
Реакция с солянокислым гидроксиламином является качественной реакцией на карбонильную группу и используется также для количественного определения альдегидов и кетонов.
– С гидразином в зависимости от соотношения реагентов
реакция протекает по разному:
с одной молекулой оксосоединения образуются гидразоны
R |
|
C |
|
R' + H2N |
|
NH2 |
|
H2O + R |
|
C |
|
N |
|
NH2 |
|||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|||||||||||||
|
|
O |
|
|
|
|
|
|
|
R' |
|||||||
|
|
|
|
|
|
|
|
|
|
|
гидразон |
||||||
с двумя – азины (альдазины или кетазины)
2R |
|
C |
|
R' + H2N |
|
NH2 |
|
R |
|
C |
|
N |
|
N |
|
C |
|
R + 2H2O |
|||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
O |
|
|
|
|
|
|
|
R' |
|
|
|
|
|
R' |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
кетазин |
||||||||
нагреванием гидразонов с твѐрдым КОН получают насыщенные углеводороды.
|
|
|
|
|
|
|
|
|
|
|
H |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
C |
|
N |
|
NH2 |
|
R |
|
С |
|
H + N2 |
||
|
||||||||||||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|||||||||
|
||||||||||||||
|
|
|
|
|
|
|
|
|||||||
|
|
R' |
|
|
|
R' |
||||||||
|
|
|
|
|
|
|
|
130 |
|
|
|
|
|
|
