
Uchebnik
.pdf
При наличии в растениях многих типов флавоноидных молекул одновременно, оптимальную экстракцию осуществляют 70-80% метанолом; экстракт концентрируют до небольшого объема и проводят последовательную обработку хлороформом (или бензолом), этилацетатом и каждую из полученных фракций исследуют методом двумерной бумажной хроматографии на наличие флавонов, флавонолов, флаван-3-олов, флаван-3,4-диолов и их гликозидов.
Если в сырье обнаружены антоцианы, их отделяют обработкой 1%
метанольным раствором НСl либо в метанольный экстракт пропускают ток сухого хлороводорода. Затем экстракт разбавляют 1:3 водой и проводят экстрагирование изоамиловым спиртом. Как правило, антоцианы на хроматограммах окрашены в красный цвет. Более 3-х антоцианов в экстракте успешно разделяют препаративно на бумаге или на колонках с целлюлозой.
Флавон-С-гликозиды, галактозиды и ксилозиды, замещенные по 6- и 8-
или по 6,8-положениям, а также моно-, ди- и тригликозиды разделяют в системе этилацетат - пиридин - вода - метанол 80:12:10:5, при этом 6- и 8-С- глюкозиды имеют Rf 0.44 и 0.63; 6- и 8-С-галактозиды - 0.32 и 0.46; 6- и 8-С- ксилозиды - 0.62 и 0.70, 6,8-С-диглюкозид – 0.62 и 0.70; 6,8-С-диглюкозид –
0.11; 6,8-ди-С-ксилозид - 0.30, 6-С-ксилозил-8-С-глюкозид - 0.19.
Изофлавоноиды делят в системе хлороформ - метанол 4:1, флаваноны - бензол-уксусная кислота-вода 125:72:3, хлороформ - уксусная кислота - вода 2:1:1 и бензол - пиридин - муравьиная кислота 6:9:5, дигидрофлавонолы - хлороформ-метанол-уксусная кислота 7:1:1, халконы и ауроны в системе: бензол - этилацетат - муравьиная кислота 9:7:4, хлороформ - этилацетат - муравьиная кислота 6:3:1, толуол - этилацетат - муравьиная кислота 5:4:1, антоцианидины и антоцианины: этилацетат - муравьиная кислота - 2н НСl или этилацетат - бутанол - муравьиная кислота - вода 5:3:3:1.
Птерокарпаны и изофлавоны разделяют на силикагеле Меrск-60 в системах бензол - этилацетат - метанол - петролейный эфир 6:4:1:6 или хлороформ - метанол 8:2.
Разделение катехинов и отделение их от полимеров проводят на силикагеле, а из водных растворов - на кожном порошке, десорбируя катехины эфиром и этилацетатом, а полимеры катехинов - ацетоном и 50% ацетоном.
Разделение антоцианов возможно на силикагеле или целлюлозе с использованием в качестве элюентов и растворителей БУВ 4:1:5 или препаративно на бумаге в этой же подвижной фазе.
Разделения, основанные на адсорбции, успешно использованы для большинства групп флавоноидов. Например, разделение антоцианов на G-25 в 60% водном этаноле, в водном ацетоне с добавлением кислоты, на LH-20 в подкисленном метаноле, флавоновых и флавоноловых гликозидов на G-10 с использованием смеси метанол - вода 1:1, изофлавонов на G-25 в 0.1M гидроксиде аммония, катехинов, процианидиновых димeров и процианидиновых агликонов на LH-20 в этаноле или смеси его с пропанолом 1:1 и широкий набор флавоноидов и их гликозидов на LН-20 в метаноле.
442
Примером успешного применения ВЭЖХ может служить исследование интенсивно окрашенных экстрактов чашелистников Poinsettia на колонках с µ- Бондапаком С18 и Лихросорбом RР18 в режиме изократического и градиентного элюирования смеси 2% уксусная кислота - ацетонитрил или 2% уксусная кислота – тетрагидрофуран или на основе триацетата целлюлозы на СГ-диоле с использованием в качестве элюентов гексан - изопропиловый спирт 9:1 или метанол при повышении его содержания от 20% до 60% в течение 20 минут (УФ-детектор, 295 нм).
Эффективное разделение достигается на колонке с Нуклеосилом 100-С18 в двух вариантах: - градиентное элюирование смесью метанол - тетрагидрофуран
– 0.5% фосфорная кислота переменного состава от 22.5:22.5:55 до 30:30:40 с УФ-детектором на 340 нм или элюирование смесями, состав которых в течение 30 минут меняется: изопропиловый спирт - тетрагидрофуран 25:65 с ацетонитрилом и 0.5% фосфорной кислотой 15:15:83.5 до 0:78:75 с УФдетектором 254 и 350 нм, на колонке с Реll ODS и с Нуклеосилом С18 при 320С при градиентном элюировании смесью уксусная кислота - вода 10:90 - 82:18 в течение 47 минут и от 82:18 до 100:0 за 8 минут (УФ-детектор 277 нм).
Анализ катехинов проходит в условиях нормального фазового процесса с использованием колонки с Лихросфером 100-СN (5 мкм) и подвижной фазы н- гексан - этилацетат 55:45 с УФ-детектором 278 нм.
Для антоцианидинов пригоден µ-Бондапак С18 с использованием элюента вода -уксусная кислота - метанол 71:10:19, для антоцианов - Лихросорб RP18 с использованием 1.5% фосфорной, 20% уксусной кислот и 25% раствора ацетонитрила в воде, для флавонов и флавонолов - µ-Бондапак - этанол-вода- уксусная кислота 650:1:350, для бифлавоноидов - Меркосорб S-160 с 8% раствором метанола в диизопропиловом эфире, для флавонол-гликозидов - µ- Бондапак С18 - 2% уксусная кислота и тетрагидрофуран (градиент), для изофлавоноидов - Порасил - 3 части смеси дихлорметан - этанол - уксусная кислота 485:15:1 и 22 части гексана, для метилированных флавонов - Лихросорб 81-60 с гептан - этанолом 3:1, для проантоцианидинов - Лихросорб RP8 с использованием смеси воды с метанолом.
Использование обращенно-фазовой высокоэффективной ТCХ на силикагеле пригодно для разделения флавоноидов и отделения их от фенолокарбоновых кислот, причем полученная картина разделения принципиально отличается от характерной для обычной ТСХ.
Для разделения гликозидов флавоноидов на препаративном уровне (от нескольких мг до нескольких грамм) предложена капельная противоточная хроматография.
Доступны компьютерные варианты сочетания 2-3 методов анализа, разделения и идентификации веществ одновременно из одной аналитической пробы, например: хромато-масс-спектрометрия, хромато-УФ-, хромато-ИК-, хромато-УФ-ПМР- и т.д. Описано быстрое разделение полиметоксифлавонов методом сверхкритической флюидной хроматографии, ВЭЖХ и аффинной хроматографии.
443
Вопросы для самоконтроля студентов
1Классифицируйте флавоноидные молекулы.
2Приведите примеры влияния степени окисленности гетерокольца на свойства флавоноидов.
3Выявите взаимосвязь характера сочленения ароматических колец и их реакционной способности.
4Сравните зависимость реакционной способности флавоноидов от природы и взаимного расположения заместителей.
5Опишите строение и свойства флавоноидных алкалоидов.
6Укажите основные фармакофорные группы молекул флавоноидов.
7Составьте общую схему выделения флавоноидов.
8Сравните возможности хроматографических методов в разделении флавоноидных молекул.
9Сравните различные электрохимические методы исследования флавоноидных молекул.
10Назовите основные промышленно-важные флавоноиды.
Химические свойства флавоноидов
Все типы флавоноидных молекул относятся к полифенольным соединениям и, не смотря на различия структур, общие химические свойства
различных групп флавоноидов определяются свойствами ароматических
колец А и В, функциональными группами в них, степенью окисленности трехуглеродного звена С2-3-4. Так, общими химическими свойствами являются:
реакции электрофильного замещения в ароматических кольцах А и В. При этом необходимо учитывать различный характер их конденсации и, связанную с этим, различную реакционную способность (галогенирование, нитрование, сульфирование, диазотирование и др.);
реакции конденсации с образованием С-С и С-О-С связей;
ОН-группы в кольцах А и В являются фенольными и могут участвовать
вреакциях электрофильного замещения протона ОН-группы или нуклеофильного обмена ОН-групп; в зависимости от расположения, ОН-группы могут быть
связаны внутримолекулярной водородной связью, что сказывается на их реакционной способности;
3-ОН группа отличается от ОН-групп колец;
реакции направленного присоединения по С=О группе и нуклеофильного обмена кислорода карбонильной группы;
реакции направленного присоединения по двойной связи – С2=С3 С=О и (или) по двум двойным связям (восстановление);
реакции комплексообразования с участием ОН и С=О-групп.
Мерой реакционной способности ОН-групп флавоноидов могут служить константы их кислотности, отражающие степень поляризации связей О Н. Кислотные свойства находятся во взаимосвязи с их основностью, связанной с
444
наличием нуклеофильных центров в пирановом фрагменте. Ниже приведены химические реакции для идентификации различных флавоноидов в присутствии родственных соединений:
№ |
Реагент |
Спектральный |
Цвет |
Группа соединений |
|
|
диапазон |
|
|
|
|
видимая |
оранжевый, фукси- |
антоцианы,бетацианы |
|
|
область |
новый, розовато- |
|
|
|
|
лиловый |
|
|
|
|
ярко-желтый |
халконы, ауроны |
|
|
|
бледно-желтый |
флавоны, ксантоны, |
|
|
|
|
антрахиноны |
|
|
УФ, 254 нм |
темные пятна на |
флавоны, изофлаво- |
|
|
|
флуоресцирующем |
ны, простые фенолы |
|
|
|
фоне |
|
|
|
УФ, 300 нм |
бледно- |
флавоны, флавонол- |
|
|
|
коричневый |
3-гликозиды |
|
|
|
абрикосовый |
ксантоны |
|
|
|
ярко-желтый |
флавонолы |
|
|
|
желто-зеленая |
флавоны без 5-ОН- |
|
|
|
флуоресценция |
группы |
|
|
|
голубая |
3,5-диметоксифлаво- |
|
|
|
флуоресценция |
нолы, кумарины, |
|
|
|
|
коричные кислоты |
1 |
Пары NH3, 2н |
УФ, 300 нм |
изменение цвета |
большинство фено- |
|
или 5% вод- |
|
|
лов, фенолокислот, |
|
ный раствор |
|
|
флавоноидов, кроме |
|
Na2CO3 |
|
|
изофлавонов |
|
|
|
появление синей |
флороглюцин, п- |
|
|
|
окраски |
кумаровая кислота и |
|
|
|
|
подобные соединения |
|
|
|
исчезновение |
метилированные |
|
|
|
синей окраски |
коричные кислоты |
|
|
|
флуоресценция |
кумарины и |
|
|
|
|
подобные соединения |
|
|
видимый |
желтый |
флавоны, флавононы, |
|
|
свет |
|
флавонолы |
|
|
|
красный |
антрахиноны |
|
|
|
оранжево-красный |
халконы, ауроны |
|
* Нуклеофильность карбонильной группы в реакциях замещения у |
|||
флавонов и флавонолов понижена, однако взаимодействие с аммиаком проходит без нагревания, при этом образуются имины желтого цвета:
445

HO |
O |
OH |
|
HO |
O |
OH |
|
HO |
O |
OH |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
NH3 |
|
|
|
|
|
|
|||
OH O |
|
|
|
OH OH |
NH2 |
|
|
- HOH |
|
OH NH |
|
|
|
|
|
|
|
|
|||
* При нагревании спиртового раствора мирицетина с концентрированным раствором аммиака возможно раскрытие пиранового кольца с образованием
3,4,5,2’,4’,6’-гексаокси- -оксихалкона и 1-(2,4,6-триоксифенил)-3-(3,4,5-три-
оксифенил)пропан-1,2-диона с общим выходом двух названных продуктов 86%. Структура дикетона доказана по реакции с о-диаминобензолом:
2 FeCl3/K3Fe(CN)6 |
видимая |
синий, сине- |
все фенольные |
|
область |
фиолетовый |
соединения и |
|
|
|
флавоноиды |
|
|
зеленый |
флавоноиды со |
|
|
|
свободной 5-ОН, |
|
|
|
мета-ОН других |
|
|
|
полифенолов |
|
|
коричневый |
флавонолы со |
|
|
|
свободной 3-ОН, |
|
|
|
карбоновые |
|
|
|
кислоты |
* Оттенок окраски зависит от числа и расположения ОН-групп. Однако, при различном расположении ОН-групп в кольцах А и В, оттенок не может быть однозначным доказательством их расположения. Например, в структуре мирицетина в кольце А – мета-ОН, в кольце В – три орто-ОН. Суммарный цвет раствора является наложением двух оттенков.
446

3 |
Диазотированные |
видимая |
желтый, |
флавоноиды и боль- |
|
п-нитроанилин или |
область |
коричневый |
шинство фенольных |
|
сульфаниловая |
|
или красный |
соединений со |
|
кислота |
|
|
свободными о-, п- |
|
|
|
|
положениями, отно- |
|
|
|
|
сительно ОН-групп, |
4 |
Свежеприготовленный |
видимая |
оранжево- |
сразу – 7-оксифлаво- |
|
раствор диазотирован- |
область |
красный |
ны, 7-оксифлавоно- |
|
ного сульфаниламида |
|
|
лы и 7-оксиизо- |
|
(1 мл 0.5% р-ра белого |
|
|
флавоны |
|
стрептоцида в 10% |
|
|
через 1-2 минуты – |
|
серной кислоте + 0.2% |
|
|
7-оксифлаваноны, |
|
р-р нитрита натрия) + |
|
|
7-гликозиды после |
|
10% р-р щелочи |
|
|
гидролиза в парах |
|
|
|
|
25% горячей HCl |
5 |
Аммиачный раствор |
видимая |
коричневый, |
о-диоксигруппи- |
|
азотнокислого серебра |
область |
черный |
ровки флавоноидов |
|
|
|
|
и др. полифенолов, |
|
|
|
|
кислоты |
6 |
Молибдат натрия |
видимая |
желтый |
о-диоксигруппи- |
|
|
область |
|
ровки флавоноидов |
|
|
|
|
и др. полифенолов, |
|
|
|
|
кислоты |
* Комплексы с молибденом особенно устойчивы по 3-ОН группе:
7 |
1% ванилин в |
видимая |
красно- |
флороглюцин и его |
|
конц. HCl |
область |
фиолетовый |
фрагменты в |
|
(р.Запрометова) |
|
|
структурах флаво- |
|
или H2SO4 |
|
|
ноидов (катехины, |
|
|
|
|
конденсированные |
|
|
|
|
дубильные |
|
|
|
|
вещества) |
|
|
|
бледно-розовый |
пирокатехин и его |
|
|
|
(после нагревания) |
фрагменты в струк- |
|
|
|
|
турах флавоноидов |
|
|
|
малиновый |
флаван-3,4-диолы |
447

|
красный или |
димеры |
|
оранжевый (после |
флавоноидов |
|
нагревания при |
|
|
1050С) |
|
|
ярко-желтый |
флавоны, |
|
|
флавонолы |
|
розовый |
эфиры катехинов |
|
ярко красный |
галлокатехины |
* Цвет определяют окрашенные ионы карбония:
8 |
1% NaBH4 в |
|
|
видимая |
|
красный |
|
|
|
флаваноны и |
|
|||||
|
этиловом или |
|
|
область |
|
|
|
|
|
|
|
изофлаваноны |
|
|||
|
изопропиловом |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
спирте + AlCl3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
9 |
2,4,5-тринитро- |
|
|
видимая |
|
красный |
|
|
|
катехины |
|
|||||
|
фенол в С2Н5ОН/ |
|
|
область |
|
|
|
|
|
|
|
|
|
|
||
|
этанольный |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
раствор КОН |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
1-3% раствор AlCl3 |
|
|
видимая |
|
от бледно-желтой |
|
|
флавоны, |
|
||||||
|
в спирте |
|
|
область |
|
до желтой |
|
|
|
флавонолы, |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
халконы, ауроны |
||
|
|
|
|
|
УФ, 254 нм |
|
желто-коричневый |
|
|
флавоны |
|
|||||
|
|
|
|
|
|
|
|
желтый |
|
|
|
халконы |
|
|||
|
|
|
|
|
|
|
|
желто-зеленый |
|
|
|
флавонолы |
|
|||
|
|
|
|
|
|
|
|
зеленый |
|
|
|
ауроны |
|
|
||
11 |
5% раствор AlCl3 и |
|
|
УФ, 254 нм |
|
красный |
|
|
|
халконы |
|
|||||
|
пары NH3 |
|
|
|
|
|
коричнево-желтый |
|
|
изофлавоны |
|
|||||
|
|
|
|
|
|
|
|
оранжевый |
|
|
|
ауроны |
OH |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
O |
|
|
O |
|
|
Cl |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
Al Cl |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
OH |
|
|
|
OH |
|
|
|
OR |
|
Cl |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
||||
OH |
O |
O |
|
|
OH |
O |
|
|
|
|
|
|||||
|
Cl |
|
OR |
O |
|
|
||||||||||
Al |
|
|
|
|
||||||||||||
|
Al |
|
|
|
|
|
|
|
|
|
|
|||||
Cl |
Cl |
|
|
Cl |
Cl |
|
Cl |
Al |
Cl |
|
|
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
Cl |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* Устойчивость продуктов реакции при добавлении HCl – различна и это свойство используется для идентификации характера гидроксилирования колец А, В и С.
448

12 |
Реактив |
видимая |
оранжевый или |
флавоны, |
|
|
|
Мартини- |
область |
желтый |
флавонолы |
|
|
|
Беттоло (насыщ. |
|
желтый |
флаваноны, |
|
|
|
раствор SbCl3 в |
|
|
|
изофлавоны |
|
|
CCl4) |
|
красный или |
халконы |
|
|
|
|
|
красно- |
|
|
|
|
|
|
фиолетовый |
|
|
|
|
|
|
зеленый, переходя- |
каротиноиды |
|
|
|
|
|
щий в синий |
|
|
|
|
|
|
зелено-бурый |
тритерпеноиды |
|
|
|
* Структуры аналогичны образующимся от действия AlCl3. |
|
||||
|
|
|
|
|
|
|
13 |
5% раствор |
УФ, 254 нм |
желтый |
|
флавоны, флаво- |
|
|
ацетата магния в |
|
|
|
нолы, халконы, |
|
|
метаноле |
|
|
|
изофлавоны |
|
|
|
|
голубой |
|
флаваноны |
|
|
|
|
розовый, красный |
|
антрахиноны |
|
14 |
Реактив Димрота |
УФ, 254 нм |
желтый, |
|
5-оксифлавонолы и |
|
|
(насыщ. р-р |
|
оранжевый |
|
их метиловые эфиры |
|
|
H3BO3 в уксусном |
|
|
|
|
|
|
ангидриде), 100- |
|
|
|
|
|
|
1100 |
|
|
|
|
|
|
3-5% водные |
Видимый |
белый или |
|
все флавоноиды и |
|
|
растворы борной |
свет |
желтоватый |
|
др. полифенолы с |
|
|
кислоты |
|
осадок |
|
орто-диокси- |
|
|
|
|
|
|
группировкой |
|
|
раствор борной |
|
желтый |
|
5-оксифлавоны |
|
|
кислоты в ацетоне |
|
|
|
|
|
|
Реакция идет по орто-ди(три) |
оксигруппировке или при наличии сочетания |
|
|||
ОН и С=О групп: |
|
|
|
|
|
|
* Добавление лимонной кислоты усиливает окраску растворов или осадков.
15 2% раствор хлор- |
видимая |
желтый |
5-оксифлавоны и |
окиси циркония в |
область |
|
5-оксифлавонолы |
метаноле |
УФ, 254 нм |
зеленый |
5-оксифлавонолы |
(р.Хорхаммера и |
|
(флуоресценция) |
|
Миллера) |
|
|
|
* При добавлении лимонной кислоты комплекс по 5-ОН группе разрушается, что можно использовать для идентификации 3- и 5-ОН групп:
449
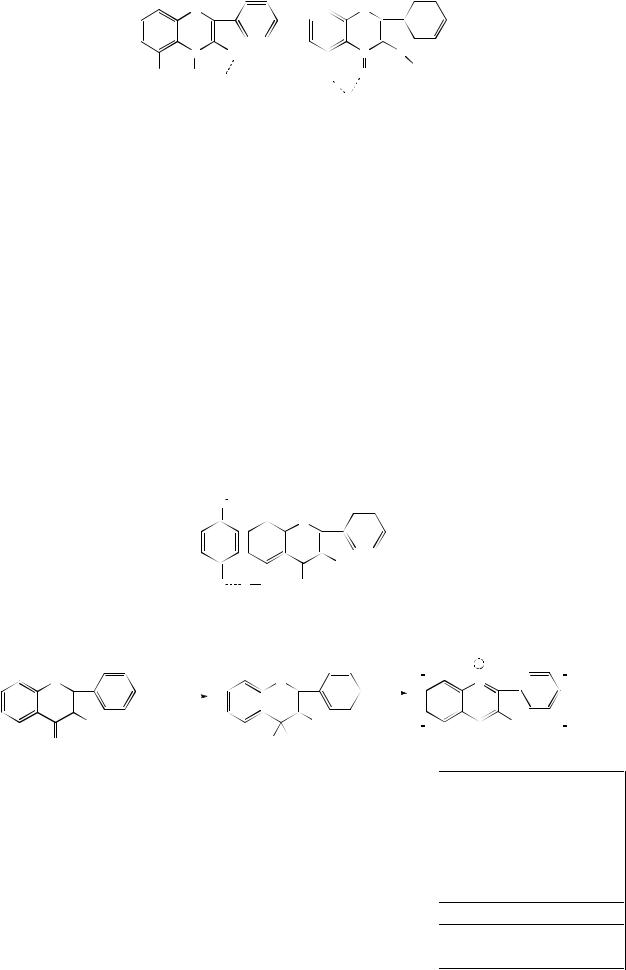
16 |
Цинк в 18% |
видимая |
красный, ярко- |
флавоны, |
|
растворе HCl |
область |
оранжевый |
дигидрофлавонолы |
|
|
|
розовый |
флавонолы, флава- |
|
|
|
|
нонолы, 3-глико- |
|
|
|
|
зиды флавонов |
17 |
1% водный раствор |
видимая |
зеленый |
дубильные вещес- |
|
железоаммониевых |
область |
|
тва с пирокатехи- |
|
квасцов (ЖАК) |
|
|
новым фрагментом |
|
|
|
темные оттенки до |
дубильные вещес- |
|
|
|
черного |
тва с пирогалло- |
|
|
|
|
вым фрагментом |
|
|
|
серые оттенки до |
фенолокислоты |
|
|
|
серо-фиолетового |
|
18 |
2% раствор п- |
видимая |
красный |
5,8-диоксизаме- |
|
бензохинона в |
область |
|
щенные флавоно- |
|
спирте («госсипе- |
|
|
иды с п-диокси- |
|
тиновая проба») |
|
|
замещением |
19 |
Mg/HCl конц. |
видимый |
красный, |
флавоны, флаво- |
||||||||||
|
(«цианидиновая |
|
свет |
оранжевый |
нолы, флаваноны |
|||||||||
|
проба») |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
20 |
1% свинца ацетат |
видимый |
красный осадок |
флавонолы |
|
основной |
свет |
желтый |
флавоны |
|
2% свинца ацетат |
|
ярко-желтый |
флавоны, халконы, |
|
средний |
|
|
ауроны, флавонолы с |
|
|
|
|
о-диоксигруппи- |
|
|
|
|
ровкой |
|
|
|
красный, синий |
антоцианы |
|
10% свинца |
|
осадок |
дубильные вещества |
|
ацетат |
|
|
|
|
|
|
450 |
|

 6,8-дигликозиды
6,8-дигликозиды  6-, 8- моногликозиды
6-, 8- моногликозиды