
Uchebnik
.pdf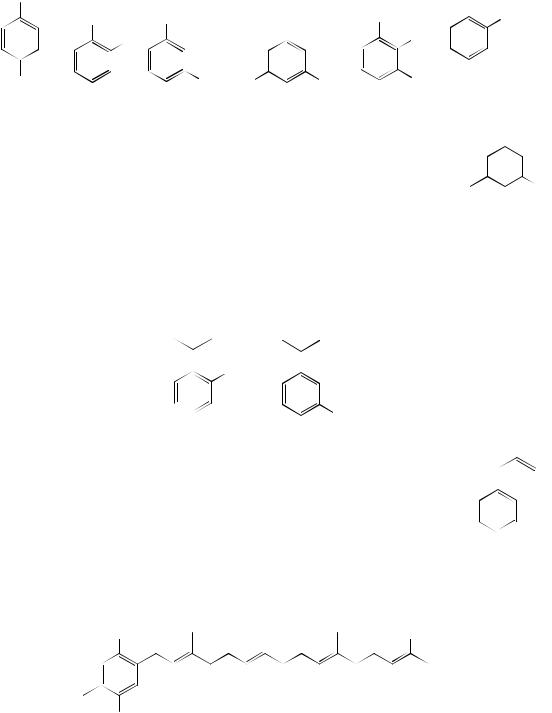
Как правило, перечисленные группы веществ в различных сочетаниях, содержатся в составе практически всех растений и являются действующими веществами более 70% лекарственных средств растительного происхождения.
Фенолы
Все содержащиеся в лекарственных растениях фенолы образуются из углеводов, продуктов их превращения и из оксибензойных и оксикоричных кислот. По числу ОН-групп определяется атомность фенолов. В растениях преобладают 2-х и 3-х атомные фенолы:
OH |
|
|
|
|
|
|
OH |
|
OH |
OH |
|
OH |
OH |
|
OH |
|
OH |
|
|
|
|
OH |
|
OH |
пиро- |
OH |
HO |
OH |
пиро- |
OH |
OH |
гидро- |
резорцин |
флороглюцин |
|
оксигидро- |
|||
хинон |
катехин |
|
|
|
галлол |
хинон |
|
Гомолог резорцина, орсин входит в состав многих лишайников и отличается от резорцина по окраске с хлороформным раствором КОН (красный желтый с зеленой флуоресценцией).
Фенол найден в хвое сосны, в листьях черной смородины, пирокатехин – в листьях тополя бальзамического и бадана толстолистного, в эпидермисе лука, флороглюцин – в гравилате, шишках секвойи, кожуре цитрусовых; гидрохинон и его глюкозид - арбутин содержатся в коре, листьях, семенах груши, в листьях толокнянки и др. растений. Тимол и карвакрол – компоненты эфирных масел, используются в медицине в качестве антисептиков:
Хавикол содержится в маслах различных растений и используется для полосканий горла и ран. Метиловый эфир хавикола, эстрагол и в его изомер, анетол содержатся в анисовом, укропном и других эфирных маслах и
используются в виноделии и парфюмерии. |
OH |
К простейшим фенольным соединениям относят также пренилированные |
|
производные – убихиноны, пластохиноны, |
токоферолы, комбовая кислота из |
семян Pycnanthus kombo: |
|
OH |
COOH |
OH
361

Токсичное начало сумаха Toxicodendron radicans, урушиол – смесь производных пирокатехина содержится, также, в млечном соке лаковых деревьев Rhus vernicifera (Япония):
R = (CH2)14CH3
(CH2)7CH=CH(CH2)5CH3
(CH2)7CH=CH-CH2(CH=CH)2CH3
(CH2)7(CH=CH-CH2)2CH=CH2
Урушиол входит также в состав действующего начала ядовитого плюща.
Из лекарственного растения Ardisia japonica (Myrsinaceae), используемого в китайской медицине для лечения туберкулеза и астмы, выделен ардизинол:
Эффективные антиоксиданты, проявляющие, кроме того, протекторную активность при поражении печени канцерогенами описаны из коры Betula рlatyphylla, например, бетулаплатозиды состава:
Широко представлены в растениях токоферолы, особенно состава: R=R’=CH3
R=CH3; R’=H
R=H; R’=CH3 R=R’=H
Более сложное строение фенола имеет галлюциногенное начало конопли Cannaвis sativa, тетрагидроканнабинол состава:
Из печеночника Мastigophoria diclados выделено два оптических изомера, активирующих рост нервных тканей, мастигофорены А и В:
362

Среди природных фенолов описаны Cl, Br, I – производные, продуцируемые грибами, водорослями, лишайниками, микроорганизмами. Например, 2,4-дихлорфенол выделен из почвенного гриба Penicilliиm sp., половой гормон 2,6-дихлорфенол обнаружен у нескольких видов кровососущих паразитов, грибы Drosophille содержат дрософиллин А (2,3,5,6-тетрахлор-4- метоксифенол).
Бромсодержащие фенолы впервые были описаны в составе красных и бурых водорослей, например, бромкатехол, ланосол и др.:
R1=R3=Н, R2=Вr, R4=CHО, R5= Cl, R6=ОH - бромкатехол
R1=R5=Н, R2=R3= Вr, R4=CH2ОH, R6=ОH - ланосол
R1=R5=Н, R2=R3=Вr, R4=CH2ОCH3, R6=ОH - метилат ланосола
Хлорфенолы образуются в результате действия ферментов (галопероксиды) в грибах, лишайниках и растениях; бромфенолы, особенно дифенилметанового типа, например, телефенол (обладающий противогрибковой активностью) – морскими растениями и микроорганизмами. Красные и зеленые водоросли продуцируют метаболиты:
В отличие от дифенилметанов, дифениловые эфиры обнаружены в морских губках, бурых и красных водорослях:
363

Во многих красных водорослях содержится необычный сульфат бром-
содержащего фенола: R1=SO3K, R1=R3=Вr, R4=СH2OSO3K, R5=H, R6=ОH.
Все фенолы, как кислоты, растворимы в воде и водно-органических смесях, спиртах, ацетоне, поэтому фенолы, совместно с родственными соединениями, извлекают из сырья экстракцией водой или низко-
процентными водно-спиртовыми растворами.
Пренилированные фенолы и С-С (С-О-С)- фенольные димеры и тримеры, встречающиеся в ряде растений, извлекают спиртами или чаще 70-90% водноспиртовыми и 50% водно-ацетоновыми растворами.
Для выделения С-С и С-О-С фенольных димеров воздушно-сухое сырье экстрагируют кипящим метанолом. Сконцентрированный досуха в мягких условиях метанольный экстракт растворяют в воде очищенной и последовательно фракционируют н-гексаном, хлороформом, этилацетатом и н- бутанолом. Хлороформную фракцию наносят на колонку с силикагелем и элюируют сначала бензолом, затем смесью бензол-этилацетат с увеличением содержания последнего. Фракции, элюированные смесью состава (17:3 и 13:7) по отдельности препаративно рехроматографируют методом ВЭЖХ (80% СН3СN). Хроматографирование бутанольного экстракта осуществляют на колонке с сефадексом LH-20, элюируя водным метанолом (0-100%). Фракцию, элюированную 20% водным метанолом рехроматографируют на колонке с RP18 сорбентом и подвижной фазой 40-50% водный метанол.
Для выделения простых пренилированных фенолов воздушно-сухое сырье последовательно экстрагируют петролейным эфиром и ацетоном. Ацетоновый экстракт исчерпывающе экстрагируют хлороформом. Хлороформный экстракт концентрируют досуха в мягких условиях, обезжиривают действием гексана и наносят на колонку с силикагелем СС. Компоненты экстракта элюируют с колонки хлороформом и ацетоном. Первую хлороформную фракцию препаративно разделяют методом ТСХ в системе: петролейный эфирхлороформ (3:1), последующие хлороформные фракции делят в системе хлороформ-этилацетат (4:1). Препаративное выделение веществ ацетоновых фракций осуществляют в системе: пропанол-2 – хлороформ (1:25).
Качественных реакций, селективных для фенолов не существует, поскольку родственные соединения извлекаются вместе с фенолами, поэтому к водно-спиртовому (10-30%) извлечению:
364
Добавляют 1-3 капли бромтимолового голубого, появляется желтое окрашивание на голубом фоне (фенолокислоты, фенолы, полифенолы).
Добавляют 1-3 капли бромкрезолового зеленого, появляется желтое окрашивание на зеленом или сине-зеленом фоне (фенолокислоты, фенолы).
Добавляют 1-2 мл 2% раствора свинца ацетата основного, появляется осадок или окрашивание: желтое или оранжевое (фенолы, фенолокислоты,
полифенолы, дубильные вещества).
Реакция Робертса-Вуда. Добавляют 1-5 капель 0.2 % раствора квасцов железоаммониевых, появляется зеленое окрашивание (орто-диоксигруппировка любых фенольных соединений); серо-синее до фиолетового окрашивание (три рядовых ОН-группы любых фенольных соединений).
Реакция Запрометова. Добавляют 1-3 капли 1% раствора ванилина в кислоте хлороводородной концентрированной, появляются оттенки красного цвета (мета-диоксигруппировка любых фенольных соединений).
Добавляют 1-3 мл 1-5% раствора железа хлорида (III), появляется различное окрашивание зеленых, синих, фиолетовых оттенков (любые фенольные соединения, кроме тимола).
Добавляют кристаллик сульфата железа закисного, появляется сиреневое, затем темно-фиолетовое окрашивание, а затем темно-фиолетовый осадок
(флороглюцины).
Добавляют 3-5 капель раствора 1% железа окисного хлорида и 3-5 капель 1% раствора калия ферроцианида, появляется темно-зеленое окрашивание. При добавлении 3-5 капель раствора кислоты азотной концентрированной, появляется темно-бурое окрашивание (фенолы, полифенолы).
Добавляют 2-3 капли реактива Паули по Кутачеку (3 г сульфаниламида растворяют в 200 мл воды, добавляют 6 мл конц. HCl и 14 мл н-бутилового
спирта. Перед употреблением 20 мл этого раствора смешивают с 0.3 г натрия нитрита), появляется вишнево-красное окрашивание, переходящее в оранжевое
(флороглюциды, арбутин).
Реакция Либермана. Добавляют 1-2 мл кислоты хлороводородной концентрированной и 1-2 мл 10% раствора натрия нитрита, появляется
меняющееся окрашивание: оранжево-желтое оранжево-красное кровавокрасное с зеленым оттенком смородиново-красное (двух- и трехатомные фенолы, производные салициловой кислоты).
Добавляют 2 мл аммиака концентрированного, 1 мл 10% раствора натрия фосфорномолибденового в 10% кислоте хлороводородной, появляется синее окрашивание (арбутин).
Хроматографический анализ фенольных соединений растений может быть осуществлен на бумаге или в тонком слое и приборными методами: ГЖХ, ЖЖХ, ВЭЖХ. Для исследования «первого» общего экстракта растений, обычно содержащего большое количество компонентов различной природы, когда исследователю еще не известен даже предположительный состав объекта исследования, можно использовать несколько общих для фенолов хроматографических систем. Так, в методе хроматографии на бумаге, хорошо
365
зарекомендовали себя: н-бутанол – уксусная кислота – вода (40:12:29 и 4:1:5 органический слой); 2, 6 или 15% уксусная кислота; фенол, насыщенный водой; этилацетат, насыщенный водой.
Для ВЭЖХ хроматографии, в случае исследования общих полифенольных экстрактов растений, разработана следующая система: колонка с YMC-Pack ODS-AP сорбентом и подвижной фазой ацетонитрил-вода (4:1), УФ детектор при длинах волн 254 и 276 нм. Другой оригинальной хроматографической системой, предназначенной для препаративного выделения веществ общих экстрактов является: колонка с LiChrosorb Si-60 и хлороформ-метанол (9:1) в качестве подвижной фазы, с использованием фотодиодного детектора.
Общие химические свойства фенолов описаны в учебниках «Органическая химия», а специфические свойства фенолов растений обусловлены, в первую очередь, способностью их окисления до соответствующих хинонов или подобных им соединений.
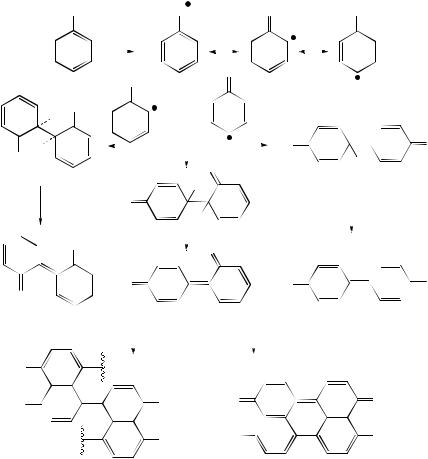
Окисление фенолов протекает по радикальному механизму, поэтому они обладают определенным сродством к свободным радикалам и выполняют роль ловушек свободно-радикальных частиц, в том числе кислорода. Отдавая атом водорода от гидроксильной группы, они образуют радикал С6Н5О•, который обрывает радикальную цепную реакцию, выполняя, роль антиоксиданта и гасителя других радикальных процессов, которые обычно приводят к явлениям, ускоряющим гибель клеток (старение) и мутагенным эффектам. Последующее окислительное дегидрирование приводит к образованию меланинов А, В и С:
|
OH |
[O] |
|
|
O |
|
|
|
|
|
|
|
O |
|
|
O |
|
|
|||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
H O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
O H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
O |
|
|
H |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
O |
|
H |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
O |
|
|
H |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
O |
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
O |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
меланин В |
|
|
|
|
|
|
|
|
|
|
|
меланин С |
|
меланин А |
|||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
O |
|
|
|
|
|
O |
|
|
|
|
O |
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
HO |
|
|
OH |
||||||
|
|
|
|
|
|
|
D |
|
|
|
|
|
|
|
|
|
|
E |
|||||
366

Меланины (А,В,С) имеют глубокую окраску (темно-коричневые и черные),
и обнаружены в семенах Helianthus annuus и Citrullus vulgaris, в спорах Ustilago maydis, в аскомицете Daldinia concentrica.
Двухатомные фенолы окисляются аналогично:
Трехатомные фенолы преобладают в растениях, но содержатся вместе с двухатомными и ведут себя в реакциях аналогично, т.е. обменивают протон водорода – О Н и протоны ароматического кольца, особенно легко в структуре флороглюцина (согласованная ориентация 3-х ОН-групп), вступают в реакции комплексо-, хелато-, солеобразования:
Пирокатехин легко отделяется от резорцина и гидрохинона по реакции с солями свинца, которые не растворимы в большинстве растворителей:
Для выделения, идентификации и очистки фенолов используют реакцию
схлорангидридами бензойной, анисовой и толуолсульфокислотой:
Спутниками фенолов в растениях являются продукты различной степени окисления алкильной цепи – фенолоспирты, фенолоальдегиды, фенолокислоты. Например, в коре ивы содержится значительное количество салицилового спирта и салициловой кислоты, в стручках Vanille – альдегид ванилин, в клетках камбия многих растений – коричные спирты:
367

OH |
OH |
OH |
OH |
|
OH |
OH |
|
O |
O |
O |
O |
|
|
|
|
|
салициловый |
O |
OH |
OH |
OH |
спирт ванилин |
п-кумаровый |
конифериловый |
синаповый |
|
|
|
спирт |
спирт |
спирт |
Значительная противовоспалительная активность и биодоступность отличает гликозидированные формы фенолов, например, арбутин, флорин, салицин и др.:
На примере урушиола осуществлена модификация структуры:
Гваякол (монометиловый эфир) и вератрол (диметиловый эфир) пирокатехина содержатся в смолах, в продуктах разложения алкалоидов и используются в медицине при простудных заболеваниях, в терапии туберкулеза, а из гваякола в промышленности получают ванилин.
Природные эвгенол и изоэвгенол – душистые вещества гвоздики (Eиgenia) изомеризуются при нагревании с КОН:
Все фенолы вступают в реакции с диазометаном и фенилизоцианатом, а
вформе кетонов – дают оксимы, например:
368

Из нитропроизводных фенолов большое значение имеет 2,4,6-тринитро- фенол - пикриновая кислота и 2,4,6-тринитрорезорцин – стифниновая кислота, используемые как реактивы в анализе оснований и в производстве взрывчатых веществ.
В траве петрушки содержится производное  тетраоксибензола, апиол, который в щелочных
тетраоксибензола, апиол, который в щелочных 

 растворах изомеризуется в изоапиол, подобно
растворах изомеризуется в изоапиол, подобно  эвгенолу.
эвгенолу. 
Многие фенолы окрашивают раствор нитрита калия в концентрированной серной кислоте (реакция Либермана), что используется в качественном анализе:
При перегонке с Zn-пылью фенолы восстанавливаются до углеводородов соответствующего строения, что используется для установления углеродного скелета исходного фенола.
Многоатомные фенолы взаимодействуют с раствором аммиака при нагревании до 2000 и выше; а с флороглюцином – при слабом нагревании:
Простые  эфиры фенолов, как правило, обладают сильным запахом. Среди природных преобладают метиловые эфиры, например:
эфиры фенолов, как правило, обладают сильным запахом. Среди природных преобладают метиловые эфиры, например:
Анизол С6Н5-ОСН3 - жидкость с приятным запахом.
369

Димеризацией и полимеризацией фенолоспиртов, например, кониферилового, образуются лигнаны.
Структурное разнообразие лигнинов обусловлено характером связи между мономерными молекулами («голова к хвосту» или «хвост к голове»), степенью окисленности γ-углеродных атомов и т.д. В растениях они накапливаются во всех органах, находятся в растворенном виде в эфирных маслах, смолах, особенно часто встречаются в семенах сосновых, барбарисовых, сложноцветных, аралиевых, папоротниковых, например, дегидротриконифериловый спирт:
Лигнины - полимеры на основе тех же фенилпропановых (С6-С3) блоков кониферилового спирта с тем же способом соединения этих блоков между собой, причем образование полимерной структуры характеризируются бессистемностью, т.е. осуществляются разные способы соединения фрагментов и сами фрагменты, как правило, не идентичны:
Несмотря на некоторое сходство, лигнины не только разных растений, но и разных тканей одного растения, отличаются между собой.
Нейротропную активность проявляет неолигнан, американол из семян
Phyfolacca аmericana L.:
Клеточные стенки древесины хвойных пород на 20-35% состоят из лигнина. Сложность изучения строения лигнинов объясняется неоднород-
370
