
- •Таврический национальный университет
- •Лекция № 1. Водород
- •Соединения водорода
- •Литература: [1] с. 330 - 338, [2] с. 411 - 415, [3] с. 262 - 270 Лекция № 2. Элементы VII-a-подгрупы (галогены)
- •Cоединения галогенов
- •Лекция № 3. Элементы via-подгруппы
- •3.1. Кислород
- •Соединения кислорода
- •2Hso4- - 2e- h2s2o8
- •Соединения серы
- •3.3. Подгруппа селена
- •Соединения селена и теллура
- •Литература: [1] с. 359 - 383, [2] с. 425 - 435, [3] с. 297 - 328 Лекция № 4. Элементы va-подгруппы
- •Соединения азота
- •4.2. Фосфор
- •Соединения фосфора
- •4.3. Элементы подгруппы мышьяка
- •Соединения мышьяка, сурьмы и висмута
- •Литература: [1] с. 383 - 417, [2] с. 435 - 453, [3] с. 328 - 371 Лекция № 5. Элементы iva-подгруппы
- •5.1. Углерод
- •Соединения углерода
- •5.2. Кремний
- •Соединения кремния
- •5.3. Германий, олово, свинец
- •Соединения германия
- •Соединения олова
- •Соединения свинца
- •Литература: [1] с. 417 - 435, 491 - 513, [2] с. 453 - 472, [3] с. 371 - 409 Лекция № 6. Элементы iiia-подгруппы
- •Соединения бора
- •6.2. Алюминий
- •Соединения алюминия
- •6.3. Подгруппа галлия
- •Соединения элементов подгруппы галлия
- •Литература: [1] с. 608 - 619, [2] с. 472 - 481, [3] с. 412 - 446 Лекция № 7. Элементы iia-подгруппы
- •7.1. Бериллий
- •Соединения бериллия
- •7.2. Магний
- •Соединения магния
- •7.3. Щелочноземельные металлы
- •Соединения щелочноземельных металлов
- •Литература: [1] с. 587 - 599, [2] с. 481 - 486, [3] с. 447 - 460
- •7.4. Элементы ia-подгруппы (щелочные металлы)
- •Соединения щелочных металлов
- •Литература: [1] с. 543 - 551, [2] с. 486 - 489, [3] с. 461 - 470 Лекция № 8. Общая характеристика d-элементов. Элементы iiiв - vb подгрупп (подгруппы скандия,титана и ванадия)
- •8.1. Общая характеристика d-элементов
- •8.2. Элементы iiiв подгруппы (подгруппа скандия)
- •Соединения элементов подгруппы скандия
- •8.3. Элементы ivв подгруппы (подгруппа титана)
- •Соединения титана, циркония и гафния
- •8.4. Элементы vв подгруппы (подгруппа ванадия)
- •Соединения ванадия, ниобия и тантала
- •Литература: [1] с. 619 - 633, [2] с. 489 - 523, [3] с. 478 - 481, 499 - 520 Лекция № 9. Элементы viв- и viiв-подгрупп
- •9.1 Элементы viв-подгруппы (подгруппа хрома)
- •Соединения хрома, молибдена и вольфрама
- •9.2. Элементы viiв-подгруппы (подгруппа марганца)
- •Соединения маргнаца, технеция и рения
- •Литература: [1] с. 633 - 645, [2] с. 523 - 539, [3] с. 521 - 548 Лекция № 10. Элементы viiib-подгруппы
- •10.1. Элементы триады железа
- •Соединения железа
- •Соединения кобальта
- •Соединения никеля
- •Литература: [1] с. 650 - 679, [2] с. 540 - 550, [3] с. 548 - 584
- •10.2. Платиновые металлы
- •Соединения рутения и осмия
- •Соединения родия и иридия
- •Соединения палладия и платины
- •Лекция № 11. Элементы ib- и iib-подгрупп
- •11.1 Элементы ib-подгруппы (подгруппы меди)
- •Соединения меди
- •Соединения серебра
- •Соединения золота
- •11.2. Элементы iib-подгруппы (подгруппа цинка)
- •Соединения цинка и кадмия
- •Соединения ртути
- •Литература: [1] с. 551 - 563, 599 - 608, [2] с. 550 - 554, [3] с. 585 - 602 Лекция № 12. Химия f-элементов
- •12.1. Лантаниды
- •Соединения лантанидов
- •12.2. Актиниды
- •Соединения актинидов
- •Лекция № 13. Инертные газы
- •13.1. Гелий. Неон. Аргон
- •13.2. Элементы подгруппы криптона
- •Соединения криптона, ксенона и радона
- •Список рекомендуемой литературы
- •Оглавление
Литература: [1] с. 633 - 645, [2] с. 523 - 539, [3] с. 521 - 548 Лекция № 10. Элементы viiib-подгруппы
Побочная подгруппа VIII-группы периодической системы химических элементов включает 9 элементов, объединенных вместе по геометрическим соображениям, о чем можно судить по их общим электронным формулам (без учета провала электрона):

В то же время близость их электронных конфигураций к завершению d-подуровня обуславливает сходство свойств элементов данной подгруппы и их соединений. Кроме этого, внутри подгруппы наряду с вертикальной аналогией более или менее отчетливо проявляется аналогия у элементов одного периода, которые образуют триаду железа (Fe, Co, Ni), легкие платиновые металлы (Ru, Rh, Pd) и тяжелые платиновые металлы (Os, Ir, Pt). При этом сходство внутри данных семейств иногда просматривается более четко, нежели подобие в пределах группы электронных аналогов.
10.1. Элементы триады железа
Железо один из наиболее распространенных металлов земной коры (2 мол.%). Основные минералы: Fe3O4 - магнетит, Fe2O3 - гематит, Fe2O3nH2O - лимонит, FeCO3 - сидерит, FeS2 - пирит Кларк кобальта составляет 0,0015 мол.%. Кобальт образует небольшое число минералов, основным из которых является кобальтин (кобальтовый блеск) - CoAsS.
Никель - довольно распространенный элемент земной коры, его кларк составляет 0,0032 мол.%, обычно содержится в сульфидных медно-никелевых рудах. Известно несколько самостоятельных минералов, из которых наибольшим содержанием никеля отличается миллерит - NiS.
Железо и никель - серебристо-белые металлы, кобальт - блестящий белый металл с серым оттенком.
|
Свойства |
Fe |
Co |
Ni |
|
Плотность, г/см3 |
7,87 |
8,90 |
8,91 |
|
Т.пл., С |
1539 |
1492 |
1455 |
В промышленности железо и его сплавы (чугун) получают восстановлением оксидов железа оксидом углерода(II) при высоких температурах:
+ CO + CO + CO
Fe2O3 Fe3O4 FeO Fe
Очень чистое железо получают термическим разложением его пентакарбонила:
Fe(CO)5 Fe + 5CO
Кобальт и никель получают в результате ряда пирометаллургических операций из NiO и Со3О4, восстанавливая оксид чаще всего коксом.
Основная область применения железа - это использование его в виде сплавов, преимущественно, чугуна и сталей. Чугун - сплав на основе железа с содержанием углерода в виде графита и цементита (Fe3C) выше 2%. Специальные марки чугуна содержат в своем составе и другие элементы, например, ферросилиций (12-14% кремния), ферромарганец (60-90% марганца), зеркальный чугун (12% кремния, 20% марганца). Стали - сплавы железа с содержанием углерода 0,1 - 2%. По химическому составу выделяют углеродистые и легированные стали (легирующие добавки других металлов придают стали новые технологические свойства).
Основное количество кобальта и никеля идет на производство твердых сплавов и сверхтвердых металлокерамических композиций. Большое значение кобальт и никель имеют как легирующие добавки к сталям. Никель используется для изготовления коррозионно-устойчивой посуды и аппаратуры, для нанесения защитных покрытий. Мелкодисперсные кобальт и никель применяются как катализаторы процессов гидрирования и дегидрирования углеводородов.
Железо играет важную роль в жизнедеятельности животных и человека, входит в состав гемоглобина, миоглобина и в состав некоторых ферментов. Наряду с серой железо входит в состав ферредоксинов - переносчиков электронов в биохимических процессах. Катионы кобальта(III) входят в состав витамина В12, играющего важную роль в процессе образования эритроцитов.
Химические свойства железа. Железо - металл средней химической активности. В компактном состоянии в атмосфере сухого воздуха устойчиво, во влажном воздухе корродирует. Примеси сильно ускоряют данный процесс. При нагревании до температуры белого каления железо энергично окисляется кислородом:
3Fe + 2O2 = Fe3O4
При высоких температурах окисляется галогенами и серой:
t + S + S
2Fe + 3Cl2 = 2FeCl3 ; Fe FeS FeS2
С фосфором, углеродом и кремнием железо образует соединения переменного состава: Fe3P, Fe2P, FeP, Fe3Si2, FeSi, FeSi2, Fe3C.
При повышенных температурах железо окисляется парами воды и аммиака:
800 С t
3Fe + 4H2O Fe3O4 + 4H2; 4Fe + 2NH3 2Fe2N + 3H2
В ряду стандартных электродных потенциалов железо стоит левее водорода:
Fe2+ + 2e- Fe; E0 = -0,44 B
Легко растворяется в водных растворах кислот с образованием солей железа(II). Концентрированная азотная и серная кислоты на холоду железо пассивируют, при нагревании реагируют с образованием солей железа(III).
Химические свойства кобальта. По химической активности кобальт несколько уступает железу. При обычной температуре компактный кобальт устойчив к действию сухого и влажного воздуха, воды, щелочей и разбавленных растворов органических кислот. При 300 С окисляется кислородом воздуха, при нагревании взаимодействует с галогенами, серой, углеродом:
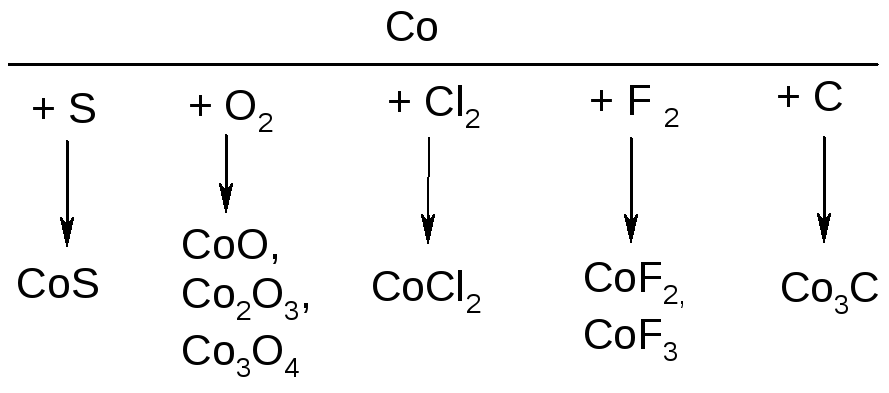
С фосфором, мышьяком, кремнием и бором образует соединения переменного состава. Не реагирует с азотом, но при нагревании до температуры красного каления реагирует с аммиаком, сероводородом и водой.
По сравнению с железом кобальт более устойчив к действию кислот, медленно растворяется в разбавленной соляной и серной кислоте, быстро - в разбавленной азотной кислоте, с образованием солей кобальта(II). Концентрированная азотная кислота кобальт пассивирует. Со щелочами кобальт практически не взаимодействует.
Химические свойства никеля. По химической активности никель уступает железу и кобальту, он не корродирует в воде, на воздухе и в различных растворах. Кислородом окисляется при температуре выше 500 С. При нагревании никель, особенно в измельченном состоянии, реагирует с галогенами и серой с образованием соответствующих бинарных соединений:
Ni + Cl2 = NiCl2; Ni + S = NiS
При высоких температурах Ni реагирует также с фосфором, углеродом, кремнием и бором с образованием соединений переменного состава (твердых растворов). При 600 С никель реагирует с водой:
Ni + H2O = NiO + H2
При незначительном нагревании взаимодействует с оксидом углерода с образованием тетракарбонила:
Ni + 4CO = Ni(CO)4
Разбавленные соляная, азотная и серная кислота медленно растворяют никель с образованием солей Ni2+. Концентрированная азотная кислота на холоду никель пассивирует. По отношению к щелочам никель устойчив.
