
4 курс / Общая токсикология (доп.) / Врожденные пороки сердца
.pdf1022 |
Часть 12. КОМПЛЕКСНЫЕ ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА |
|
|
|
|
Восходящую аорту канюлируют обычно. По лые вены канюлируют изогнутыми под прямым углом канюлями, ВПВ — возле места впадения в нее безымянной вены, НПВ — в месте кавоатри ального соединения.
Начинают искусственное кровообращение и охлаждают больного. Вокруг канюли ВПВ обжи мают тесьмой. Ниже места канюляции, на рассто янии 4–5 мм кверху от кавоатриального соустья, ВПВ пережимают сосудистым зажимом и пересе кают. Затем на сокращающемся сердце наклады вают анастомоз между головным концом ВПВ и верхней стенкой правой легочной артерии, как при выполнении ДКПА. Во время формирования этого анастомоза больного охлаждают до 22–24 0С, в результате чего наступает гипотермическая оста новка сердца. Далее пересекают легочный ствол и его проксимальный конец ушивают двурядным непрерывным швом. Сердечный конец ВПВ рас секают спереди и медиально, чтобы его диаметр соответствовал диаметру НПВ, оставляя непов режденной артерию синусового узла. В случаях, когда легочная артерия располагается сзади и справа от аорты, сердечный конец ВПВ анастомо зируют прямо к дистальной части легочного ство ла. Когда магистральные артерии располагаются нормально или легочный ствол находится слева от аорты, пересеченную часть легочной артерии ушивают непрерывным швом, а ВПВ анастомози руют с нижним краем правой легочной артерии. Для расширения соустья иногда используют ма ленькую треугольную заплату, которую вшивают в переднемедиальной плоскости.
Следующий этап операции заключается в соз дании внутрипредсердного канала, через который отводится кровь из НПВ к соустью между легоч ной артерией и кардиальным концом ВПВ. Эту часть операции выполняют в условиях кардиопле гии. Для этого пережимают восходящую аорту и вводят кардиоплегический раствор. Разрез на пра вом предсердии делают параллельно разграничи вающей борозде (рис. 17). Для создания внутрип редсердного канала может применяться различ ный материал. Он может быть сформирован из по литетрафлюороэтиленового (Gore Tex) протеза, который подшивают к окружностям мест впаде ния полых вен, или являться комбинацией запла ты (ксеноперикард, Gore Tex, аутоперикард) со стенкой венозного синуса. Мы предпочитаем ис пользовать заплату из аутоперикарда, обработан ную 1% раствором глютаральдегида, или заплату из политетрафлюороэтилена.
При создании канала с использованием запла ты измеряют расстояние между устьями полых
вен. Длина заплаты не должна превышать это рас стояние. Ширина ее должна быть такова, чтобы вместе со стенкой венозного синуса был образо ван канал диаметром 16–18 мм. Заплату подшива ют латерально вдоль crista terminalis, снизу и сверху
— к окружностям полых вен и сзади — к межпред сердной перегородке. Коронарный синус оставля ют вне внутрипредсердного туннеля, чтобы он дренировался через ДМПП в левое предсердие (см. рис. 17). После этого ушивают стенку правого предсердия, производят эвакуацию воздуха из по лостей сердца и снимают зажим с аорты.
В зависимости от патологии могут использо ваться дополнительные процедуры:
•билатеральные кавопульмональные анасто мозы;
•пластические операции на клапанах при их не достаточности или их протезирование;
•закрытие заплатой АV клапана при его недоста точности;
•создание ДМПП.
Существуют несколько альтернативных мето дик для создания полного кавопульмонального соединения. Среди них — методика, в основе ко торой лежит создание внутрипредсердного тунне ля из стенки предсердия по типу операции Senning (177, 178). Основным недостатком этой методики является большая вероятность возникновения на рушений ритма в послеоперационном периоде.
Полное кавопульмональное соединение с разгрузочным отверстием
Ранняя послеоперационная летальность после операции Fontan может быть связана с преходя щими гемодинамическими нарушениями, таки ми, как повышение сопротивления легочных со судов или дисфункция системного желудочка. Любое из этих нарушений приводит к гипертензии в системных венах. В результате высокого веноз ного давления происходит просачивание жидкос ти из капиллярного русла в интерстициальное пространство, а также в плевральные, брюшную и перикардиальную полости. Венозная гипертензия также вызывает повышение давления в лимфати ческой системе легких и застойные явления, в ре зультате чего повышается ЛСС. Кроме того, вне запное уменьшение объемной нагрузки на един ственный желудочек, которое возникает после операции Fontan, может привести к резким изме нениям геометрии желудочка (45, 141). Это вызы вает ухудшение его диастолической функции и уменьшение сердечного выброса вплоть до крити ческого (179). Применение полного кавопульмо

Глава 63. ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОРОКОВ СЕРДЦА С ФУНКЦИОНАЛЬНО ЕДИНСТВЕННЫМ ЖЕЛУДОЧКОМ |
1023 |
|
|
|
|
б
а
|
|
|
|
|
в |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
ДМПП |
|||||||
|
|
|
|
Коронарный |
||||||
|
|
|
|
|
|
|
|
|||
ВПВ |
|
|
|
|
||||||
|
|
|
|
|
|
синус |
||||
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
НПВ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
г
Легочные вены
д
Рис. 17. Этапы формирования (аñд) внутрипредсердного туннеля, соединяющего устья нижней и верхней полых вен
нального соединения с созданием разгрузочного |
Существует несколько методик создания разг |
отверстия в стенке внутрипредсердного канала |
рузочного отверстия в канале, разграничивающего |
позволяет ограничить влияние порочных меха |
кровоток по системным и легочным венам. Одна |
низмов кровообращения по Fontan на выживае |
из них предусматривает создание резидуального |
мость и раннее послеоперационное течение. |
отверстия в месте подшивания заплаты, образую |
Создание разгрузочного отверстия сохраняет |
щий туннель, к задней стенке предсердия (180). |
возможность право левого сброса крови, за счет |
Посередине линии шва, прикрепляющего заплату |
которого поддерживается сердечный выброс при |
к задней стенке предсердия, оставляют отверстие, |
ухудшении диастолической функции желудочка и |
не вовлеченное в шов. Матрацный шов с проклад |
ограничивается повышение давления в полых ве |
ками накладывают вокруг отверстия и выводят че |
нах. Умеренное снижение насыщения артериаль |
рез боковую стенку предсердия наружу. Под конт |
ной крови кислородом вследствие перемешива |
ролем зрения шов затягивают для того, чтобы про |
ния ее с венозной кровью компенсируется повы |
верить, насколько герметично он будет закрывать |
шением величины сердечного выброса. |
отверстие. Затем его отпускают и герметизируют |
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
1024 |
Часть 12. КОМПЛЕКСНЫЕ ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА |
|
|
|
|
стенку правого предсердия. Матрацный шов про пускают в длинный турникет, конец которого вы водят через белую линию живота под кожу. Таким образом можно легко регулировать величину отве рстия в раннем послеоперационном периоде.
Мы просекаем разгрузочное отверстие в стенке канала калиброванными перфораторами. Диаметр отверстия зависит от возраста больного и факторов риска. Чтобы насыщение артериальной крови было не ниже 85%, для разгрузки венозной системы дос таточно отверстия диаметром 4–6 мм. При исполь зовании аутоперикардиальной заплаты для форми рования канала ее необходимо перед употреблени ем обработать 1% раствором глютаральдегида.
Для венозной разгрузки можно использовать несколько небольших отверстий диаметром до 2 мм, созданных с помощью толстой иглы. Имеются наблюдения, что эти маленькие отверстия со вре менем самопроизвольно закрываются.
Через некоторое время при сниженном насы щении артериальной крови кислородом отверстие может быть закрыто. Это можно сделать оператив ным путем или путем катететеризации сердца с помощью специального устройства (181).
Недостатком фенестрации является повышен ный риск возникновения тромбоэмболии в сосу ды головного мозга и другие системные органы в отдаленном послеоперационном периоде.
О пользе разгрузочного отверстия свидетель ствуют снижение ранней послеоперационной ле тальности и уменьшение транссудации (182–184). Отмечено, что со временем отверстие может спон танно закрыться (184, 185). Так, у 90% пациентов с разгрузочными отверстиям диаметром 2,5 мм они закрывались спонтанно в течение первого года пос ле операции. Спонтанное закрытие фенестра диа метром 4 мм отмечается в 64% случаев (185, 186).
Некоторые хирурги используют методику час тичного отведения печеночных вен от нижней по лой вены таким образом, что одна или несколько печеночных вен остаются вне кавопульмонально го соединения и дренируются вместе с коронар ным синусом в левое предсердие (59). Однако эта методика хуже предыдущих в связи с тем, что в не которых случаях наблюдается переток венозной крови на уровне печеночных вен, в результате чего увеличивается количество сбрасываемой веноз ной крови в левое предсердие и значительно сни жается насыщение артериальной крови кислоро дом. Кроме этого, исключение попадания пече ночной крови в легкие способствует развитию ар териовенозных фистул после операции (93, 94).
Экстракардиальное полное кавопульмональное соединение
В последнее время стала популярной одна из модификаций операции Fontan в виде экстракар диального полного кавопульмонального соедине ния. Эта модификация имеет некоторые преиму щества по сравнению с ранее описанными. В част ности, экстракардиальное соединение выполняют без пережатия аорты, что предотвращает ишемию миокарда. Также исключается возможность воз действия высокого давления на стенку правого предсердия и вовлечения в шов большого количе ства тканей, в результате чего уменьшается веро ятность возникновения аритмий в послеопераци онном периоде.
Операцию выполняют из срединного доступа в условиях искусственного кровообращения. Выде ляют легочные артерии, восходящую аорту, верх нюю и нижнюю полые вены. Канюлируют восхо дящую аорту и обе полые вены. В НПВ канюлю вводят как можно ближе к диафрагме, а в ВПВ — в месте впадения левой плечеголовной вены. После перехода на искусственное кровообращение об жимают тесемки вокруг канюль на полых венах.
На сокращающемся сердце без пережатия аор ты накладывают зажим у устья ВПВ, на 4–5 мм дистальнее кавоатриального соединения. Голов ной конец ВПВ анастомозируют с правой легоч ной артерией аналогично тому, как это делают при выполнении ДКПА. Кардиальный конец ВПВ ушивают непрерывным швом. Затем накладывают зажим на основание правого предсердия, прокси мально от места его соединения с НПВ. Предсер дие пересекают ниже зажима, в результате чего ос тается часть правого предсердия в виде скошенной манжетки НПВ. Культю правого предсердия уши вают непрерывным швом ниже зажима. Продоль ным разрезом вскрывают нижнюю стенку правой легочной артерии. При наличии сужений прокси мального участка легочной артерии разрез продле вают к центру и латерально — при наличии суже ния ее дистальной части. Следующим этапом вшивают гибкий трубчатый протез. Лучше всего использовать сосудистый протез из политетраф люороэтилена диаметром 20–22 мм или аорталь ный аллографт без клапана. Конец протеза обреза ют под углом и анастомозируют «конец в конец» с НПВ непрерывным обвивным швом. Протез рас полагают так, чтобы его дуга находилась впереди верхней правой легочной вены и простиралась к разрезу правой легочной артерии. Край протеза обрезают таким образом, чтобы он соответствовал

Глава 63. ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОРОКОВ СЕРДЦА С ФУНКЦИОНАЛЬНО ЕДИНСТВЕННЫМ ЖЕЛУДОЧКОМ |
1025 |
|
|
|
|
контуру разреза на легочной артерии. При необхо димости протезом можно расширить участок су жения на ней. После наложения анастомоза меж ду протезом и правой легочной артерией проверя ют, не сдавливает ли он рядом лежащие структуры (в частности, верхнюю правую легочную вену). Из протеза эвакуируют воздух и отпускают тесемки на полых венах.
Если необходимо оставить небольшое сообще ние между протезом и правым предсердием, фор мируют прямой анастомоз (рис. 18) или их соеди няют сосудистым протезом соответствующего ди аметра (4 , 5 мм или 6 мм). Для того чтобы в пос леоперационном периоде можно было регулиро вать размеры сообщения, анастомоз, соединяю щий экстракардиальный «кондуит» и правое пред сердие, обводят лигатурной нитью, которую про водят в турникет (187).
После отключения искусственного кровообра щения в экстракардиальное кавопульмональное соединение проводят катетер для измерения дав ления. С этой же целью канюлируют левое пред сердие. После стабилизации гемодинамики изме
ряют давление в экстракардиальном кондуите. Ес ли оно ниже 15 мм рт. ст., соустье между протезом
иправым предсердием постепенно суживают под контролем давления в венозном канале. Если дав ление не превышает 15 мм рт. ст., соустье можно полностью перекрыть и удалить турникет. При по вышеном венозном давлении турникет оставляют
ивыводят наружу через нижний угол раны.
Впослеоперационном периоде всем пациентам необходимо назначать антикоагулянты для предо твращения тромбоза экстракардиального канала. Регуляция размера собщения между венозным ка налом и правым предсердием может понадобиться в раннем послеоперационном периоде. В зависи мости от течения оно может быть частично откры тым или полностью перекрытым в раннем послео перационном периоде или позже.
Интра экстракардиальное полное кавопульмональное соединение
Альтернативной техникой является импланта ция интра экстракардиального кондуита, которая
б
а
в
Рис. 18. Техника создания разгрузочного отверстия между экстракардиальным каналом и правым предсердием. Отверс тие заданного диаметра (обычно 4 мм) в сосудистом протезе просекают перфоратором. Анастомоз выполняют, отступя 3–4 мм от края фенестрации, 5/0 проленом или швом из Gore Tex. Швы проводят на всю толщину стенки предсердия и поверхностно на стенке кондуита (аñв этапы операции)
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
1026 |
Часть 12. КОМПЛЕКСНЫЕ ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА |
|
|
|
|
особенно полезна у пациентов с множествнными отверстиями печеночных вен, открывающихся в правое предсердие. Пациентов охлаждают до 22°С, чтобы иметь возможность снизить кровоток. По лые вены обжимают турникетами, вводят в аорту кардиоплегический раствор для остановки сердца. Производят продольный разрез правого предсер дия до нижнего кавоатриального соединения. Снижают скорость кровотока, пережимают и уда ляют канюлю НПВ, заменяя ее тонким отсосным наконечником.
Отверстия НПВ и печеночных вен должны быть хорошо видны. Подбирают трубку из Gore Tex подходящего размера и пришивают ее вокруг всех венозных отверстий (рис. 19, а). Линию шва начинают с медиального края отверстия НПВ. После анастомозирования нижнего конца конду ита последний выводят наружу сердца через отве рстие в предсердии. Выбирают место перфорации кондуита внутри предсердия и просекают 4 мм от верстие аортальным пробойником (рис. 19, б). Да лее края разреза предсердия пришивают к наруж ной поверхности кондуита непрерывным 5/0 или 6/0 проленовым швом. Верхний конец трубки дол
жен быть без натяжения и избытка прилажен к нижней поверхности правой легочной артерии. Выполняют разрез правой легочной артерии от места ее отхождения до начала ветвления. Анасто моз выполняют непрерывным 6/0 проленовым швом (рис. 19, в). Отсосный наконечник удаляют из НПВ и через отверстие, ограниченное кисет ным швом, вводят венозную канюлю. Аорту за полняют кровью, удаляют воздух и больного сог ревают.
Особенности ведения раннего послеоперационного периода
Ведение раннего послеоперационного периода у больных, перенесших операцию Fontan, имеет специфические особенности. При данной модели кровобращения источником энергии является только один желудочек, который обеспечивает кровоток как в системных, так и в легочных сосу дах. Поэтому очень важно, чтобы сопротивление потоку крови на всех ее участках было минималь ным. В связи с этим надо быть абсолютно уверен ным в отсутствии градиента давления между по лыми венами и легочными артериями. Градиент
а
б
в
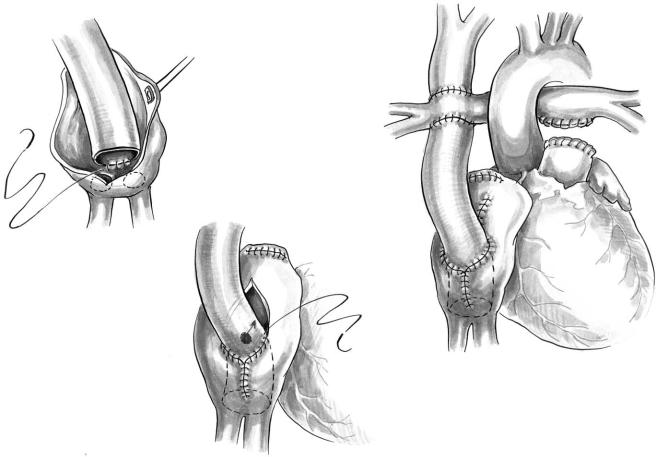
Рис. 19. Этапы выполнения операции Fontan в виде интра экстракардиального полного кавопульмонального соединения
Глава 63. ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОРОКОВ СЕРДЦА С ФУНКЦИОНАЛЬНО ЕДИНСТВЕННЫМ ЖЕЛУДОЧКОМ |
1027 |
|
|
|
|
|
|
|
давления больше 2 мм рт. ст. указывает на наличие |
ниже, чем при искусственной вентиляции легких, |
|
существенного сужения в месте анастомоза, кото |
поэтому мы предпочитаем переводить больных на |
|
рое необходимо устранить. |
самостоятельное дыхание как можно раньше, если |
|
Для оценки состояния кровообращения в пер |
позволяет состояние гемодинамики. При спон |
|
вые 24 ч после операции важными показателями |
танном дыхании во время вдоха давление в плев |
|
являются величины давления в правом и левом |
ральных полостях и легочных капиллярах снижа |
|
предсердиях. Если операция выполнена адекват |
ется, что облегчает приток крови в малый круг |
|
но, показатель отношения среднего давления в |
кровообращения и увеличивает сердечный выб |
|
правом предсердии к среднему давлению в левом |
рос. Во время искусственной вентиляции при пос |
|
предсердии должен быть около 2, что является от |
туплении газовой смеси в легкие повышается |
|
ражением оптимальных условий кровотока в ма |
внутрилегочное давление, а это приводит к умень |
|
лом круге кровообращения при отсутствии в нем |
шению притока крови к правому предсердию и |
|
активной нагнетающей камеры (129). Повышение |
ухудшению легочного кровотока. В эксперименте |
|
давления в левом предсердии неизбежно приводит |
Shemin и соавторы (188) обнаружили снижение |
|
к повышению давления в правом предсердии из за |
кровотока по атриопульмональному кондуиту при |
|
возрастания постнагрузки. Считается, что после |
повышении дыхательного объема и давления на |
|
операций, которые предусматривают двухжелу |
вдохе. Во время выдоха кровоток по кондуиту рез |
|
дочковый тип кровообращения, среднее давление |
ко возрастал. Вместе с тем, общий объем протека |
|
в левом предсердии должно быть в пределах 14 мм |
емой крови не менялся. Williams и соавторы (189) |
|
рт. ст. После операции Fontan такое давление мо |
изучали влияние искусственной вентиляции с по |
|
жет существенно ухудшить легочный кровоток. |
ложительным давлением в конце выдоха (дыха |
|
Для обеспечения нормального сердечного выб |
тельного режима, который довольно часто приме |
|
роса правопредсердное давление необходимо под |
няется после операций на сердце) на гемодинами |
|
держивать на уровне 10–15 мм рт. ст. Если для |
ку у больных после операции Fontan. Они устано |
|
поддержания адекватной гемодинамики в раннем |
вили, что положительное давление в конце выдоха |
|
послеоперационном периоде необходимо повы |
существенно повышало РаО2. Однако с нараста |
|
сить давление в правом предсердии выше 16 мм рт. |
нием давления снижался сердечный выброс. Па |
|
ст., это свидетельствует о наличии факторов, нега |
дение величины сердечного выброса было связано |
|
тивно влияющих на кровообращение: сужения в |
с повышением ЛСС. В то же время многолетний |
|
месте анастомоза, высокого ЛСС, гипоплазии ле |
клинический опыт показывает, что на практике |
|
гочных артерий, а также высокого давления в ле |
вредное влияние искусственной вентиляции на |
|
вом предсердии из за патологии АV клапанов или |
гемодинамику можно наблюдать не так часто (30). |
|
миокардиальной недостаточности. Указанные |
У 7,9% больных, которым мы выполняли опе |
|
факторы приводят к повышению давления в пра |
рацию Fontan, во время перевода на самостоятель |
|
вом предсердии, а это, в свою очередь, ухудшает |
ное дыхание наблюдалось повышение артериаль |
|
гемодинамику и усиливает транссудацию. |
ного давления в среднем на 8 + 3 мм рт. ст., а у |
|
Известно, что на обеспечение артериального |
11,8% пациентов — повышение сатурации артери |
|
кровотока расходуется около 90% энергии систем |
альной крови кислородом (190). |
|
ного желудочка, а венозного — только 10%. В цик |
В связи с тем что при данной модели кровообра |
|
ле кровообращения по Fontan легочный кровоток |
щения имеется тенденция к просачиванию жидкос |
|
является продолжением венозного, поэтому един |
ти из кровяного русла в интерстициальное простра |
|
ственный желудочек должен затрачивать энергию |
нство, необходимое давление в правом предсердии |
|
на преодоление не только сопротивления систем |
должно поддерживаться за счет инфузии раствора |
|
ных сосудов, но и общелегочного сопротивления. |
10% альбумина или нативной плазмы. Для поддер |
|
Повышение венозного давления в результате |
жания адекватного сердечного выброса обычно тре |
|
Fontan коррекции приводит к рефлекторному по |
буется инотропная поддержка допамином. |
|
вышению тонуса артериол, что также влияет на |
В наших наблюдениях в назначении допамина |
|
постнагрузку (36). Вследствие этого возникает не |
нуждались 84 % больных. Доза допамина у выжив |
|
обходимость в применении вазодилататоров (нат |
ших больных не превышала 10 мкг/кг/мин. Отме |
|
рия нитропруссида или амринона) для снижения |
чено, что у пациентов, умерших вследствие синд |
|
общего периферического сопротивления. Также |
рома малого сердечного выброса, увеличение дозы |
|
необходимо создать оптимальный режим вентиля |
выше 10 мкг/кг/мин не оказывало существенного |
|
ции легких в целях предотврашения повышения |
эффекта (190). |
|
ЛСС. Во время самостоятельного дыхания ЛСС |
Одним из важных моментов ведения раннего |
|
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
1028 |
Часть 12. КОМПЛЕКСНЫЕ ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА |
|
|
|
|
послеоперационного периода является определе ние возможности пациента адаптироваться к фи зиологии кровообращения по Fontan. Больным, которые не могут приспособиться к этому типу кровообращения, в целях сохранения жизни сле дует предпринять срочное вмешательство по кон версии его в состояние, приближенное к исходно му. Признаками недостаточности кровообраще ния по Fontan являются: повышенное венозное давление (больше 16–18 мм рт. ст.), артериальная гипотония, олигурия, нарушение периферическо го кровообращения, резистентность к высоким дозам инотропной поддержки. Наличие стойкого повышенного давления в левом предсердии (выше 12 мм рт. ст.), также является угрожающим приз наком. В этих случаях немедленно должны быть произведены эхокардиография и катетеризация сердца для выявления дефектов коррекции, которые следует сразу же устранить. Если это не возможно, необходимо конвертировать операцию Fontan в ДКПА или системно легочный анасто моз. По данным Castaneda и соавторов (36), транс формация кровообращения Fontan в ДКПА пред почтительнее другого варианта.
Наиболее частым осложнением раннего после операционного периода является выраженная транссудация в плевральные, перикардиальную и брюшную полости. В связи с этим обязательным компонентом операции является дренирование всех полостей.
Возникновение транссудации связано с повы шением системного венозного давления. Предпо лагается, что в механизме транссудации важную роль играет венозный застой в органах брюшной полости. Среди наших больных после ДКПА, у ко торых отмечалось повышение венозного давления только в верхней половине туловища, транссуда ция наблюдалась значительно реже (4%), чем у па циентов, перенесших полную коррекцию по Fontan (52%) (49). Jacobs и Norwood (59) наблюда ли существенное снижение частоты возникнове ния транссудации в плевральные полости у боль ных, которым во время выполнения операции Fontan печеночные вены отводили в левое пред сердие (т.е. оставляли их в зоне низкого давления). Необходимо также отметить, что стенки капилля ров печени обладают большей проницаемостью, чем стенки капилляров других органов.
Наш опыт показывает, что частота возникнове ния транссудации у пациентов после операции Fontan с разгрузочным отверстием была меньше, чем у пациентов без фенестрации венозного кана ла (30% против 75,5% соответственно). Наличие фенестра также сказалось на уменьшении продол
жительности транссудации (7,2 ± 3,4 сут против 22,2±5,3 сут соответственно) (49).
Впоследнее время установлено, что в генезе выпотевания жидкости в экстравазальное прост ранство имеет значение повышение уровня нат рийуретического фактора (пептида) в плазме кро ви, который способствует усилению транссудации (191). В дальнейшем Mainwaring и соавторы (192) показали, что у пациентов с кровообращением по Fontan наблюдается усиленная эндокринная реак ция, проявляющаяся повышением уровня антиди уретического гормона, альдостерона, ренина и ан гиотензина II. Эти данные позволили сделать предположение о том, что повышенная актив ность ренин ангиотензиновой системы также принимает участие в патогенезе транссудации. Та кая взаимосвязь была подтверждена последующи ми исследованиями (193).
У детей младшего возраста риск возникнове ния стойкой транссудации значительно выше, чем
устарших. Установлено, что проницаемость сис темных капилляров у них выражена больше (194, 195). Этим объясняется большая вероятность воз никновения и тяжесть протекания этих осложне ний у младенцев.
Всвязи с потерей белка из за транссудации возникает необходимость в его ежедневном вос полнении. В первые дни после операции это дос тигается путем внутривенных инфузий белковых препаратов, а в последующем — сочетанием сба лансированного питания, обеспечивающего син тез нового белка, с инфузией белковых препара тов. Кроме того, назначают диету с исключением жиров, соли и ограничением употребления жид кости. Если транссудация не прекращается в тече ние 2–3 нед после операции, для исключения при чин анатомического характера производят катете ризацию сердца.
Втечение первых 3–6 нед прекратившаяся транссудация может возобновиться, поэтому больные должны находиться под постоянным наблюдением врача. В этот период им назначают диуретики и рекомендуют соблюдение режима с ограничением приема жидкости и соли.
Серьезным осложнением ближайшего послео перационного периода является хилоторакс. Если в первые дни после операции обычно наблюдается выпот серозной жидкости, то при длительной транссудации всегда следует ожидать хилоторакс. Причины развития данного осложнения до конца не выяснены. Если исключить простую травму грудного протока во время операции, то появле ние этого осложнения, очевидно, связано с чрез мерным повышением венозного давления, вслед
Глава 63. ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОРОКОВ СЕРДЦА С ФУНКЦИОНАЛЬНО ЕДИНСТВЕННЫМ ЖЕЛУДОЧКОМ |
1029 |
|
|
|
|
ствие которого нарушается дренаж лимфы (196). Подобное осложнение встречается и у больных без выраженного повышения венозного давления. Ле чение хилоторакса включает выполнение плев ральных пункций, диетотерапию, восстановление нормального уровня белка крови. В случаях, когда не удается избавиться от лимфореи путем консер вативного лечения, можно сформировать торако абдоминальный шунт. Для этих целей лучше ис пользовать армированную силиконовую трубку, которую проводят в плевральную полость через VI межреберный промежуток и фиксируют к надко стнице ребра. Второй конец силиконовой трубки проводят через подкожный канал и отверстие в брюшной стенке в полость живота.
Осложнения после операции Fontan
Несмотря на значительные успехи, достигну тые за последние годы в лечении аномалий сердца с функционально единственным желудочком, ос тается целый ряд проблем отдаленного периода. Они обусловлены несовершенством этого типа кровообращения.
Вожможны следующие осложнения операции Fontan:
—правая атриомегалия и дисфункция печени;
—дилатация коронарного синуса;
—вероятность повторных вмешательств;
—тромбэмболия в системный и легочный круги кровообращения;
—энтеропатия с потерей белка;
—развитие артериовенозных фистул легких;
—миокардиальная недостаточность;
—обструкция выхода в системный круг кровооб ращения;
—обструкция легочных вен;
—реканализация лигированного легочного ствола;
—нарушения ритма сердца;
—образование системно легочных коллатералей;
—неврологические осложнения;
—пластический бронхит.
Правая атриомегалия и дисфункция печени яв ляются наиболее характерными осложнениями у пациентов, которым была выполнена операция Fontan в виде модификаций, предусматривающих соединение правого предсердия с легочным ство лом или правым желудочком (98, 197–204). Это обусловлено повышенным давлением в правом предсердии в случаях, когда использовали прямое соединение правого предсердия с легочным ство лом. При модификации Bjork расширение правого предсердия возникает вследствие систолической регургитации из правого желудочка в правое пред
сердие (205). Дисфункция печени, вероятно, свя зана с дилатацией печеночных вен, однако убеди тельных доказательств того, что это способствует развитию цирроза печени, нет (197–199). Есть на дежда, что с применением более современных мо дификаций операции Fontan в виде полного каво пульмонального соединения с разгрузочным отве рстием значительно уменьшится частота приве денных осложнений. При наличии симптомов дисфункции печени необходимо исключить ана томические и гемодинамические причины нару шения кровообращения путем комплексного обс ледования, включая ангиокардиографию.
Дилатация коронарного синуса. Современные модификации операции Fontan предусматривают дренирование крови из коронарного синуса в левое предсердие, в котором давление остается низким. Несмотря на небольшой сброс венозной крови в системное кровообращение, этот прием исключает нарушение коронарного кровотока и другие ослож нения, связанные с дилатацией коронарного сину са (98, 201–204). На раннем историческом этапе применения операции Fontan у большинства боль ных коронарный синус оставляли в зоне высокого венозного давления, что в некоторых случаях спо собствовало расширению коронарного синуса. Описаны случаи, когда дилатация коронарного си нуса была настолько выраженной, что затрудняла приток крови к митральному клапану (98, 206).
В отдаленном периоде у некоторых пациентов остается вероятность повторных хирургических или других интервенционных вмешательств. Несмотря на то, что существует тенденция к самопроизволь ному закрытию разгрузочных отверстий или уменьшению их размеров со временем, в больши нстве случаев их приходится закрывать из за уси ления цианоза или угрозы образования тромбов. Во многих клиниках для этого используют прис пособления, которые позволяют закрыть отверс тие катетерным способом (98).
Наиболее частой причиной повторных вмеша тельств является возникновение обструкций на пу ти потока крови из вен в легочные артерии. По со вокупным данным двух кардиохирургических центров, основанным на опыте лечения 334 боль ных, через год после операции не нуждаются в пов торном хирургическом вмешательстве 99% паци ентов, через 5 лет — 96%, а через 10 и 15 лет — 86% и 59% соответственно (207). Существует законо мерность частоты повторных вмешательств в зави симости от применяемой модификации операции Fontan. Обструкцию чаще наблюдали у пациентов после применения кондуита между правым пред сердием и правым желудочком по сравнению с те
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
1030 |
Часть 12. КОМПЛЕКСНЫЕ ВРОЖДЕННЫЕ ПОРОКИ СЕРДЦА |
|
|
|
|
ми, у кого формировали прямое соединение пра вого предсердия с правым желудочком. Частота ре операций через 5, 10 и 15 лет в первом случае сос тавила соответственно 17, 13 и 23%, а во втором — 4, 1 и 10%. Аналогичная закономерность установ лена при сравнении результатов выполнения атриопульмонального соединения с использова нием кондуита и без него. Обструкция возникает обычно на уровне дистального или проксимально го концов экстракардиального полного кавопуль монального соединения, а также дистального анас томоза внутрипредсердного туннеля (98).
Не существует единой тактики по вопросу при менения антикоагулянтной терапии, ее продол жительности и выбора медикаментозных средств. Очевидна ее необходимость, так как описаны слу чаи тромбоэмболии в системные и легочные арте рии (208–212). Частота этих осложнений, по дан ным разных авторов, варьирует от 2,6 до 20% (209, 212–214). Тромбоэмболии возникали как в первые сутки после операции, так и через несколько лет. Мы наблюдали лишь два случая тромбоэмболии в легочные артерии у пациентов с прямым соедине нием правого предсердия и легочного ствола спус тя 10 и 12 лет после операции. Это осложнение бы ло следствием возникшей мерцательной аритмии.
Одним из самых серьезных осложнений опера ции Fontan является энтеропатия с потерей белка (ЭПБ). По данным литературы, это осложнение встречается у 3–15% больных, перенесших такое вмешательство. На протяжении 5 лет после воз никновения этого осложнения 50% пациентов умирают (215–225). Энтеропатия с потерей белка может возникнуть в любое время, на первой неде ле или через несколько лет после операции (215, 216). Патофизиологический механизм возникно вения этого осложнения не совсем понятен.
Клинические проявления ЭПБ обусловлены снижением уровня белка в плазме крови за счет плохой утилизации его на уровне кишечника. Вледствие этого уменьшается онкотическое давле ние в сосудистом пространстве. Избыточное на копление белка в стенке кишечника является при чиной поносов и спазматических болей. Интен сивная кишечная потеря белка приводит к усиле нию дренирования в лимфатическую систему, ди латации лимфатических сосудов кишечника и ухудшению абсорбции жира. Вследствие гипопро теинемии развиваются периферические отеки, ас цит, а также транссудация в плевральные и пери кардиальную полости. Из за недостаточного со держания гамма глобулинов ухудшается иммуни тет пациента. Наблюдается также дефицит лимфо цитов, которые не попадают в кровеносное русло
из за потери в кишечнике по причине дилатации лимфатических протоков. На потерю белка также может реагировать свертывающая система крови возникновением гиперкоагуляции (226, 227).
Начальные признаки этого осложнения могут быть едва заметными и маскироваться под симп томы продромального периода вирусной инфек ции. Первыми признаками ЭПБ являются отеч ность тканей вокруг глаз после сна и лодыжек ног. У маленьких детей наблюдается вздутие живота, а у старших детей и у взрослых пациентов внезапно возникают профузные поносы или жидкий стул.
Диагноз ЭПБ с потерей белка устанавливают на основании вышеперечисленных симптомов и дан ных биохимических исследований крови, которые указывают на снижение уровня общего белка в крови, а также снижение содержания альбумино вой фракции. Другими причинами гипопротеине мии могут быть ухудшение синтезирующей функ ции печени и нефротический синдром. Наиболее достоверным биохимическим маркером ЭПБ яв ляется клиренс альфа 1 антитрипсина в кале па циента (228). Альфа 1 антитрипсин является ста бильным белком, который вырабатывается в пече ни и не метаболизируется. Он нормально выво дится из организма путем экскреции в стенку ки шечника. При ЭПБ содержание альфа 1 антит рипсина в кале значительно увеличивается и в со ответствии с этим также увеличивается его кли ренс. Последний определяется путем сравнения содержания его в кале, собранного за 24 ч, с кон центрацией в крови больного.
Для выбора правильного лечения ЭПБ следует выполнить тщательное обследование пациента в целях определения анатомических или функцио нальных причин нарушения кровообращения. К таким причинам относятся нарушения ритма, на личие недостаточности AV клапанов, дисфункция желудочка, наличие сужений или градиента давле ния в системе венозного оттока. Не установлена связь между возникновкиением ЭПБ и величиной центрального венозного давления (216).
С учетом того, что спектр клинических прояв лений этого осложнения широкий, терапия долж на быть подобрана соответственно выраженности симптомов. Лечение проводят по трем направле ниям:
—коррекция гипопротеинемии;
—улучшение функции слизистой оболочки ки шечника;
—улучшение сердечной гемодинамики.
Как упоминалось раньше, из за потери белка снижается онкотическое давление в сосудистой системе, вследствие чего развиваются перифери
Глава 63. ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ПОРОКОВ СЕРДЦА С ФУНКЦИОНАЛЬНО ЕДИНСТВЕННЫМ ЖЕЛУДОЧКОМ |
1031 |
|
|
|
|
ческие отеки. В связи с этим полезное действие оказывают диуретики, а именно фуросемид и ве рошпирон. Важным условием лечения является соблюдение специальной диеты. Она заключается в приеме пищи с высоким содержанием белка и исключении жиров. Рекомендуется принимать продукты с содержанием среднецепочечных триг лицеридов (6–12 атомов углерода). В отличие от длинноцепочечных, среднецепочечные жирные кислоты расщепляются в тонкой кишке без учас тия панкреатической и кишечной липазы и попа дают в кровоток (воротную вену) вместе с амино кислотами без образования хиломикронов и выде ления в лимфу. Для транспорта среднецепочечных триглицеридов через мембрану митохондрий не требуется карнитин, что также облегчает их усвоя емость. В состав модуля среднецепочечных триг лицеридов входят такие насыщенные жирные кислоты, как капроновая, каприловая, каприно вая и лауриновая, естественными источниками которых являются кокосовое и пальмовое масла. Для восполнения потери белка необходимо пере ливать белковые препараты (раствор альбумина, нативную плазму). В случаях выраженной потери белка и снижения онкотического давления, обус ловленных отеком кишечника, полезно внутри венное вливание аминокислот.
Уменьшению потери белка через слизистую оболочку кишечника способствуют кортикостеро иды и гепарин. Описаны случаи эффективного ле чения ЭПБ высокимих дозами преднизона (1–2 мг/кг/день на протяжении 14–21 дня) (218, 229). Препарат вводили парентерально в связи с плохой всасываемостью в отечном кишечнике.
Эффективное воздействие гепарина на слизис тую оболочку кишечника у пациентов с ЭПБ впер вые установили в Мичиганском университете (220). Авторы предложили назначать гепарин в до зе 5000 ЕД/м2/день подкожно. Отмечено, что лече ние низкомолекулярным гепарином в таких слу чаях не оказывает эффекта. Механизм действия как преднизона, так и гепарина основан на том, что они способствуют стабилизации клеточных мембран и таким образом препятствуют потере белка через слизистую оболочку кишечника.
Несмотря на то что лечение ЭПБ вышепере численными средствами относительно эффектив но, терапевтическое лечение не влияет на этиопа тогенез осложнения. Этиологической причиной осложнений являются значительные изменения сердечно сосудистой системы вследствие созда ния неестественной модели кровообращения. По этому в комплексе лечения ЭПБ основная роль принадлежит хирургическим способам улучшения
функции сердца для создания максимально воз можного сердечного выброса.
Одним из таких способов является разгрузка венозного канала через перфорационное отверс тие для обеспечения сброса крови справа налево (230, 231). В результате сброса крови увеличивает ся наполнение желудочка и, как следствие, увели чивается сердечный выброс. Увеличение сердеч ного выброса сопровождается некоторым сниже нием насыщения артериальной крови кислородом (232, 233). Важным условием достижения положи тельного эффекта является подбор оптимального размера отверстия. Обычно отверстие диаметром 4–5 мм обеспечивает достаточное шунтирование крови справа налево без значительного снижения сатурации артериальной крови. Об адекватном размере разгрузочного отверстия можно судить по насыщению артериальной крови кислородом, ко торое при дыхании комнатным воздухом должно находится в пределах 80–85 % (231). Нормализа ция содержания белка в крови больного происхо дит через 6–8 нед после фенестрации.
Одной из причин уменьшения сердечного выб роса могут быть нарушения координации сокра щений предсердий и желудочка вследствие сла бости синусового узла. Имплантация двухкамер ного стимулятора позволяет избавиться от этого осложнения (225).
Улучшение функции кровообращения может быть достигнуто путем конверсии атриопульмо нального соединения в полное кавопульмональ ное соединение, которое более совершенно с точ ки зрения гидродинамики. Такая операция обыч но сочетается с имплантацией двухкамерного сти мулятора, криоабляцией проводящих путей и формированием разгрузочного отверстия.
Крайним вариантом лечения пациентов с вы раженной формой ЭПБ является трансплантация сердца. Однако результаты значительно хуже, чем у пациентов, перенесших трансплантацию сердца по поводу других заболеваниий (216). Это связано с длительным существованием ЭПБ и необрати мыми изменениями в кишечнике, легких, иммун ной системе и других органах (218).
В результате разделения венозной и артериаль ной крови после операции Fontan пациенты с функционально единственным желудочком из бавляются от цианоза. Возникновение артериаль ной гипоксемии может быть вызвано:
—шунтированием крови через разгрузочное отве рстие в венозном канале, сформированное во время операции;
—шунтированием крови через резидуальные со общения между предсердиями;
Рекомендовано к покупке и изучению сайтом МедУнивер - https://meduniver.com/
