
- •В. Н. Седалищев Физические основы получения измерительной информации с использованием генераторных и параметрических первичных преобразователей Учебное пособие
- •Введение
- •Глава 1
- •1. Информационно-энергетические основы теории измерений
- •1.1 Понятие информации. Разновидности информации
- •1.2 Количественная оценка информации
- •1.3 Связь понятий энергии и информации Информационный подход к анализу физических процессов
- •1.4 Применение энерго-информационного подхода к анализу физических процессов
- •Аномалии физических и химических свойств воды
- •1.5 Связь теории информации с теорией измерений
- •Количественная оценка измерительной информации
- •Естественные пределы измерений
- •1.6 Причины наличия ограничений количества информации, получаемой при измерениях
- •Разновидности шумов и причины их появления
- •1.7 Способы повышения информативности измерительного процесса
- •1.8 Общая характеристика этапов измерительного преобразования
- •Метрологические характеристики измерительных преобразователей
- •1.2 Классификация физических эффектов и областей их применения в измерительной технике
- •«Фундаментальное единство» природы. Метод электромеханических аналогий
- •Физические основы построения измерительных преобразователей генераторного типа
- •Физические основы создания электромеханических измерительных преобразователей генераторного типа
- •2.3 Пьезоэффект и его применение в измерительной технике
- •2.3.1 Теоретические основы построения пьезоэлектрических измерительных преобразователей генераторного типа
- •2.3.3 Ээсз пьезоэлектрического преобразователя генераторного типа
- •2.3.4 Физические основы работы пьезорезонансных измерительных преобразователей
- •2.3.2 Электрострикция и области применения ее в измерительной технике
- •2.4 Физические основы создания термоэлектрических измерительных преобразователей
- •2.4.1 Пироэффект и применение его в измерительных устройствах
- •2.4.2 Термоэлектрические эффекты в проводниках и полупроводниках
- •2.4.3 Особенности практической реализации термоэлектрических эффектов в измерительных устройствах
- •2.5 Гальваномагнитные эффекты и применение их в измерительных устройствах
- •2.5.1 Эффект Холла и применение его в измерительных устройствах
- •3. Физические эффекты, связанные с модуляцией активного сопротивления ээсз измерительного преобразователя
- •3.1 Принципы построения и разновидности резистивных измерительных преобразователей
- •3. 2 Физические основы создания пьезорезистивных преобразователей контактного сопротивления
- •3.3 Физические основы создания тензорезистивных проводниковых измерительных преобразователей
- •3.4 Физические основы полупроводниковых тензорезистивных преобразователей
- •3.6 Физические основы магниторезистивных измерительных преобразователей
- •3.7 Физические основы работы проводниковых терморезистивных измерительных преобразователей
- •3.8 Физические основы создания полупроводниковых терморезистивных измерительных преобразователей
- •3.9 Физические основы создания фоторезистивных измерительных преобразователей
- •3.10 Физические основы применения явления сверхпроводимости в измерительных устройствах
- •3.10.1 Свойства сверхпроводников
- •3.10.2 Квантово-механическая теория сверхпроводимости
- •Объяснение понятий экситона и поляритона
- •3.10.3 Применение явления сверхпроводимости в измерительной технике
- •3.10.4 Эффект Мейснера и его практическое применение
- •3.10.5 Стационарный и нестационарный эффекты Джозефсона и применение их в измерительной технике
- •4. Физические основы создания электрохимических измерительных преобразователей
- •4.1 Полярографический эффект в растворах и применение его в измерительных устройствах
- •4.2 Физические основы работы кондуктометрических измерительных преобразователей
- •4.3 Применение в измерительной технике электрокинетических явлений в растворах
- •4.4 Принципы работы гальванических измерительных преобразователей
- •5. Физические основы создания первичных преобразователей, основанных на модуляции магнитных параметров измерительной цепи
- •5.1 Принцип работы магнитоиндукционных измерительных преобразователей генераторного типа
- •5.2 Теоретические основы создания индуктивных измерительных преобразователей
- •5.3 Принцип работы вихретоковых измерительных устройств
- •5.4 Физические основы магнитомодуляционных измерительных преобразователей
- •Эффект Виганда
- •5.5 Физические эффекты, связанные с модуляцией магнитных характеристик материалов
- •Пример реализации магнитострикционного эффекта в датчиках линейных перемещений
- •Принцип работы устройства
- •Дополнительные эффекты, возникающие в магнитомодуляционных преобразователях
- •5.6 Физические основы создания магнитоупругих измерительных преобразователей
- •5.7 Зависимость магнитной проницаемости ферромагнетиков от влияющих факторов
- •6. Физические основы создания емкостных измерительных преобразователей
- •6.1 Модуляция геометрических размеров емкостных преобразователей
- •Принципы работы емкостных измерительных преобразователей
- •Емкостной преобразователь с переменной площадью обкладок
- •6.2 Физические основы емкостных измерительных устройств, основанных на модуляции диэлектрических свойств веществ
- •6.2.1 Строение материалов
- •6.2.2 Виды связей и механизмы поляризации диэлектриков
- •6.2.3 Влияние агрегатного состояния вещества на его диэлектрические свойства
- •6.2.4 Примеры практической реализация емкостных измерительных устройств, основанных на управлении диэлектрической проницаемостью веществ
- •7. Физические основы создания биодатчиков генераторного и параметрического типов
- •Глава 1. Информационно-энергетические основы теории измерений
- •Глава 2. Физические основы построения измерительных преобразователей генераторного типа
- •Глава 3. Физические эффекты, связанные с модуляцией активного сопротивления ээсз измерительного преобразователя
- •Глава 4. Физические основы создания электрохимических измерительных преобразователей
- •Глава 5. Физические основы создания первичных преобразователей, основанных на модуляции магнитных параметров измерительной цепи
- •Глава 6. Физические основы создания емкостных измерительных преобразователей
- •Глава 7. Физические основы создания биодатчиков генераторного и параметрического типов
- •Перечень физических эффектов
1.4 Применение энерго-информационного подхода к анализу физических процессов
Рассмотрим пример
энерго-информационного подхода к анализу
термодинамических процессов, протекающих
в реальных системах. Например, лед массой
m
= 0,1кг, имеющего начальную температуру
![]() 240К,
нагреем и расплавим, затем нагреем
образовавшуюся воду и испарим ее.
Произведем расчет изменения энтропии
в такой системе и сравним между собой
информативность протекающих при этом
физических процессов.
240К,
нагреем и расплавим, затем нагреем
образовавшуюся воду и испарим ее.
Произведем расчет изменения энтропии
в такой системе и сравним между собой
информативность протекающих при этом
физических процессов.
При нагревании вещества потребляемая им тепловая энергия расходуется на изменение внутренней энергии (кинетической, потенциальной и энергии взаимодействий атомов и молекул), что и обуславливает в итоге изменение его агрегатного состояния. При повышении температуры вещества возрастает хаотизация молекул и атомов, что приводит к росту энтропии термодинамической системы. В процессе плавления льда и испарения воды температура тела практически не изменяется, так как поступающая в систему энергия расходуется на разрушение связей между частицами, на изменение его внутреннего строения, структуры, что является также информационным процессом. Поэтому информативность протекающих при нагревании вещества процессов можно оценить количественно.
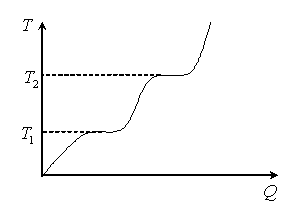
Рис 1.3 График зависимости температуры реальной системы от количества поглощенного ей тепла.
Исходные данные для расчетов:
![]()
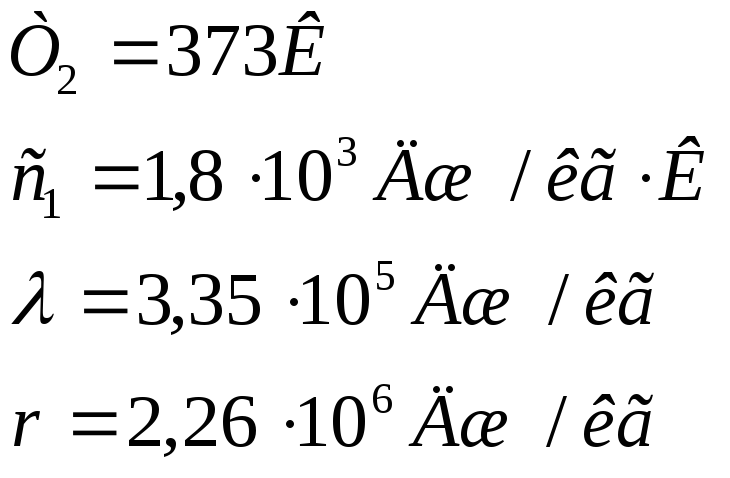
![]()
![]()
Для информационного анализа протекающих процессов воспользуемся известными соотношениями.
При нагревании льда:
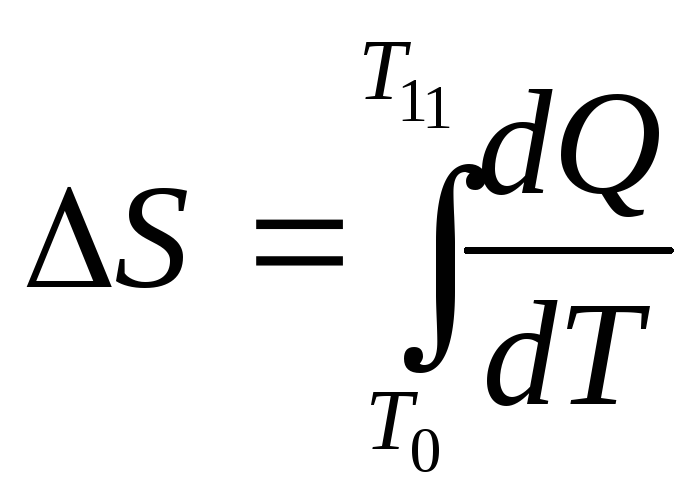 ,
,
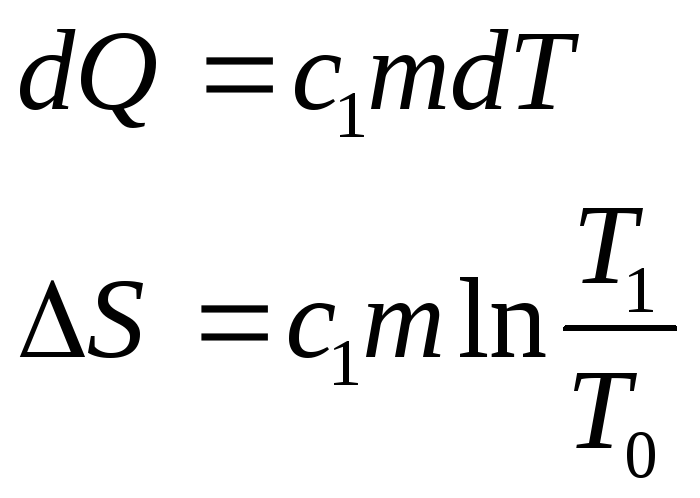
При плавлении льда:
![]()
При нагревании воды:
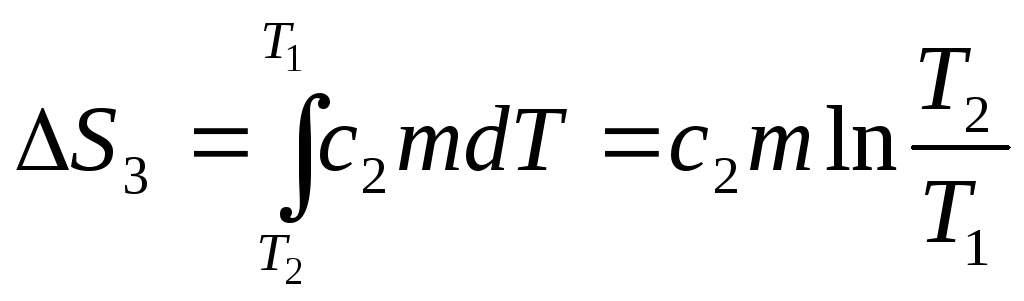
При кипении воды:
![]()
При нагревании пара:
![]()
Изменение энтропии и информативность процессов определим по формулам:
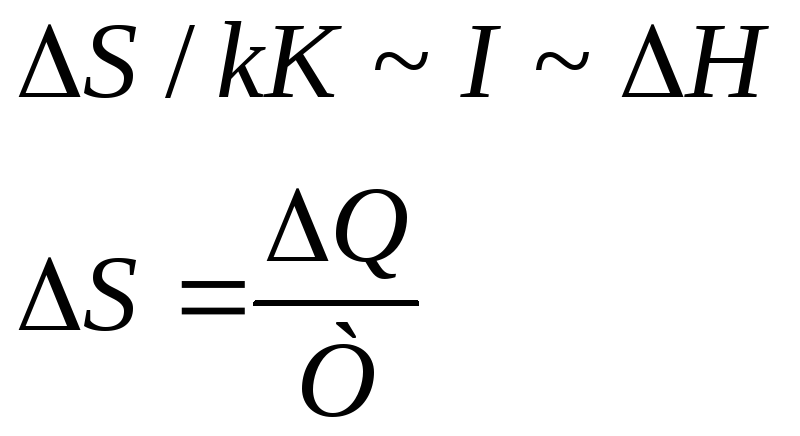 (1.13)
(1.13)
![]() (1.14)
(1.14)
![]()
![]()
На основе данного примера можно показать, что:
процессы, связанные с изменением агрегатного состояния вещества, с изменением его внутренней структуры (плавление льда, испарение воды) намного информативнее процессов простого нагревания вещества, сопровождающегося изменением его температуры;
нагрев воды информативнее процесса нагревания льда;
процесс испарения воды информативнее процесса плавления льда.
высокое значение информативности физического процесса предполагает возможность его использования для создания измерительных устройств высокой чувствительности и разрешающей способности.
Термодинамические процессы в реальных системах характеризуются наличием фазовых переходов двух видов. При термодинамическом переходе первого рода выделяется или поглощается энергия – скрытая теплота перехода. При таком переходе существует многофазная область, в которой фазы находятся в равновесии между собой (например, при переходе жидкости в газообразное или твердое состояние). В точках фазового перехода температура вещества постоянна (Т = const), а молярная теплота перехода (q), соответственно, при плавлении и испарении равна:
![]() ;
;
![]() ;
(1.15)
;
(1.15)
где
![]() - соответствующие приращения энтропии
системы.
- соответствующие приращения энтропии
системы.
Для сравнения информативности данных физических процессов используем следующее соотношение:
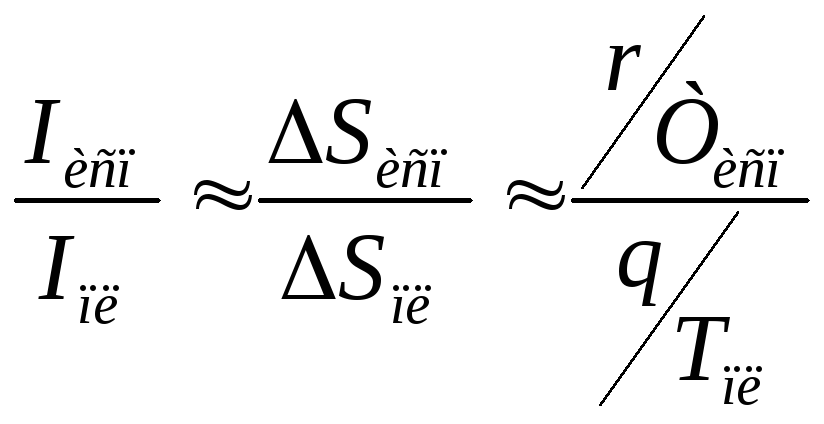 (1.16)
(1.16)
где r; q – значения удельной теплоты испарения и плавления вещества
В таблице 1.1 приведены результаты сравнительной оценки информативности процессов плавления и испарения для некоторых материалов.
Таблица 1.1
|
Вещество
|
удельная теплоемкость
|
температура плавления
|
удельная теплота плавления
|
температура кипения
|
удельная теплота испарения
|
|
|
Алюминий
|
0,88 |
932
|
350 |
2573 |
9220 |
9,5 |
|
Железо |
0,457 |
1803 |
293 |
3323 |
6300 |
12 |
|
Золото |
0,13 |
1336 |
67 |
3073 |
1575 |
10 |
|
Никель |
0,46 |
1725 |
280 |
3273 |
7210 |
13 |
|
Олово |
0,23 |
505 |
59 |
2543 |
3020 |
10 |
|
Серебро |
0,235 |
1234 |
88 |
2433 |
2350 |
13 |
|
Калий |
0,763 |
337 |
61 |
1033 |
2080 |
11 |
|
Натрий |
1,3 |
371 |
113 |
1156 |
4220 |
12 |
|
Вода |
4,19 |
273 |
334 |
373 |
2260 |
5 |
|
Ацетон |
2,18 |
179 |
96 |
329 |
524 |
3 |
|
Бензол |
1,705 |
278 |
127 |
353 |
396 |
2,5 |
|
Спирт этиловый |
2,43 |
159 |
105 |
351 |
846 |
3,7 |
|
Эфир этиловый |
2,35 |
157 |
113 |
308 |
351 |
1,6 |
Как следует из приведенного примера, процесс испарения вещества является более информативным, но требует больших затрат энергии.
Для создания измерительных устройств нужно использовать такие физические процессы, которые позволяют регистрировать малые энергетические воздействия на рабочее вещество. Поэтому наиболее энергозатратный процесс испарения наименее пригоден для создания измерительных устройств, но относительная чувствительность таких устройств, соответственно и их информативность, будет выше.
Для измерения температуры широко применяют жидкостные термометры, а для визуализации процесса тепловыделения или поглощения удобно использовать процессы плавления – кристаллизации веществ. Устройства данного типа нашли применение для создания эталонов температуры. Процессы испарения – конденсации можно рекомендовать для измерения больших тепловых потоков.
Необходимо учитывать, что реальные термодинамические процессы являются нелинейными даже в промежутке между фазовыми переходами, что является причиной появления дополнительных составляющих погрешности измерительных устройств.
Например, известно, что удельная теплоемкость (с) описывает определенные свойства вещества и, строго говоря, не является постоянной величиной во всем температурном диапазоне, включая все состояния вещества. Она может существенно меняться при изменении состояния материала, например, при переходе от твердой фазы к жидкой.
Теплоёмкость системы невзаимодействующих частиц (например, газа) определяется числом степеней свободы частиц, что характеризует число возможных микросостояний частиц, то есть информативность системы. В молекулярно-кинетической теории газов показывается, что молярная теплоёмкость идеального газа с i степенями свободы при постоянном объеме равна:
![]()
R = 8.31 Дж/(моль К) — универсальная газовая постоянная.
При постоянном давлении
![]()
Удельные теплоёмкости многих веществ приведены в справочниках обычно для процесса при постоянном давлении.
На микроскопическом уровне удельная теплоемкость отражает структурные изменения материала.
