
3.4. Методы эндоваскулярного лечения последствий чмт
Эндоваскулярное лечение может быть осущесталено в условиях специализированного учреждения специалистом, имеющим подготовку по эндоваскулярной хирургии, хорошо представляющего патофизиологию и гемодинамику патологического образования и головного мозга и при наличии соответствующего эн-доваскулярного инструментария. Оперативное лечение в большинстве случаев может быть отсрочено, но некоторые состояния, как профузные носовые кровотечения, ложные аневризмы артерий или прогрессирующее снижение зрения при ККС, требуют ускоренной эндоваскулярной операции. Однако, даже в этих случаях в настоящее время больного предпочтительнее доставить в специализированное учреждение, нежели пытаться выполнить паллиативные операции (перевязка артерий на шее, ЛОР-операции в поисках источников кровотечения).
3.4.1. Эндоваскулярное лечение травматических ккс
Эндоваскулярные операции при ККС наиболее разработаны. Практически во всех случаях трансарте-риалъный доступ обеспечивает излечение больного. В институте нейрохирургии им. Н.Н. Бурденко используется преимущественно чрескожный транс-каротидный доступ. Пункция сонной артерии осуществляется той же иглой, что и для проведения раздельной ангиографии НСА и ВСА с баллон-катетером^ просветом 0,9 мм и двумя входными от-
верстиями в павильоне иглы. Через разьемную осевую муфту вводится разделяемый баллон-катетер. Нами используется разделяемый баллон-катетер Ф.А. Сербинснко. Баллон изготавливается из латекса. В головной части баллона имеется серебряный маркер для идентификации его на телеэкране. Катетер, к которому присоединяется баллон, изготовлен из полиэтилена, наружный диаметр катетера 0,7 мм в проксимальном отделе и 0,3 мм в дисталь-ном отделе. Соответственно просвет катетера изменяется от 0.4 до 0,1—0,2 мм.
Операция проводится под нейролептаналгези-ей и местным обезболиванием. При появлении из иглы струи артериальной крови, игла по проводнику (мандрсну) продвигается в просвет сосуда и под рентгеновским контролем подачей небольшого количества контрастного вещества определяется положение иглы в сосуде. Необходимо, чтобы игла свободно располагалась в общей или внутренней сонной артерии, не упиралась в стенку артерии и не отслаивала интиму артерии. Правильное положение иглы, являясь основным условием успешной операции, не будет препятствовать выходу из иглы баллона и продвижению баллон-катетера.
Баллон-катетер соответствующего диаметра и предварительно проверенный на беспрепятственное его прохождение через иглу, проводится под рентгеноскопическим контролем по игле, особенно тщательно контролируется момент выхода баллона из иглы в просвет сосуда, а затем легко продвигается к области фистулы. Как правило, входя в фистулу, баллон резко изменяет свое направление движения и начинает вибрировать в турбулентном потоке крови. Баллон устанавливается вблизи дефекта в артерии со стороны кавернозного синуса, в этом положении фиксируется проксимальная часть катетера разьем-ной гайкой, через которую введен баллон-катетер. Производится раздувание баллона введением разбавленного контрастного вещества при одновременном периодическом контроле на телеэкране степени выключения соустья введением контрастного вещества через боковое отверстие иглы. При полном выключении соустья, измеряется количество введенного в баллон контрастного вещества и оно заменяется таким же количеством наполнителя баллона. В качестве наполнителя мы используем полиамидакриловый гель. Через 1—2 минуты после полимеризации геля, катетер отделяется от баллона и производится контрольная ангиография.
При травматических ККС может быть выполнены два вида операции: реконструктивная и деконструк-тивная. Реконструктивная операция заключается в сохранении или полном восстановлении кровотока по
87
Клиническое руководство по черепно-мозговой травме

Реконструктивные и деконструктивные операции при ККС могут быть выполнены трансартериальным трансфеморальным доступом. Этот доступ имеет много преимуществ перед транс кар отидным и получил широкое применение. Балл он-катетер вводится через проводниковый катетер, установленный в сонной артерии. Это создает больший комфорт для больного и уменьшает лучевую нагрузку на оператора. При этом доступе использование баллон-катетеров Ф.А. Сербиненко затруднено из-за большой мягкости полиэтиленовых катетеров и наличия значительного» мертвого» пространства в длинном катетере, которое не ликвидируется при замене контрастного вещества на гель. Трансартериальный трансфеморальный доступ легко осуществим при использовании коммерческих баллон-катетеров с самозакрывающимися клапанами, которые позволяют в качестве наполнителя баллона использовать контрастное вещество.
Трансартериальный доступ в большинстве случаев обеспечивает успех операции. Однако, в некоторых наблюдениях, при узком дефекте в сонной артерии и для сохранения просвета сонной артерии, может быть применен трансвенозный подход
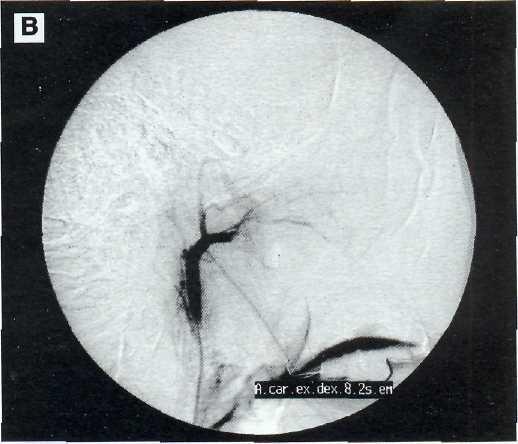
Рис. 3—7. Реконструктивная операция при ККС. Правосторонняя каротидная ангиография.Полное шунтирование кровотока ВСА через фистулу с дренажем кавернозного синуса по глазным венам, нижнему каменистому синусу (А). Кранио-грамма. Положение окклюзируюшего баллона (емкость 0,4 мл.) (Б). Ангиография правой внутренней сонной артерии после отделения катетера и реконструкции правой ВСА (В).
88
Эндовпекулярные методики в хирургии черепно-мозговой травмы

Пунктируется внутренняя яремная вена на шее или же производится катетеризация внутренней яремной вены трансфеморальным венозным доступом. Через проводниковый катетер вводится баллон-катетер в кавернозный синус, например, через нижний каменистый синус (рис. 3—8). Контроль за полнотой выключения фистулы обеспечивается трансартериальной трансфеморальной ангиографией пораженной сонной артерии.
В 1990г. для эмболизации различных сосудистых образований, и в первую очередь артериальных аневризм, были разработаны платиновые и вольфрамовые микроспирали, вводимые специальным устройством через катетер (GDC и MDS). Для лечения ККС их использование остается редким, но в некоторых ситуациях при неполном выключении
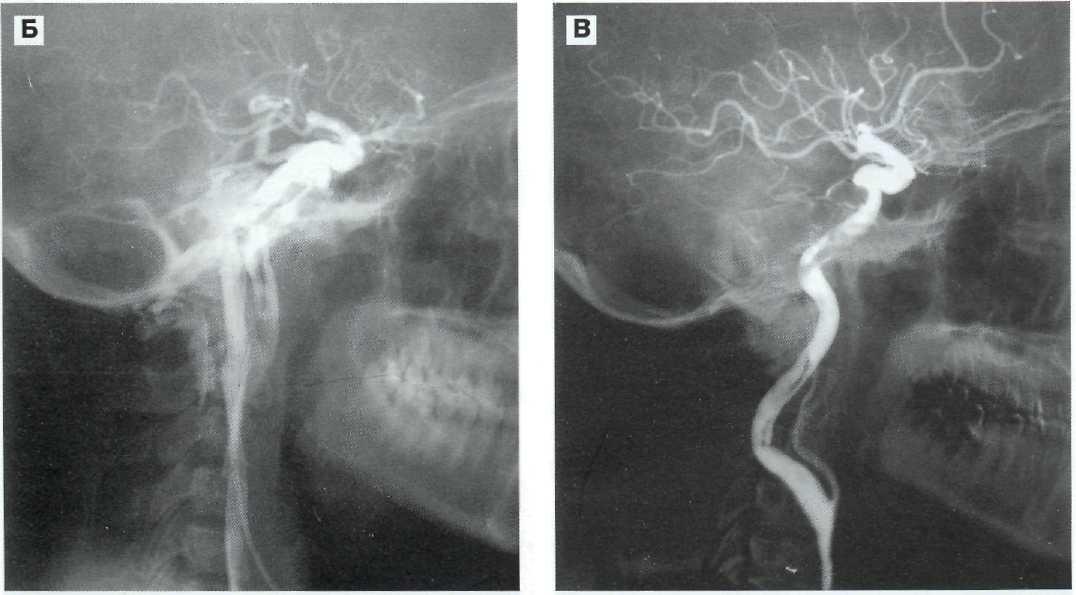
Рис. 3—8. Травматическое ККС слева. Тринсвенозный доступ с окклюзией кавернозного синуса баллоном и реконструкцией ВСА. Каротидная ангиография левой ВСА (А). Дренаж кавернозного синуса происходит по нижнему каменистому синусу. Югулогра-фия слева через катетер, установленный во внутренней яремной вене (Б). При югулографии получено контрастирование не только дренажных путей, но и супраклиноидпой части ВСА, мозговых сосудов. Контрастирование произошло через дефект во ВСА. Каротидная ангиография после установки 2 баллонов в кавернозном и нижнем каменистом синусах с реконструкцией ВСА (В).
89
Клиническое руководство по черепно-мозговой травме
соустья
баллоном или маленьких размерах фистулы,
наличии
остаточной неокклюзированной полости
синуса
или сохраняющегося дренажа дополнительное
применение микроспиралей позволяет
получить
хороший результат [30]. Особенно полезными
микроспирали
оказались для лечения дуральных
артериовенозных
фистул. Введение микроспиралей может
осуществляться как трансартериальным,
так и трансвенозным доступом с подходом
через нижний
каменистый синус или верхнюю глазную
вену.
3.4.2. Эндоваскулярное лечение артериовенозных фистул вертебральной и сонной артерий
Лечение травматических фистул других локализаций (вертебральной артерии, сонной артерии на шее) эндоваскулярньши методами также эффективно. Целью операции является окклюзия близлежащей к фистуле венозной коммуникации баллоном или микроспиралями с сохранением проходимости важного магистрального сосуда. Также допустима окклюзия несущего фистулу сосуда баллоном на уровне фистулы при условии адекватного коллатерального кровоснабжения мозга.
Операция проводится под местной анестезией, позволяющей осуществлять контроль за состояни-
ем больного. Трансфсморальным доступом катетеризируется позвоночная артерия, в ней устанавливается проводниковый катетер, по которому проводится баллон-катетер. Баллон подводится к месту разрыва позвоночной артерии и через шунтирующее отверстие баллон устанавливается в дренирующей вене вблизи дефекта в артерии. Вблизи отверстия баллон раздувают до полного исчезновения шума, аускультируемого в заушной или за-тылочно-шейной области. Чрезбедренная катетеризация обеих позвоночных артерий позволяет контролировать полноту окклюзии фистулы как со стороны проксимального отрезка, так и дисталь-ной части поврежденной вертебральной артерии. Во время операции может быть также проведено контрастирование других сосудов, Особенно важным является контрастирование одноименной наружной сонной артерии для выявления часто встречающегося анастомоза между затылочной и вертебральной артериями. При неполном закрытии фистулы подключаются к шунтированию через фистулу многочисленные коллатерали, которыми являются ветви затылочной, глубокой и восходящей шейных и сегментарных артерий.
Идеальным методом в лечении артериовенозных фистул позвоночной артерии является выключение фистулы с восстановлением кровотока по вертебральной артерии (рис. 3—9). При проведении

Рис. 3—9. Соустье между правой позвоночной артерией и венами позвоночника и спинного мозга после колотого ранения шеи. Правосторонняя вертебральная ангиография: прямая (А) и боковая (Б) проекции.
90
Эндоваскулярные методики в хирургии черепно-мозговой травмы

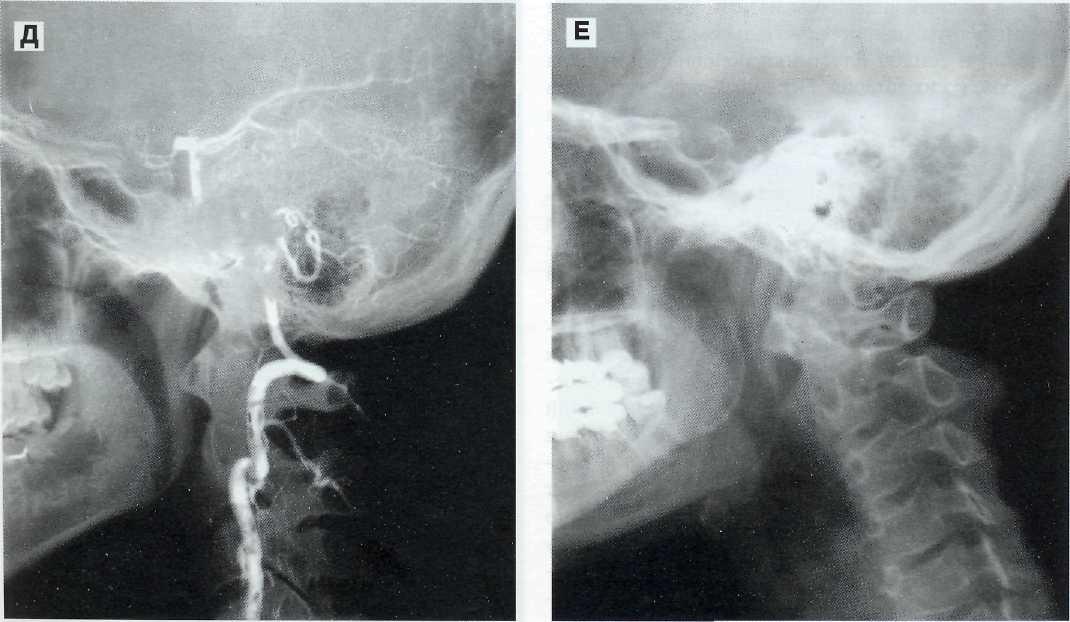
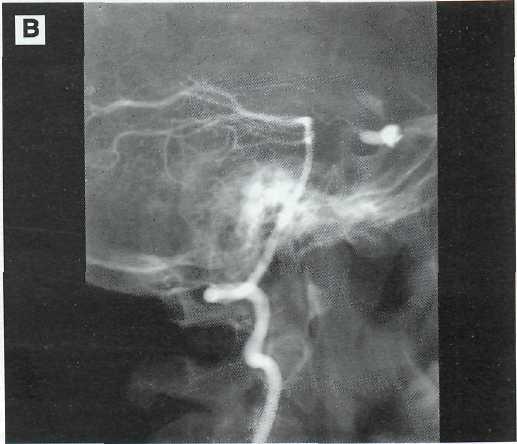
Рис. 3—9 (продолжение). Варикозно расширены затылочные и эпидуральные вены. Левосторонняя вертебральная ангиография выявила умеренно выраженный steal-синдром и состояние дистального супрафистульного отдела правой позвоночной артерии (В). Суперселективная ангиография правой затылочной артерии, выявившая анастомоз между затылочной артерией и правой позвоночной артерией. Позвоночная артерия контрастаруется до фистулы (Г). Правосторонняя всртебральная ангиография после окклюзии фистулы 3 баллонами и восстановления кровотока по правой позвоночной артерии (Д). Рентгенограмма (Е), выполненная через 19 лет после операции. Положение баллонов не изменилось. Клинических признаков функционирования соустья нет.
91
Клиническое руководство по черепно-мозговой травме


3.4.3. Эндоваскулярное лечение
посттравматических ложных аневризм
Посттравматические ложные аневризмы наиболее часто образуются при повреждении ВСА в экстракавернозной ее части, лежащей в сонной борозде основной кости. Эти анеризмы проявляются про-фузными носовыми кровотечениями, кровотечения обильны (от 800 мл и более за короткий промежуток времени), носят рецидивирующий характер. Первые наиболее обильные кровотечения развиваются через месяц и более после травмы. Травматические ложные аневризмы пазухи основной кости формируются при первоначальном повреждении артерии и тонкой пластинки основной кости, на которой лежит артерия. Первоначально, аневризма ограничивается слизистой клиновидной пазухи, а затем, по мере увеличения аневризмы, происходит разрыв слизистой и кровь проникает в носоглотку. При прямой ринофарингоскопии источник кровотечения практически никогда не определяется. При развившемся профузном кровотечении первая помощь заключается в пальцевом прижатии сонной артерии на шее и срочной передней и задней тампонаде полости носа. В виду того, что ложная анер-вризма не имеет истинных стенок, позволяющих фиксировать окклюзирующее устройство в полости аневризмы, в настоящее время радикальной операцией является эндоваскулярная окклюзия ВСА на уровне дефекта артерии с получением локального выпячивания стенки баллона в дефект артерии или окклюзия одним баллоном частично полости аневризмы и сонной артерии (по типу песочных часов или гентели (рис. 3—10). Ангиогра-фическое исследование бассейнов всех магистраль-
Рис. 3—10. Травматическая ложная аневризма. Дооперацион-ная правосторонняя каротидная ангиография (А). Окклюзия ВСА и аневризмы по типу «песочных часов» или «гантели» (Б) с контролем полноты выключения аневризмы контрастированием бассейна противоположной ВСА (Б) и вертебраль-ной (В) артерий.
92
Эндоваскулярные методики в хирургии черепно-мозговой травмы
 ных
сосудов должно подтвердить отсутствие
контрастирование
ложной аневризмы как ретроградным
путем,
так и через каротидно-офтальмический
анастомоз.
Такое оперативное вмешательство может
быть
выполнено при адекватном коллатеральном
кровотоке,
а при его несостоятельности — с пред-
ных
сосудов должно подтвердить отсутствие
контрастирование
ложной аневризмы как ретроградным
путем,
так и через каротидно-офтальмический
анастомоз.
Такое оперативное вмешательство может
быть
выполнено при адекватном коллатеральном
кровотоке,
а при его несостоятельности — с пред-
варительным или непосредственно последующим созданием экстра-интракраниального анастомоза. В большинстве случаев технически возможно выключение полости ложной аневризмы баллоном с сохранением кровотока по ВСА (рис. 3—11). Однако, как правило, кровотечение может возобновить-
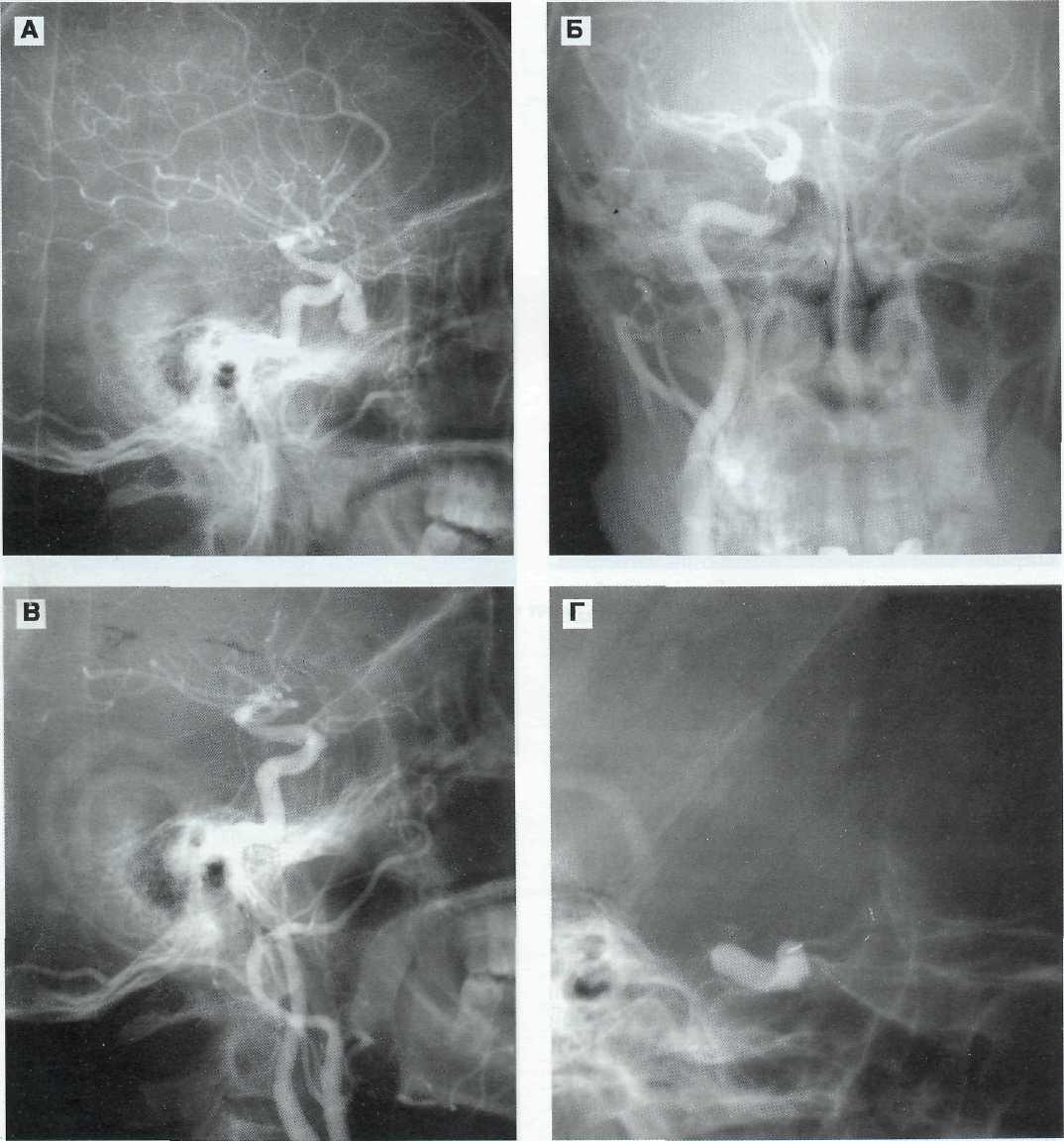
Рис. 3—11. Травматическая ложная аневризма левой ВСА с профузными носовыми кровотечениями. Левосторонняя каротидная ангиограмма (А). Исследование коллатерального кровотока по передним отделам виллизиева круга (Б). Левосторонняя каротидная ангиография после эмболизации аневризмы цианакрилатами (В). Через 5 дней после реконструктивной операции у больного появились признаки носового кровотечения. Произведена окклюзия левой ВСА на уровне устья аневризмы, на что указывает выпячивание стенки баллона в дефект артерии (Г).
93
Клиническое руководство по черепно-мозговой травме


Имеются сообщения о применении микроспиралей для выключения ложных аневризм клиновидной пазухи основной кости при носовых кровотечениях с сохранением кровотока по сонной артерии [35]. Однако, для микроспиралей характерен феномен компрессии внутри аневризмы с открытием частя аневризмы и поэтому также возможны повторные кровотечения.
Относительно необильные посттравматические кровотечения встречаются не редко. Они могут быть обусловлены повреждением конечных ветвей НСА, в частности, внутренней челюстной артерии с образованием ложных микроаневризм. При ангио-графическом исследовании НСА выявляется гипертрофия конечных ветвей внутренней челюстной артерии. Иногда эти источники можно выявить только при проведении ангиографии на фоне кровотечения (рис. 3—12). В этих случаях проводится эмболиза-ция ветвей внутренней челюстной артерии с двух сторон.
Ложные травматические аневризмы сонной артерии на шее (рис. 3—13) или вертебральной артерии характеризуются широким устьем.Эндоваскулярная операция чаще заключается в окклюзии магистрального сосуда ниже дефекта артерии. Ретроградный кровоток при этом наблюдается редко из-за проксимального расположения аневризмы. В некоторых случаях оправдан трепинг аневризмы хирургическим доступом с иссечением самой аневризмы или протезирование артерии с привлечением сосудистых хирургов. Для прямых операций затрудняющим моментом является высокое расположение аневризм под углом нижней челюсти. Перспективным может быть внутрисосуди-стое протезирование с использованием стентов [25].
Таким образом, последствиями ЧМТ могут быть повреждения экстра-интракраниальных сосудов на разных уровнях с образованием артериовенозных фистул, аневризм, тромбоза магистральных сосудов. Клинические проявления многих из последствий ЧМТ являются отсроченными. Эндоваскулярный метод является основным и эффективным методом лечения последствий повреждений сосудов при ЧМТ.
Рис. 3—12. Профузное носовое кровотечение, развившееся после травмы.
Правосторонняя каротидная ангиограмма в прямой (А) и боковой (Б) проекциях. Выявляется источник кровотечения: ложная аневризма дистальных отделов конечных ветвей внутренней челюстной артерии, кровоснабжающих верхние отделы полости носа. Аигиограмма после суперселективной эмбо-лизации конечных ветвей внутренней челюстной артерии (В).
94
Эндоваскулярные методики в хирургии черепно-мозговой травмы

Литература
Арутюнов А.И., Бурлуцкий А.П. Новая модифика ция операции Brooks. В кн. Материалы к Объединенной конференции нейрохирургов. Л., 1964, с. 67.
Сербиненко Ф.А. Новый ангиографический инст рументарий. Вопр. нейрохир., 1964, 2, с. 49—52.
Сербиненко Ф.А. Катетеризация и окклюзия магист ральных сосудов головного мозга и перспективы развимтия сосудистой нейрохирургии. Вопр. нейрохир., 1971, 5, 17—27.
Сербиненко Ф.А. Окклюзия баллоном кавернозно го отдела сонной артерии как метод лечения каротид- но-кавернозных соустий. Вопр. нейрохир., 6, с. 3—8.
Сербиненко Ф.А. Реконструкция кавернозного от дела сонной артерии при каротидно-кавернозных соус тьях. Вопр. нейрохир., 1972, 2, с. 3—8.
Сербиненко Ф.А. Окклюзия баллоном мешотчатых аневризм артерий головного мозга. Вопр. нейрохир., 1974,
4, с. 8-15.
7. Сербиненко Ф.А., Лысачев А.Г, Суперселективная катетеризация мозговых сосудов. Вопр. нейрохир., 1984,
5, с. 6-14.
8. Bavinski G., Killer M., Gruber A., Richling В. Treat ment of post-traumatic carotico-cavcrnous fistulae using elec-
trolytically detachable coils: technical aspects and preliminary experience. Neuroradiology (1997), 39:81—85.
9. Brooks B. The treatment of traumatic arteriovenous fis tula. South Med. J., 23:100-106, 1930.
DandyW.E. Intracranial aneurysms of internal carotid artery, cured by operation. Ann. Surg. (1938), 107: 654—7.
Davie J., Richardson R:Distal internal carotid throm- bo-embolectomy using a Fogarty catheter in total occlusion: technical note. J. Ncurosurg., 27:171 — 177, 1967.
Debrun G., Lacour P., Caron J.P. et al.: Inflatable and released ballon technique. Experimentation in dog. Ap plication in man. Neuroradiology, 9: 267—271, 1975.
Dott N. Intracranial aneurysms: cerebral arteriorad- iography: surgical treatment. Trans. Med. Chir. Soc, Edinb, 1932, 47:219-40.
Fogarty Т., Cranley J., Krause R. et al.: A method for extraction of arterial emboli and thrombi. Surg. Gynecol. Ob- Stet., 116: 241-244, 1963.
Fox A.G. Endovascular therapy of cerebral aneurysms: London, Ontario experience. AJNR:11, 226, 1990.
Guglielmi G., Vinueela F., Sepetka J, Maccelari V. Elcctrothrombosis of saccular aneurysms via endovascular approach. 1. Electrochemical basis, technique and experimental results. Neurosurg., 1991, 75:1—7.
95
Клиническое руководство по черепно-мозговой травме
 Guglielmi
G, Vinuela F., Dion J., Duckwiler G. Elec-
trothrombosis
of saccular aneurysms via endovascular approach.
2.
Preliminary
clinical experience. J. Ncurosurg., :75:8—14,
1991.
Guglielmi
G, Vinuela F., Dion J., Duckwiler G. Elec-
trothrombosis
of saccular aneurysms via endovascular approach.
2.
Preliminary
clinical experience. J. Ncurosurg., :75:8—14,
1991.Guglielmi G., Vinuela F., Briganti F., Duckwiler G. Carotid-cavernous fistula caused by a raptured intracavern- ouse aneurysm: endjvascular treatment by electrothrombosis with detachable coils. Neurosurgery, 31:591—595, 1992.
Higashida R.T, Halbach V.V, Tsai F.Y. et al: Inter- ventional neurovascular treatment of traumatic carotid and vertebral lesions. Results in 234 cases. AJR: 153:577—583, 1989.
Kerber C. Balloon catheter with a calibrated leak. A new system for superselective angiograthy and occiusive catheter therapy. Radiology, ] 20:547—550, 1976.
Konovalov A.N., Serbinenko F.A., Filatov J.M. et al.: Endovascular treatment of arterial aneurysms. AJNR:11,225, 1990.
Le Veen H.H., Curruti M.M. Surgery of large inac cessible arteriovenouse fistulas. Ann. Surg., 158:285—289, 1963.
Lewis A.I., Tomsick Th.A., Tew J.M. and Lawless M.A. Long-term results in direct carotid-cavernous fistulas after treatment with detachable balloons. J. Neurosugery, 84:400-404, 1996.
Luessenhop A., Velasques A.C. Observation on the tolerance of the intracranial arteries to catheterization. J. Neurosurgio, 21:85-91, 1964.
Miyachi S., Shiguchi T.I., Taniguchi K. et al.: Endovas cular Stcnting for Pseudoaneurysms of the Cervical Carotid Artery. Interventional Neuroradiology 3 (Suppl 2), 1997, 129—132.
Moret J., Picard L. Endovascular treatment of berry aneurysms by endovascular approach: analysis of 40 cases. AJNR:11, 1990, 225.
Moret J., Cognard C, Weill A. et al. :The «remodeling technique» in the treatment of wide neck intracranial aneu-
rysms. Angiographic results and clinical follow-up in 56 cases. Interventional Neuroradiology, 3:21—35, 1997.
Mullan S. Treatment of carotid-cavernous fistulas by cavernous sinus occlusion. J. Neurosurg 50:131—144, 1979.
Mullan S., Dude E.E., Patronas NJ. Some examples of balloon technology in Neurosurgery. J. Neurosurgery, 52:321-329, 1980.
Yamashita K., Taki W., Nishi S. et al: Transvenous embolization of dural carotid-cavernous Fistulae: technical considerations. Neuroradoilogy, 135:475—479, 1993.
Prolo D.J. and Hanbery J.W. Intraluminal occlusion of a carotid-cavernous sinus fistula with a balloon catheter. Tech nical note. J. Neurosurgery 35:237—242, 1971.
Serbinenko F.A. Balloon catheterization and occlusion of major cerebral vessels. J. Neurosurgery, 41:125—145, 1974.
Serbinenko F.A., Lysatchev A.G., Edneva Ja.N. Re sults of endovascular treatment of direct carotid-cavernous fistulas. 3-rd International Congress, Minimally Invasive Neurosurgery, Paris-France, 1997, 16/ps. .
Sheglov V.I. Endovascular occlusion of intracranial arterial aneurysms. MT1. FC2. 11.9 European Congress of Neurosurgery, Moscow, 1991.
Teitelbaum G.P., Halbach V.V., Larsen D.W. et al: Treatment of massive posterior epistaxis by detachable coil embolization of a cavernous internal carotid artery aneurysms. Neuroradiology, 37:334-336, 1995.
Todd N.V., Howie J.E., Miller J.D. Norman Dott's contribution to aneurysm surgery. J. Neurol., Neurosug., Psy- chiatr., 53:455—8, 1990.
Zubkov J.N., Nikiforov B.M., Shustin V.A. Balloon catheter technique for dilatation of constricted cerebral arteries after aneurysmal SAH. Acta Neurochir., 70:65—79, 1984.
