
Клин рук-во по ЧМТ том 2 / ГЛАВА 8
.docМультимодальный физиологический мониторинг при тяжелой черепно-мозговой травме
8
МУЛЬТИМОДАЛЬНЫЙ
ФИЗИОЛОГИЧЕСКИЙ МОНИТОРИНГ ПРИ ТЯЖЕЛОЙ ЧЕРЕПНО-МОЗГОВОЙ ТРАВМЕ
8.1. МЕТОДЫ
В настоящее время уже определен базовый комплекс методов, необходимых для оценки адекватности терапии при тяжелой ЧМТ. В его состав входят контроль ВЧД, среднего АД, церебрального пер-фузионного давления (ЦПД), исследование КТ головного мозга в динамике, оценка газового состава крови — РаО2, РаСО2, температуры тела. Каждый из оцениваемых параметров является фактором вторичного повреждения мозга в остром периоде тяжелой ЧМТ и нашел свое отражение в Рекомендациях по ведению этих больных [32].
Помимо перечисленных — в диагностический комплекс также входят широко используемые методы прикроватного физиологического мониторинга (ЭКГ, пульсоксиметрия, капнография, измерение центрального венозного давления, оценка водного баланса, основного обмена) [55].
Дополняющими базовый комплекс методов являются оценка церебральной гемодинамики, церебрального метаболизма, церебральная оксимет-рия, мониторинг биоэлектрической и вызванной активности мозга [77]. Мониторирование практически всех перечисленных физиологических параметров осуществляется в пределах единого прикроватного аппаратурного комлекса (рис. 8—1).
Можно выделить следующие основные методы мультимодального мониторинга, используемые в различных клиниках для оценки состояния больных при тяжелой ЧМТ:
1 — Минимально необходимый мониторинг
(ВЧД и ЦПД) — «золотой» стандарт ней-ромониторинга [32];
2 — Мониторинг мозгового кровообращения
(МК), с использованием:
— количественных методов оценки МК
(Хе133, КТГ со стабильным Хе, позитрон-
В.Г. Амчеславский, СВ. Мадорский, Г.И. Тома, А.К. Молдоташева, A.M. Сафин
но-эмиссионная томография — ПЭТ, МРТ
-
ангиография) [1, 11, 31, 39];
-
качественных методов оценки МК (од- нофотонная эмиссионная томография — SPECT, лазер — допллер флоуметрия, тер мальная диффузионная флоуметрия [9, 13, И, 721;
-
непрямых методов оценки МК и мета болизма (югулярная венозная оксиметрия
-
SjvO2, транскраниальная Допплер соно- графия — ТКД, инфракрасная спектроско пия - N1RS [40, 48, 49, 50, 73];
3 — Мониторинг церебрального метаболизма,
с использованием для этих целей [2, 6, 24,
26, 36, 47, 51]:
— церебральной инфракрасной спектро скопии (N1RS);
-
югулярной венозной оксиметрии;
-
динамического измерения парциально го напряжения кислорода локально в тка ни мозга (PtiO2) — (Licox-система);
-
метода позитронно — эмиссионной то мографии (ПЭТ);
-
техники интрацеребрального микродиа лиза с мониторингом содержания глюкозы, лактата, глютамата, АТФ, гипоксантина;
-
определения артериовенозной разницы по кислороду (AVDO2) и метаболитам (глюкоза, лактат, пируват).
4 — Электро-, магнито- нейрофизиологичес-
кий мониторинг, включающий в себя \1',
27, 34, 56, 74]:
-
цифровую ЭЭГ и различные методы ее обработки (спектральный анализ, когерент ность, спектральное и амплитудное карти рование);
-
оценку вызванной активности мозга — вызванные потенциалы (ВП) (стволовые
211
Клиническое руководство по черепно-мозговой травме

акустические вызванные потенциалы — АСВП, соматосенсорные вызванные потенциалы — ССВП, зрительные вызванные потенциалы — ЗВП, магнитные (моторные) вызванные потенциалы — МВП и мульти вариантный мониторинг вызванных потенциалов — ММВП).
Методы, входящие в «золотой» стандарт мониторинга были нами рассмотрены ранее.
Непрерывное измерение ВЧД (эпи-, субду-рального, паренхиматозного, вентрикулярного — какого-либо из перечисленных), в сочетании с ин-вазивным измерением системного АД и, соответственно, получением результирующей величины церебрального перфузионного давления (ЦПД) позволяет мониторировать эпизоды возможной ишемии мозга.
В случае развития ВЧГ эпизоды снижения артериального давления, как правило, приводят к снижению ЦПД и уменьшению церебральной достав-
ки и насыщения кислородом вещества мозга, то есть к гипоксии мозга (рис. 8—2).
В связи с этим, в настоящее время, повсеместно принята концепция ведения больных с тяжелым травматическим поражением мозга, ориентированная на поддержание постоянного уровня ЦПД (не ниже 70 мм рт. ст.) [68]. Даже незначительное снижение АД и повышение ВЧД при тяжелом травматическом поражении мозга приводят к уменьшению ЦПД, обуславливая церебральную гипоксию из-за нарушенной ауторегуляции МК и церебральной доставки кислорода [73].
Нарушения мозгового кровообращения представляют собой один из ведущих факторов в патогенезе вторичного поражения мозга при тяжелой ЧМТ.
Известно, что церебральный вазоспазм приводит к снижению регионарной или тотальной церебральной перфузии и к увеличению артерио-венозного шунтирования крови. Развиваясь у приблизительно 30% пострадавших с тяжелой ЧМТ, сопровож-
212
Мультимодальный физиологический мониторинг при тяжелой черепно-мозговой травме
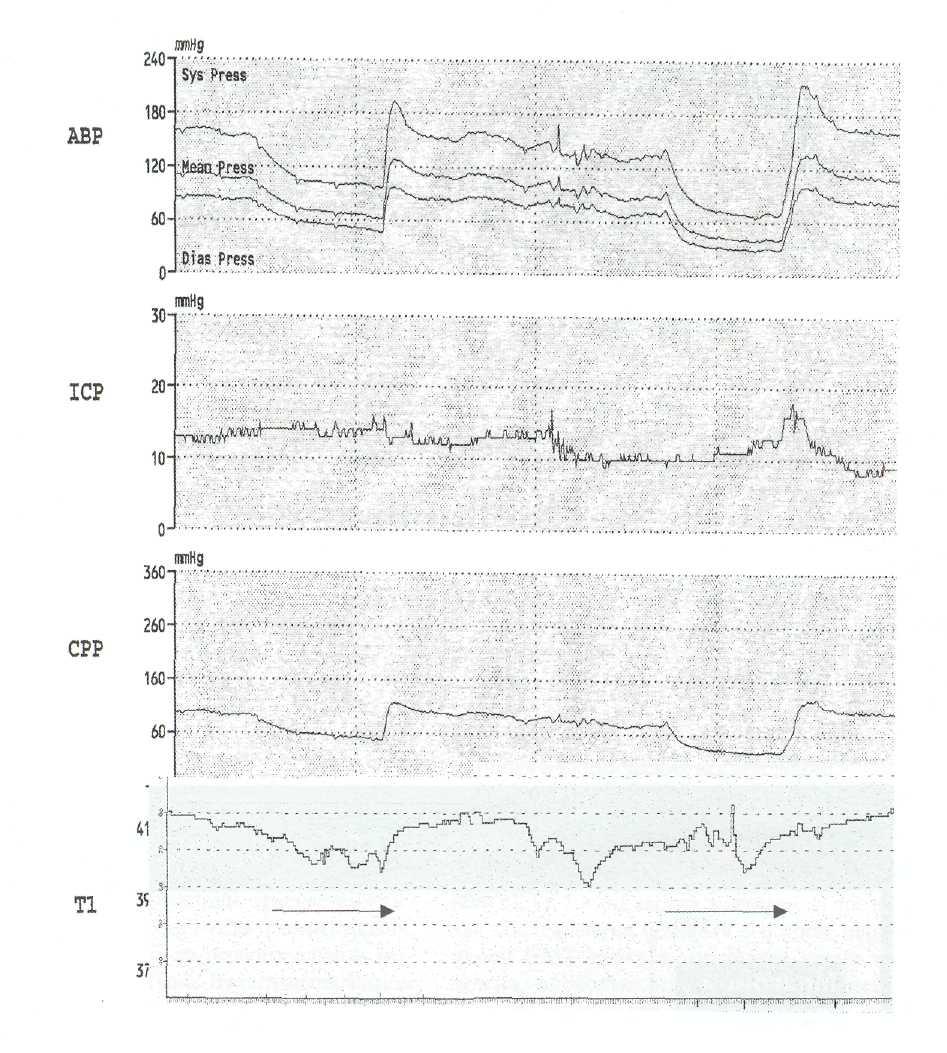
ICP — внутричерепное давление; СРР — церебральное перфузионное давление; г SO2 — коэффициент насыщения кислородом мозговой ткани по данным инфракрасной спектроскопии.
даемой массивным субарахноидальным кровоизлиянием церебральный вазоспазм является одними из ведущих патогенетических факторов вторичного ишемического поражения мозговой ткани [5, 23].
В тоже время, вазоплегия сосудов мозга приводя к острой церебральной гиперемии является одним из патогенетических механизмов повышения ВЧД[30].
213
Клиническое руководство по черепно-мозговой травме
8.1.1. Радиоизотопные
исследования мозгового кровотока
В норме, в состояние покоя, тотальный мозговой кровоток составляет 55 мл/100 г/мин. В последние два десятилетия, благодаря использованию много-детекторной радиоизотопной методики Лассена и Ингвара с Хе133 подробно изучены изменения МК при разнообразных физиологических и патологических состояниях. Были выделены два принципиально различных варианта нарушений мозгового кровообращения, идентифицируемых с помощью использования радиоизотопных методов исследования — гиперемия и олигемия мозга.
Механизмы регионарной вазодилатации (гиперемии) в остром периоде тяжелой ЧМТ до сих пор окончательно не установлены, однако известно, что этот патологический процесс приводит к увеличению объема ткани мозга, усиливая патологические проявления отека — набухания [30, 54].
В зонах гиперемии мозга развиваются нарушения ауторегуляции МК, проявляющиеся в виде утери возможности сохранять постоянство МК при изменениях артериального давления. В ходе клинического исследования наблюдается феномен пассивного следования МК изменениям системного артериального давления.
В то же время остается сохранной способность церебральных сосудов к сужению при изменении
парциального давления углекислого газа it кропи больного. Учитывая избирательную сохранность при этих процессах ауторегуляторного ответа на химический стимул (РаСО2), рядом авторов было предложено использовать кратковременную гипервентиляцию со снижением РСО2 до 28 мм рт. ст., для уменьшения выраженности гиперемии мозга и, соответственно, степени выраженности ВЧГ [58, 59]. '
Другим феноменом нарушения МК при тяжелой ЧМТ является его снижение, приводящее к ишемическому поражению головного мозга.
Известно, что благодаря механизмам ауторегуляции МК поддерживается на постоянном уровне в широких пределах колебаний системного артериального давления (от 60 до 180 мм рт. ст.) (рис. 8—3). Именно нарушение ауторегуляции МК при тяжелой ЧМТ приводит к общему снижению МК и снижению ЦПД ниже 70 мм рт ст в результате системной артериальной гипотензии на фоне повышения вчд.
Другой причиной, приводящей к снижению МК является спазм церебральных сосудов, уменьшающий кровоток ткани мозга ниже уровня метаболических потребностей (рис. 8—4).
Оба описанных патологических феномена МК — церебральная гиперемия и ангиоспазм встречаются при тяжелой ЧМТ приблизительно в равном проценте случаев, доминируя в разных фазах течения травматической болезни мозга.
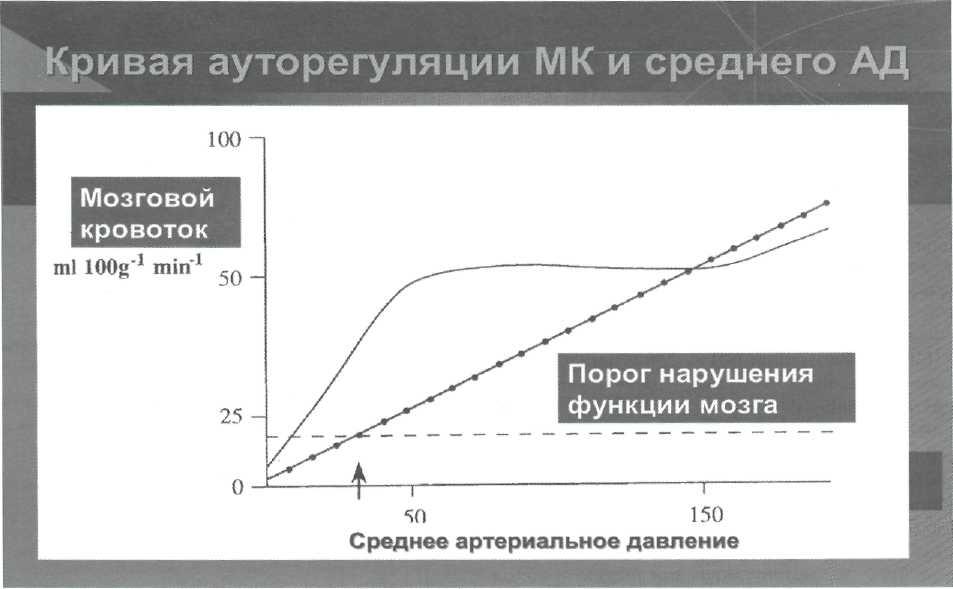
Рис. 8—3. Графическое представление взаимозависимости МК от величины среднего АД.
Мультимодалъныи физиологический мониторинг при тяжелой черепно-мозговой травме

Экспериментальные исследования [57], посвященные изучению характера нарушений МК при ЧМТ у животных показали, что непосредственно после травмы наблюдается повышение ВЧД, происходящее одновременно с быстрым ростом среднего АД (более 100 мм рт. ст.). Через 30 сек отмечается нормализация артериального давления. После этого отмечается увеличение МК в субкортикальных структурах и более значительно в неокортиксе лобных и височных долей мозга, таламусе и гипоталамусе. При локальном воздействии травмирующего фактора, в эксперименте на животных было отмечено, что через 2 мин в ипсилатеральном (по отношению к месту нанесения удара) полушарии отмечается снижение МК до 60% от исходного (до травмы) уровня. Восстановление кровотока до первоначальных значений отмечалось через 20 мин. В контралатеральном полушарии отмечено увеличение МК на 172% от исходного уровня наблюдаемое в течение 4 мин. Фаза гиперперфузии следовала за умеренной гипоперфу-зией (снижение МК до 78% от исходного уровня), которая отмечалась в течение 60 мин [60].
Учитывая все эти данные — динамическая оценка нарушений мозгового кровообращения в остром периоде ЧМТ приобретает чрезвычайно важное значение для формирования тактики патогенетически обоснованной интенсивной терапии.
Для исследования МК в остром периоде ЧМТ могут быть применены разные методы (см. выше), однако большинство из них трудоемки и не подходят для использования в условиях клинического нейромониторинга.
В 80-е годы для исследований М К широкое распространение получила многодетекторная радиоизотопная методика Лассена—Ингвара с использованием клиренса радиоизотопов технеция (Те99) и ксенона (Хе133). Хотя метод позволил получить ценные данные о характере нарушений МК при ЧМТ [65], сложность проведения и стоимость ограничили его применение небольшим количеством научных и клинических исследований.
В настоящее время эта методика практически вытеснена другими как то, позитронно эмиссионной томографией (ПЭТ) и однофотонно эмиссионной компьютерной томографией — SPECT (ОФЭКТ). Клиническая значимость последних — для обследования больных в остром периоде тяжелой ЧМТ также в настоящее время не определена, поскольку ни один из этих методов не является легко доступным для динамической оценки М К.
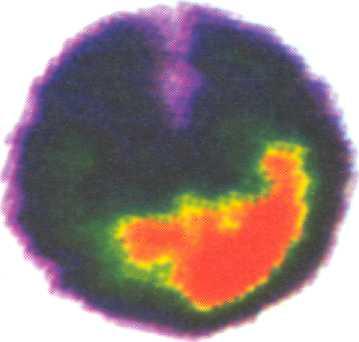
При использовании метода ОФЭКТ гамма-камера рассчитывает плотность сигналов, испускаемых ввнутривенно введенным фармпрепаратом. Результаты сканирования позволяют диагностировать ранние стадии региональной ишемии и степень ее выраженности.
ПЭТ позволяет получить информацию о состоянии регионарного мозгового кровообращения и метаболической активности мозга. Однако, необходимость работы с радионуклидами и высокая стоимость исследования объясняет тот факт, что они доступны только в ограниченном числе крупных научных центров.
215
8.1.2.Ультразвуковые
исследования мозгового кровотока
В настоящее время наиболее доступным для динамического исследования МК является метод транскраниальной Допплер сонографии (ТКД). Помимо неинвазивности и относительной простоты проведения исследования — ТКД, в отличие от ПЕТ или ОФЭКТ может быть использована для целей мониторинга МК при проведении интенсивной терапии. С определенными допущениями ТКД может быть использована также как метод неинвазивного контроля ВЧД. В свою очередь, линейная скорость кровотока (ЛСК), исследуемая с помощью ТКД, тесно зависит от величин АД, ВЧД, гематокрита, РаСО2, сохранности ауторегуляции мозгового кровотока и поэтому не может быть напрямую сопоставлена с данными о регионарном МК, полученными радиоизотопными методами.
ТКД отвечая критериям простоты и неинвазивности исследования, а также обладая возможностью непрерывного наблюдения за линейной скоростью кровотока наиболее адекватно соответствует целям и задачам прикроватного мониторинга МК при тяжелой ЧМТ. Метод является вспомогательным при оценке эффективности и адекватности проводимой интенсивной терапии на различных этапах посттравматического периода. Непрерывное мониторирование линейной скорости кровотока, включая метод непрерывной детекции эмболов дает возможность предотвратить ишемическос поражение мозга |42],
В настоящее время известно, что нарушения ауторегуляции МК коррелируют с неблагоприятными исходами при тяжелой ЧМТ. Показано, что у погибших пациентов нарушения ауторегуляции МК наблюдаются уже в первые двое суток после травмы [21, 22]. В связи с этим, по мнению Lee E.J. и соавт. [40], данные ТКД могут быть использованы для прогноза исхода при тяжелой ЧМТ. Авторами также была показана зависимость тяжести ги-поксического поражения мозга от выраженности и длительности церебрального ангиоспазма.
Goraj В. и соавт. [30] установили, что существует значимая корреляционная зависимость между индексом резистентности (соотношение между пульсовой и пиковой линейной скоростью МК — см. т. 1, с. 413 данного Руководства) по ТКД и ВЧД измеряемых на одноименной стороне.
Более детальное исследование сосудов основания мозга с их визуализацией можно провести используя методику цветного дуплексного сканирования, сочетающую в себе при применении одного прибора методику Би-сканирующего ультразвукового исследования (позволяющую получать изображение сосуда) и допплеровского анализа линейной скорости кровотока (рис. 8—5).
Характер нарушений линейной скорости кровотока (ЛСК) в остром периоде ЧМТ зависит от тяжести и вида (очаговое или диффузное) травматического поражения.
Поданным Chan и соавт. [14, 16] изучивших 121 больного с ЧМТ, средние показатели ЛСК были различными в зависимости от тяжести травмати-

Рис. 8—5. Дуплексное сканирование сосудов основания мозга
Мулыпимодальныи физиологический мониторинг при тяжелой черепно-мозговой травме
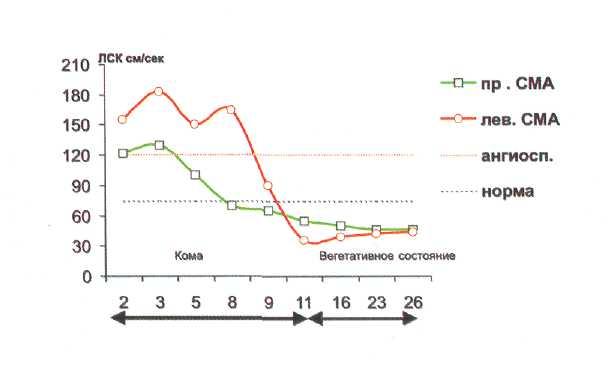
ческого поражения мозга. ЛСК в средней мозговой артерии (СМА) была ниже 35,8 см/сек при тяжелой ЧМТ, в пределах 45,5 см/сек при ЧМТ средней тяжести и 51,7 см/сек при легкой ЧМТ. При выходе из коматозного состояния у больных с тяжелой ЧМТ ЛСК в СМА достигала 46,2 см/сек. Постоянно выявляемые низкие величины ЛСК наблюдались у больных погибших в течение 72 часов после травматического поражения мозга. ЛСК меньше чем 28 см/сек, наблюдалась в 80% случаев с ранним летальным исходом после ЧМТ (рис. 8—6). Постоянно выявляемые низкие величины ЛСК наблюдались у больных погибших в течение 72 часов после травматического поражения мозга. По данным этих авторов у 90% больных с тяжелой ЧМТ наблюдаются ишемические поражения мозга.

Рис. 8—6. Снижение ЛСК ниже 28 см/сек рассматривается как неблагоприятный признак в остром периоде тяжелой ЧМТ.
Помимо низких величин ЛСК другим неблагоприятным прогностическим признаком для исхода острого периода ЧМТ являются грубые нарушения ауторегуляции МК.
Так, нарушения ауторегуляции МК, наблюдающиеся в первые два дня острого периода после тяжелой ЧМТ соответствуют летальному исходу в течение 7—10 суток после травмы у 90% пациентов [15, 17].
Нарушения МК при ЧМТ, как правило, имеют фазное течение [43].
Фаза I — гипоперфузии, наблюдается непосредственно после ЧМТ и характеризуется снижением МК до 32,2 мл/100 г/мин, при нормальной ЛСК в СМА (56,7 см/сек), нормальном полушарном индексе СМА/ ВСА — 1,67 и нормальной церебральной артерио — венозной разницей по кислороду (AVDO2) — 5,4.
Фаза II (гиперемическая) наблюдается в 1—3 сутки после ЧМТ. Характеризуется повышением МК (46,8 мл/100 г/мин), снижением AVDO2 до 3,8 мл/ 100мл, увеличением ЛСК (более 86 см/сек), полу-шарным индексом СМА/ВСА меньше 3.
Фаза III (ангиоспастическая) наблюдается на 4—15 сутки после травмы. Характеризуется снижением МК до 35,7 мл/100 г/мин, дальнейшим повышением ЛСК (96,7 см/сек), при полушарном индексе больше 3.
С учетом наиболее часто встречающегося при тяжелой ЧМТ феномена изменения МК в виде повышения линейной скорости кровотока (ЛСК) в бассейне средней мозговой артерии (СМА) [17, 79], как правило, проводится дифференциальная диагностика его причинного фактора, которым в 40% случаев является ангиоспазм а, в приблизительно 30% — церебральная гиперемия. Дифференциально диагностическим признаком может служить показатель полушарного индекса, получаемое как соотношение ЛСК в средней мозговой и внутренней сонной артерии СМА/ВСА. При церебральном вазоспазме полушарный индекс становится выше 3.
Следует отметить, что более высокие, длительно сохраняющиеся значения цифр ЛСК остаются при церебральном вазоспазме, нежели при гиперемии мозговых сосудов, чаще соответствуя очаговому травматическому поражению мозга (рис. 8—7), в том числе по данным КТ.
Триггерную роль очагов травматического размоз-жения в генезе вазоспазма в остром периоде после тяжелой ЧМТ предположили Onuma Т. и соавторы [63].
Одновременная регистрация ЛСК и уровня насыщения кислородом мозговой ткани (методом инфракрасной спектроскопии) выявляют значительную вариабельность последнего показателя, возрастающую по мере возрастания ЛСК.
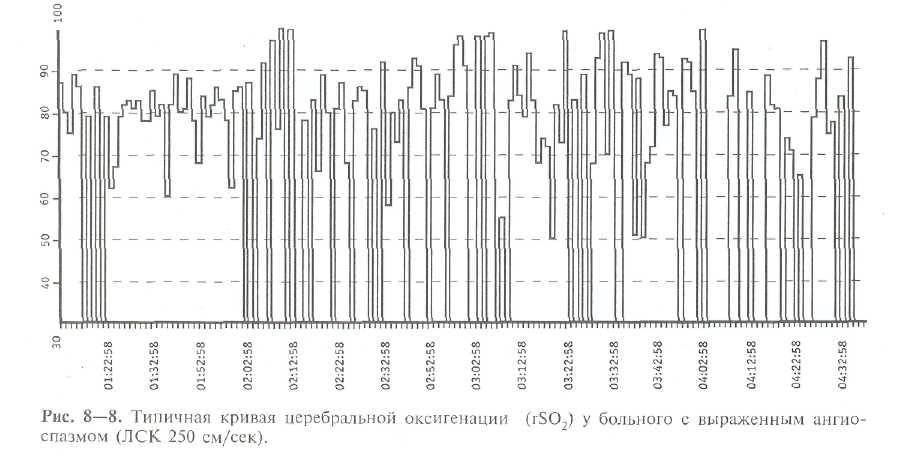
Колебания коэффициента насыщения кислородом вещества мозга (rSO2) по данным церебральной оксиметрии составляли более 50%, характерный вид оксиметрической кривой в виде «частокола» приведен на рис. 8—8.
Обычно снижение значений ЛСК в СМА при очаговых поражениях мозга наблюдают в период времени, соответствующий выходу больных из комы в состояние измененного сознания (8—9 баллов по шкале комы Глазго). Постепенная нормализация ЛСК отмечается в этих случаях к исходу 1 месяца после ЧМТ.
Повышение ЛСК при диффузном травматическом поражении мозга, наоборот, в большинстве
217
Клиническое руководство по черепно-мозговой травме

случаев, расценивается как гиперемия (средняя ЛСК>120 см/сек, полушарнътй индекс <1.8).
По данным Muttaqin и соавт. [54] острая посттравматическая гиперемия мозга встречается в 30% наблюдений у больных с диффузным травматическим поражением головного мозга, приводя к повышению ВЧД. Результаты исследования показали, что после ЧМТ в течение 48—96 часов наблюдается быстрое повышение ЛСК и снижение пульсового индекса (ПИ). Эти изменения коррелируют с повышением ВЧД. Рост ВЧД сопровождется повышением индекса резистентности (ИР). Между ИР и ВЧД существует прямая корреляционная зависимость.
Важно отметить, что ангиоспазм после тяжелой ЧМТ развивается между 2 и 8 сутками и, как правило, не наблюдается в первые сутки после травмы [69].
Паралельное исследование методом ТКД и по клиренсу Хе-133 показали, что у 3 из 5 больных с верифицированными ангиоспазмом (ЛСК в СМА больше чем 120 см/сек, полушарный индекс больше 3) наблюдается снижение МК [37].
В группе больных с массивными очагами травматического размозжения — вазоспазм более длителен и интенсивен по выраженности, повышение ЛСК достигает у отдельных больных 200 см/сек и более (срЛСК в СМА 188.2 ± 9.3 см/сек, РаСО = 33.3 ± 2.3
218
Мультимодалъный физиологический мониторинг при тяжелой черепно-мозговой травме
мм.рт.ст, полушарный индекс СМА/ВСА = 3.8 ± 0.2) (рис. 8—9). Изменения ЛСК имеют характер регионарных нарушений (асимметрии ЛСК составляют 30-40%).
Могут отмечаться колебания ЛСК в виде так называемых В-волн, что свидетельствует о нарушениях ауторегуляции сосудистого тонуса, пассивном следовании ЛСК изменениям ВЧД [76]. Лока-

лизация В-волн обычно соответствует стороне очаговых ишемических нарушений (рис. 8—10).
Newell D.W. и соавторы [59] установили корреляционную зависимость В-волн при регистрации ВЧД и флюктуации величин ЛСК в СМА. Это позволило им предположить, что В-волны, выявляемые при регистрации ВЧД являются вторичным эффектом вазомоторных волн, на фоне снижения упруго-эластических свойств ткани мозга.
Одновременное проведение у этих больных ОФЭКТ исследования установило, что в 85% случаев повышению ЛСК сопутствуют олегимические расстройства МК. У больных с билатеральным повышением ЛСК выше 220 см/сек по данным ОФЕКТ выявлялась билатеральная церебральная ишемия [67]. В дальнейшем, как правило, снижению ЛСК соответствовало формирование состояния тяжелой инвалидизациия с оценко по шкале

Рис. 8—10. Регистрация В — волн соответствует стороне и шем и чес ко го поражения мозга по данным ОФЭКТ.
219
Клиническое руководство по черепно-мозговой травме

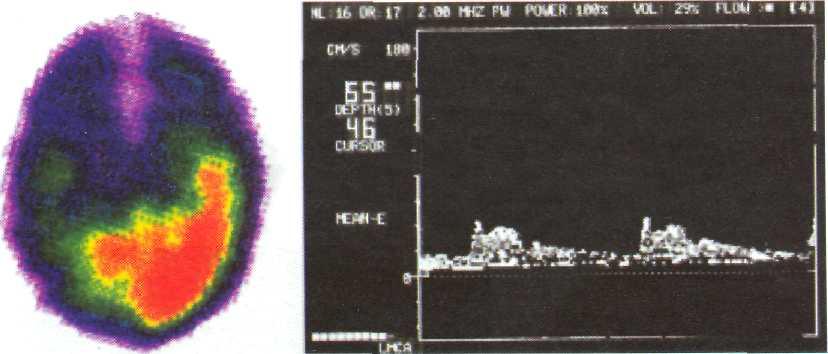
исходов Глазго (рис. 8—11). При этом отмечено, что в полушарии с более низкими величинами ЛСК отмечается повышение концентрации кислорода более 80%, что, вероятно, свидетельствует об
уменьшении экстракции кислорода веществом мозга. Стороне снижения ЛСК клинически, по данным КТ и ОФЭКТ соответствовал очаг ишемичес-кого поражения (рис. 8—12).
8.1.3. Лазерная допперовская флоуметрия
Новые данные о состоянии цереброваскулярного резерва у больных с тяжелой ЧМТ были получены с помощью инвазивной лазерной допплеровской флоуметрии (ЛДФ).
Lam J.M. и соавт. [38] показали существование прямой линейной зависимости между изменениями ЛДФ и церебрального перфузионного давления (1ДПД), что можно использовать как индикатор нарушений ауторегуляции мозгового кровотока. Использование ЛДФ позволило выявлять сохран-
220
Мультимодалъный физиологический мониторинг при тяжелой черепно-мозговой травме

Рис.
8—13. Схематическое изображение процесса
неинвазивной ЦО с помощью накожного
сенсора.

8.1.4. Инфракрасная спектроскопия
Инфракрасная спектроскопия мозга (NIRS), является сравнительно новым методом непрерывного и неинвазивного мониторинга церебральной оксигснации [5].
В основе метода церебральной оксиметрии (ЦО) лежит принцип оптической спектроскопии с применением инфракрасного света с диапазоном от 650 до 1100 нм, который проникает через скальп, кости свода черепа и мозговое вещество и избирательно поглощается специфическими молекулами хромофоров, к которым относятся окси- и дезок-сигемоглобин, цитохром-С-оксидаза и некоторые другие (рис. 8 — 13). Показанное на рисунке расположение улавливающих отраженный свет фотодетекторов позволяет определять изолированно ту часть светового пучка, которая отражается от кости и экстрацеребральных тканей и ту часть — которая отражается от церебральных структур (ткань мозга и церебральные сосуды). Использование специальных расчетов позволяет автоматически вычленить экстрацеребральный компонент и таким образом определить насыщение кислородом в подлежащем участке мозга.
