
- •В.Г. Крыштоп, н.И. Филиппова основы атомнОй и ядернОй физикИ
- •Введение
- •1. Тепловое излучение
- •2. Фотоэффект
- •3. Тормозное рентгеновское излучение
- •Эффект Комптона
- •Примеры решения задач
- •Проектное задание
- •Модуль 1. Полуклассические теории строения атома Комплексная цель модуля
- •1.1. Первая физическая модель атома – модель Томпсона
- •1.2. Опыт Резерфорда. Планетарная модель атома.
- •1.3. Спектральные закономерности
- •1.4. Постулаты Бора. Опыты Франка и Герца
- •1.5. Боровская модель атома водорода
- •1.6. Магнитный момент атома водорода
- •1.7. Гипотеза де-Бройля
- •1.8. Принцип неопределенности
- •1.9. Примеры решения задач
- •Выполните следующие задания
- •1.10. Тесты рубежного контроля
- •1.10. Принципы оценивания
- •Модуль 2. Основы квантовой механики Комплексная цель модуля
- •2.1 Уравнение Шредигера
- •2.2. Частица в прямоугольной яме
- •2.3. Потенциальные барьеры
- •2.4. Туннельный эффект.
- •2.5. Квантование момента импульса
- •2.6. Атом водорода
- •2.7. Спин электрона
- •2.8. Полный момент импульса электрона.
- •2.9. Примеры решения задач
- •2.10. Тесты рубежного контроля
- •2.11. Принципы оценивания
- •Заключение
- •Ответы на тесты рубежного контроля
- •Литература
- •Содержание
2.9. Примеры решения задач
Задача 1. Частица находится в основном состоянии в одномерной прямоугольной потенциальной яме шириной I с абсолютно непроницаемыми стенками (0 < х < I). Найти вероятность местонахождения частицы в интервале (//3, 21/3).
Решение.
Согласно
(2.12) Ψ-функция
в основном состоянии (п = 1) это
Ψ =
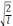
 sin(x/l).
Искомая вероятность
sin(x/l).
Искомая вероятность

где введена новая переменная у = пх/1.
Задача 2. Частица массы т находится в основном состоянии в одномерной прямоугольной потенциальной яме с абсолютно непроницаемыми стенками. Максимальное значение плотности вероятности местонахождения частицы в этом состоянии равно Рт. Найти ширину ямы и энергию Е частицы.
Решение.
Воспользовавшись выражением (2.12) для Ψ-функции, запишем плотность вероятности Р(х) для основного состояния (п = 1):

Эта величина максимальна в середине ямы, т. е. при х = 1/2. Поэтому

Отсюда находим I = 2/Рт и согласно (2.11)
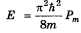
Задача 3. Электрон атома водорода находится в стационарном состоянии, описываемом волновой функцией у(г) = Ае~аг, где А и а — некоторые постоянные. Найти энергию Е электрона и постоянную а.
Решение.
В
данном случае уравнение Шредингера
(2.6) будет иметь
вид
(1)
Вычислив первую и вторую производные Ψ-функции по г, подставим их выражения в (1) и сгруппируем следующим образом:

(2)
Из этого соотношения видно, что равенство его нулю при любых значениях г возможно лишь в том случае, когда обе скобки по отдельности равны нулю. Отсюда
 .
.
2.10. Тесты рубежного контроля
1. Электронная конфигурация кобальта, у которого 27 электронов, в основном состоянии
(1) 1s2 2s2 2p6 3s2 3p63d74p2
(2) 1s2 2s2 2p6 3s2 3p63d84s2
(3) 1s2 2s2 2p6 3s2 3p63d9
(4) 1s2 2s2 2p6 3s2 3p63d74s2
2. . Если волновые свойства частицы трудно наблюдать, то это происходит из-за
(1) маленьких размеров
(2) большой массы
(3) маленького импульса
(4) большого заряда
3. Какое из утверждений неверно?
(1) волновая функция всегда действительна
(2) волновая функция полностью описывает состояние системы
(3) волновая функция конечна, однозначна, непрерывна вместе с первой производной
(4)
В одномерном случае должно выполняться

4. Кратность вырождения энергии водородоподобного атома с главным квантовым числом n.
(1) 2n
(2) 2n2
(3) 2n3
(4) 2(2l+1)
5. Среди переходов правилами отбора запрещены следующие
I 2P3/2->2S1/2 II 2F7/2->2D5/2 III 2F5/2->2P3/2
(1) Только I
(2) Только II
(3) Только III
(4) II и III
6. Какая из нижеследующих функций может быть радиальной волновой функцией электрона в атоме водорода? (А и b - постоянные)
I. A e- b r II. A sin(br) III. A/r
(1) Только I
(2) Только II
(3) Только I и II
(4) I, II, и III
7. Электронная конфигурация основного состояния фосфора, у которого 15 электронов
(1) 1s2 2s2 2p6 3s1 3p4
(2) 1s2 2s2 2p6 3s2 3p3
(3) 1s2 2s2 2p6 3s2 3d3
(4) 1s2 2s2 2p6 3s1 3d4
2.11. Принципы оценивания
При правильном ответе на 7 вопросов теста оценка – «5»;
при правильном ответе на 5 или 6 вопросов теста оценка – «4»;
при правильном ответе на 3 или 4 вопроса теста оценка – «3»;
при правильном ответе на 2 и менее вопросов теста оценка-«2».
