
- •В.Г. Крыштоп, н.И. Филиппова основы атомнОй и ядернОй физикИ
- •Введение
- •1. Тепловое излучение
- •2. Фотоэффект
- •3. Тормозное рентгеновское излучение
- •Эффект Комптона
- •Примеры решения задач
- •Проектное задание
- •Модуль 1. Полуклассические теории строения атома Комплексная цель модуля
- •1.1. Первая физическая модель атома – модель Томпсона
- •1.2. Опыт Резерфорда. Планетарная модель атома.
- •1.3. Спектральные закономерности
- •1.4. Постулаты Бора. Опыты Франка и Герца
- •1.5. Боровская модель атома водорода
- •1.6. Магнитный момент атома водорода
- •1.7. Гипотеза де-Бройля
- •1.8. Принцип неопределенности
- •1.9. Примеры решения задач
- •Выполните следующие задания
- •1.10. Тесты рубежного контроля
- •1.10. Принципы оценивания
- •Модуль 2. Основы квантовой механики Комплексная цель модуля
- •2.1 Уравнение Шредигера
- •2.2. Частица в прямоугольной яме
- •2.3. Потенциальные барьеры
- •2.4. Туннельный эффект.
- •2.5. Квантование момента импульса
- •2.6. Атом водорода
- •2.7. Спин электрона
- •2.8. Полный момент импульса электрона.
- •2.9. Примеры решения задач
- •2.10. Тесты рубежного контроля
- •2.11. Принципы оценивания
- •Заключение
- •Ответы на тесты рубежного контроля
- •Литература
- •Содержание
2.6. Атом водорода
Рассмотрим простейшую систему, состоящую из электрона е, который движется в кулоновском поле ядра с зарядом Ze. Такую систему называют водородоподобной. При Z = 1 это атом водорода, при Z = 2 — однократно ионизированный атом гелия — ион Не+, при Z = 3 — двукратно ионизированный атом лития — ион Li++ и т. д.
Потенциальная энергия взаимодействия электрона с ядром в такой системе равна

(6.29)
где г — расстояние между электроном и ядром, которое в первом приближении будем считать точечным (здесь и далее). Уравнение Шредингера в этом случае имеет вид

(6.30)
Поле (2.29), в котором движется электрон, является центрально-симметричным, т. е. зависит только от г. Поэтому решение уравнения (2.30) наиболее целесообразно проводить в сферической системе координат г, 9, ср, где оператор Лапласа V2 имеет следующий вид

(6.31)
Мы не будем воспроизводить здесь этапы решения уравнения (2.30), поскольку оно слишком громоздко (об этом красноречиво свидетельствует уже сам вид оператора Лапласа). Остановимся лишь на сути процесса решения и на анализе окончательных результатов
Решение уравнения (2.29) проводят методом разделения переменных с учетом естественных требований, налагаемых на Ψ-функцию: она должна быть однозначной, конечной, непрерывной и гладкой. В процессе решения обнаруживается, что этим требованиям можно удовлетворить при любых положительных значениях энергии £, нов области отрицательных значений Е — только при дискретных значениях Е, а именно, если

п = 1, 2, 3, … (2.32)
Этот случай (Е < 0) для нас представляет особый интерес, поскольку он соответствует связанным состояниям электрона.
Таким образом, последовательное решение уравнения Шре-дингера приводит в случае Е < 0 к формуле (6.4) для энергетических уровней — без использования каких-либо дополнительных постулатов (в отличие от первоначальной теории Бора). Кроме того, совпадение с формулой (2.25) означает, что мы пришли к той же самой системе энергетических уровней (см. рис. 2.7). Это же относится и к частотам излучения при переходах между уровнями. Поэтому повторять нет необходимости.
Различие в интерпретации относится только к состояниям электрона: в теории Бора это движение по стационарным орбитам, здесь же орбиты теряют физический смысл, их место занимают ^-функции.
Собственные функции уравнения (2.28), т. е. ^-функции, содержат, как выяснилось, три целочисленных параметра — п, I, т:
Ψ = Ψnlm(r, θ, φ) (2.33)
где п называют главным квантовым числом (это то же п, что и в выражении для Еп). Параметры же I и т — это орбитальное и магнитное квантовые числа, определяющие по формулам (5.25) и (5.26) модуль момента импульса М и его проекцию Мг. В процессе решения выясняется, что решения, удовлетворяющие* естественным условиям, получаются лишь при значениях I, не превышающих п - 1. Таким образом, при данном л квантовое число I может принимать п значений:
l = 0, 1, 2, ... ,п- 1. (2.34)
В свою очередь, при данном I квантовое число т согласно (2.21) может принимать 21 + 1 различных значений:
т=0,±1, ±2, ..., + 1. (2.35)
Энергия Еп электрона (6.4) зависит только от главного квантового числа п. Отсюда следует, что каждому собственному значению Еп (кроме случая п = 1) соответствует несколько собственных функций ц1П1т, отличающихся значениями квантовых чисел I и т. Это означает, что электрон может иметь одно и то же значение энергии, находясь в нескольких различных состояниях. Например, энергией Ег (п = 2) обладают четыре состояния: Ψ200, Ψ2i-i, Ψ210, Ψ21+1-.
Символы состояний. Различные состояния электрона в атоме принято обозначать малыми буквами латинского алфавита в зависимости от значения орбитального квантового числа I
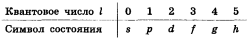
(2.36)
Принято говорить о s-состояниях (или s-электронах), р-состоя-ниях (или р-электронах) и т. д.
Значение главного квантового числа п указывают перед символом состояния с данным I. Например, электрон, имеющий главное квантовое число п = 3 и I = 2, обозначают символом 3d и т. д. Выпишем последовательно несколько состояний электрона:
Is; 2s, 2p; 3s, Зр, 3d; ... (2.37)
Собственные функции уравнения (2.28) представляют собой произведение двух функций, одна из которых зависит только от г, а другая — только от углов θ и φ:
 (2.38)
(2.38)
где первый сомножитель зависит от квантовых чисел п и I, второй же — от I и т.
