
vse_metody_MIKROB
.pdfПРАКТИЧЕСКАЯ РАБОТА
Выделение чистой культуры аэробов.
I этап исследования. Посев смеси бактерий (S.aureus+E.coli) на пластин-
чатый МПА в чашке Петри петлей секторами.
Этапы посева:
а) на дне чашки Петри с МПА карандашом по стеклу сделать надпись: но-
мер стола, номер группы, факультет;
б) прокалить петлю, над спиртовкой открыть пробирку, обжечь ее края,
внести петлю в пробирку и остудить ее о стенки пробирки. Забрать пет-
лей исследуемый материал. Закрыть пробирку над спиртовкой и поста-
вить в штатив;
в) взять чашку Петри, приоткрыть крышку и нанести петлей секторами ис-
следуемый материал на МПА, закрыть чашку, прожечь петлю;
г) посевы поставить в термостат при температуре 37°С на 24 часа.
15
Занятие №6
Тема. Рост и размножение бактерий. Выделение чистой культуры аэробов.
Влияние физических и химических факторов на микроорганизмы. Методы сте-
рилизации. Дезинфекция. Асептика. Антисептика.
Цель занятия. Изучить рост и размножение бактерий, действие физических и химических факторов на микроорганизмы, методы стерилизации, дезинфекции и антисептики. Освоить второй этап бактериологического исследования по выделению чистой культуры аэробов.
I.Теоретические знания:
1.Рост и размножение бактерий.
2.Характеристика роста бактериальной популяции на плотных и жидких пита-
тельных средах.
3.Фазы развития бактериальной популяции в жидкой питательной среде.
4.Влияние факторов окружающей среды на микроорганизмы.
5.Виды дезинфекции. Химические вещества, используемые для дезинфекции.
6.Асептика. Антисептика. Химические вещества, используемые для антисептики.
II.Практические навыки и знания:
1.Проведение II этапа бактериологического метода исследования по выделе-
нию чистой культуры аэробов.
2.Действия медицинского работника при аварийных ситуациях (угроза зара-
жения ВИЧ).
1
МЕТОДИЧЕСКИЕ УКАЗАНИЯ К ЗАНЯТИЮ
1. Рост и размножение бактерий.
Рост бактерий – это увеличение линейных размеров и массы микробной
клетки.
Размножение бактерий – это увеличение количества особей в популяции за счет поперечного деления, реже путем почкования.
Интервал времени, за который число клеток удваивается, называется време-
нем генерации (Т-генерации). Для большинства бактерий время генерации со-
ставляет 20-30 мин., у возбудителя туберкулеза – 24 часа.
Популяция бактерий – совокупность особей одного вида, сформировавшаяся в определенных условиях внешней среды.
2. Характеристика роста бактериальной популяции на плотных и жидких
питательных средах.
Популяция бактерий, развившаяся из одной микробной клетки на плотной питательной среде, называется колонией.
Культура бактерий – популяция одного вида микроорганизмов.
Для учета количества жизнеспособных клеток в культуре определяют число
колониеобразующих единиц в 1 мл материала (КОЕ/мл).
Колонии характеризуют по следующим признакам:
1)по размеру: мелкие - 1-2 мм; средние - 2-4 мм; крупные - более 4 мм;
2)по форме: круглые или неправильной формы;
3)по рельефу: выпуклые, уплощенные;
4)по характеру поверхности: гладкие или шероховатые;
5)по характеру краев: ровные, изрезанные, волнистые;
6)по оптическим свойствам: прозрачные, полупрозрачные, непрозрачные;
7)по цвету: бесцветные или пигментированные (золотистые, красные, сине-
зеленого цвета и др.);
8)по запаху, например, колонии синегнойной палочки имеют запах жасми-
2
на, фиалки, карамели;
9) по консистенции: сухие, влажные, слизистые.
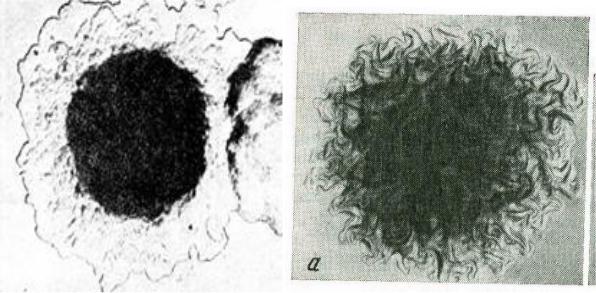
Гладкие колонии с ровными краями обозначаются как «S»-колонии (англ. smooth – гладкие), шероховатые с изрезанными краями - «R»-колонии (англ. rough – шероховатые). Внешний вид колоний у некоторых бактерий настолько характерен, что может служить одним из дифференциальных признаков при их идентификации. Например, R-колонии возбудителя чумы (Yersinia pestis) срав-
нивают с «кружевными платочками», т.к. они имеют плотный центр и прозрач-
ные волнистые края, R-колонии возбудителя сибирской язвы (Bacillus anthracis)
напоминают «гриву льва».
Возбудитель чумы (Yersinia pestis), |
Возбудитель сибирской язвы |
|
R-колонии на МПА |
(Bacillus anthracis), R-колонии на МПА |
|
Характер роста микроорганизмов в жидкой питательной среде зависит от
скорости деления и типа дыхания бактерий и может быть:
1)диффузно-мутящий (Staphylococcus aureus, Escherichia coli);
2)придонный или придонно-пристеночный (Streptococcus pyogenes);
3)поверхностно-пленчатый (Vibrio choleraе, Mycobacterium tuberculosis).
3
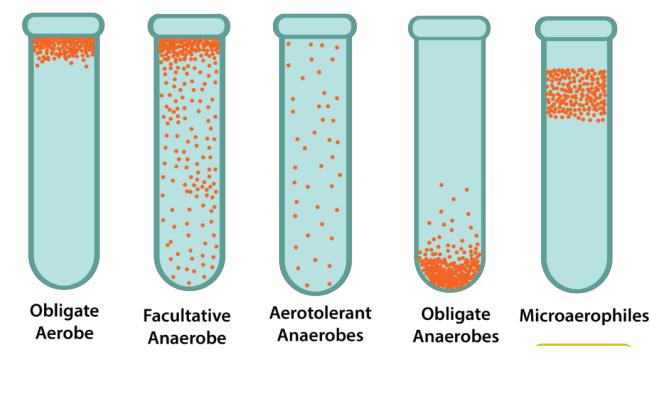
Рост микроорганизмов в жидкой питательной среде.
Некоторые виды возбудителей дают характерный тип роста в жидкой пита-
тельной среде. Например, Y.pestis образует на поверхности пленку со спускаю-
щимися вниз тяжами (нитями) - «чумные сталактиты»; B.anthracis образует придонный осадок в виде «комочка ваты».
3. Фазы развития бактериальной популяции в жидкой питательной среде.
I – лаг-фаза (от англ lag – отставать) – начальная фаза от момента посева бактерий до начала размножения. Бактерии адаптируются к новым условиям обитания.
II – экспоненциальная (логарифмическая) фаза. Характеризуется макси-
мальной скоростью деления клеток, которая зависит от вида бактерий.
III – стационарная фаза. Характеризуется равновесием между количеством погибающих и вновь образующихся клеток. В эту фазу количество живых бак-
терий в популяции достигает максимальной концентрации.
4
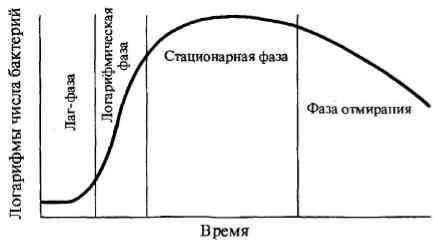
IV – фаза отмирания. Характеризуется гибелью бактерий вследствие исто-
щения питательной среды и других факторов.
Непрерывное культивирование с накоплением бактериальной массы ис-
пользуется в биотехнологических процессах и на микробиологических произ-
водствах (получение бактерийных препаратов).
Фазы развития бактериальной популяции
вжидкой питательной среде
4.Влияние факторов окружающей среды на микроорганизмы.
Физические, химические и биологические факторы окружающей среды оказывают различное воздействие на микроорганизмы: бактерицидное – при-
водящее к гибели клеток; бактериостатическое – подавляющее размножение;
мутагенное – изменяющее наследственные свойства бактерий.
Влияние физических факторов на микроорганизмы.
Методы стерилизации. Аппаратура.
1. Ультразвук. Под его действием в цитоплазме бактерий образуются ка-
витационные полости, заполненные парами жидкости под высоким давлением до 10 000 атм. Это приводит к разрушению цитоплазматических и оболочечных структур клетки. Практическое применение: для стерилизации вакцин, жид-
ких пищевых продуктов и др.
5

2. Ультрафиолетовый свет – повреждает ДНК микробной клетки. Дейст-
вие УФ-света на бактерии было доказано опытом Бухнера: в чашку Петри с МПА делают посев культуры микроорганизмов, например, S.typhi «сплошным газоном». На посев накладывают черную бумагу с вырезанными буквами, со-
ставляющими какое-либо слово, например, «typhus» и подвергают его дейст-
вию прямых солнечных лучей в течение 1 часа. После этого черную бумагу снимают и ставят чашку на сутки в термостат при температуре 370С. Рост куль-
туры микробов наблюдается только на тех участках среды, которые были за-
щищены от действия УФ-лучей. Практическое применение УФ-лучей: сте-
рилизация воздуха в операционных, родильных залах, палатах для новорож-
денных, в бактериологических лабораториях и др.
Опыт Бухнера с культурой S.typhi
3. Гамма-излучение вызывает повреждение белков и нуклеиновых кислот мик-
робной клетки (микробицидное действие). Практическое применение: для стерили-
зации одноразовых шприцев, одноразовой пластиковой микробиологической посуды,
перевязочного материала, систем для переливания крови.
4. Высокая температура – вызывает денатурацию белков и инактивацию ферментов микроорганизмов. Практическое применение: для стерилизации
различных объектов.
Стерилизация или обеспложивание (лат. sterilis - бесплодный) – полное уничтожение всех микроорганизмов и их спор в различных объектах (хирурги-
ческие инструменты, перевязочный материал, питательные среды и др.).
6

Методы стерилизации:
I. Физический:
1. Прокаливание в пламени спиртовки. Этот способ имеет ограниченное применение, в частности, для стерилизации бактериологических петель.
2. Сухим жаром в печи Пастера (воздушный стерилизатор). Режим сте-
рилизации: 180°С, 1 час. Стерилизуют стеклянную посуду (чашки Петри, пи-
петки, пробирки), хирургические инструменты.
3. Паром под давлением в автоклаве.
Параметры автоклавирования выбирают в зависимости от свойств мате-
риала. Чаще используют следующие режимы: 1 атм (1210С), 1,5 атм (1250С),
7

2 атм (1340С). При таких режимах вегетативные формы микробов погибают в течение нескольких минут, а споры за 20-30 минут.
Способ автоклавирования основан на том, что образующийся при кипении воды пар не выходит наружу, а, скапливаясь в замкнутом пространстве, повы-
шает давление. Соответственно давлению увеличивается и температура кипе-
ния воды. Тепло, генерируемое при повышении давления, называется латент-
ным теплом, оно имеет большую проникающую способность, разрушающую структуру микроорганизмов и спор.
4. Стерилизация УФ-облучением. Применяется для стерилизации возду-
ха в микробиологических лабораториях, родильных залах, палатах для новоро-
жденных, операционных, процедурных кабинетах и др. Ее проводят ультра-
фиолетовыми бактерицидными лампами различной мощности.
8
II. Химический метод стерилизации основан на использовании токсичных газов: оксида этилена, формальдегида и др. Эти вещества инактивируют фер-
менты и нуклеиновые кислоты микроорганизмов. Химическая стерилизация проводится в специальных камерах при температуре газа от 20 до 600С. Прак-
тическое применение: стерилизация оптических приборов, предметов меди-
цинского назначения из полимерных материалов.
III. Механический метод стерилизации (фильтрование) основан на меха-
нической задержке микроорганизмов и их спор мелкопористыми фильтрами с определенным диаметром пор. В микробиологической промышленности и в ла-
бораторной практике широко применяется фильтрация материала через асбе-
стовые и нитроцеллюлозные фильтры. Фильтрование используют для стерили-
зации биологических препаратов, не выдерживающих нагревания (сывороточ-
ные препараты, антибиотики, бактериальные экзотоксины и др.).
5. Виды дезинфекции. Химические вещества, используемые для де-
зинфекции.
Дезинфекция (от франц. приставки des и лат. infectio – заражение) – это комплекс мероприятий, направленных на уничтожение и удаление возбудите-
лей инфекции из объектов окружающей среды. Дезинфекция отличается от сте-
рилизации по конечному результату. Путем стерилизации уничтожаются все виды микроорганизмов и их споровые формы. При дезинфекции погибают
только вегетативные формы болезнетворных микроорганизмов.
Для проведения дезинфекции обычно используют химические дезинфици-
рующие средства. Выбор дезинфицирующего средства, а также способ его применения определяются особенностями обеззараживаемого объекта и биоло-
гическими свойствами материала.
Различают профилактическую, текущую и заключительную дезинфек-
цию.
9
