
- •1. Экзаменационные вопросы
- •Уровни организации ферментов.
- •Механизм действия ферментов. Понятие об активном центре фермента, этапы ферментативного катализа.
- •Кинетика ферментативных реакций. Зависимость скорости ферментативной реакции от различных факторов. Уравнение Михаэлиса-Ментен, роль Кm и Vmax в характеристике фермен- тов.
- •Ингибиторы ферментов. Типы ингибирования. Графическое представление зависимости скорости ферментативной реакции от присутствия ингибиторов различных типов.
- •Механизмы регуляции активности ферментов. Примеры.
- •Аллостерические ферменты. Регуляция их активности. При- меры.
- •Энзимодиагностика. Энзимотерапия. Примеры.
- •Введение в обмен веществ. Биологическое окисление
- •Важнейшие признаки живой материи. Особенности живых организмов, как открытых термодинамических систем.
- •1 Закон термодинамики:
- •2 Закон термодинамики:
- •4.Представление о биологическом окислении. Сопряжение экзергонических и эндергонических процессов в организме (на примере фосфорилирования глюкозы).
- •7. Окислительное фосфорилирование: сущность, биологическое значение процесса.
- •9. Окислительное декарбоксилирование пировиноградной кислоты: схема процесса, связь с синтезом атф. Строение пируватдегидрогеназного комплекса: ферменты, коферменты, регуляция процесса.
- •Обмен углеводов
- •1 Схема-
- •2 Схема-
- •3 Этап оу – промежуточный обмен
- •Роль фосфорилазы при мобилизации гликогена
- •Обмен аминокислот, белков и нуклеотидов
- •Глюкозо-аланиновый цикл
- •Реакции глюкозо-аланинового цикла (выделен рамкой). Реакции, связанные с транспортными формами аммиака
- •Обмен липидов и липопротеидов
- •Гидролиз эфиров холестерина
- •Стеаторея
- •Этапы биосинтеза желчных кислот
- •Регуляция синтеза желчных кислот
- •Образование вторичных желчных кислот. Энтерогепатический цикл.
- •Метаболизм кетоновых тел при голодании
- •Биологические мембраны. Перекисное окисление липидов
- •1. Основные мембраны клетки и их функции.
- •2. Строение и состав мембран: структура и свойства липидов,белков, углеводов мембран. Общие свойства мембран и их функции.
- •3. Трансмембранный перенос малых молекул. Типы переноса веществ через мембрану. Трансмембранный перенос макромолекул и частиц. Механизмы мембранного транспорта
- •Проницаемость плазматической мембраны
- •Пассивный транспорт
- •Простая диффузия
- •Облегченная диффузия
- •Особенности облегченной диффузии
- •Активный транспорт
- •Ионные каналы
- •Эндоцитоз
- •Экзоцитоз
- •Функции биологических мембран
- •4. Механизмы трансмембранной передачи гормонального сигнала в клетку.
- •5. Активные формы кислорода (афк). Биологическое действие афк. Ферментативные и неферментативные системы, генерирующие афк.
- •6. Стадии свободно-радикального окисления липидов.
- •7. Повреждающее действие первичных и вторичных продуктов пероксидного окисления на мембраны и другие структуры клетки.
- •8. Ферментативные системы антирадикальной защиты. Катализируемые реакции.
- •9. Неферментативные системы антирадикальной защиты и их физиологическое значение.
- •10. Роль афк в механизме фагоцитоза. Кислородзависимые и кислороднезависимые механизмы фагоцитоза. Роль афк в антимикробной защите грудного молока.
- •11.Роль пероксидного окисления при гипоксии (ишемии). Факторы гипоксии, инициирующие пол. Понятие о «кислородном» и «кальциевом» парадоксах.
- •12. Простагландины и лейкотриены: схема синтеза и их биологические функции.
- •Гормоны. Гормональная регуляция метаболических процессов
- •Регуляция синтеза и секреции
- •Механизм действия
- •Мишени и эффекты
- •Патология Гипофункция
- •Биохимия питания и печени. Нервная, мышечная и соединительная ткани. Биохимия крови
- •Метаболизм скелетных мышц ( поперечно-полосатые мышцы)
- •Метаболизм скелетных мышц ( поперечно-полосатые мышцы)
- •Двойственная роль креатинфосфата
- •Пути генерации атф и восстановление атф в мышечных клетках миокарда
- •Механизм мышечного сокращения
- •Этапы цикла мышечного сокращения
- •Миозиновая регуляция сокращения
- •Сравнение актин-миозинового взаимодействия в 2-х видах мышц
- •Механизм расслабления поперечнополосатого мышечного волокна
- •Метаболические нарушения при инфаркте миокарда
- •Лабораторная диагностика инфаркта миокарда
- •Обмен железа: основные функции, пул железа в организме, всасывание в жкт, «ферритиновый блок».
- •Поступление экзогенного железа в ткани из кишечника
- •Нарушение метаболизма железа
- •4 Семестр
- •Диабет и мутации митохондрий.
Глюкозо-аланиновый цикл
В мышцах основным акцептором лишнего аминного азота является пируват. При катаболизме белков в мышцах происходят реакции трансаминирования аминокислот, образуется глутамат, который далее передает аминоазот на пируват и образуется аланин. Из мышц с кровью аланин переносится в печень, где в обратной реакции передает свою аминогруппу на глутамат. Образующийся пируват используется как субстрат в реакциях синтеза глюкозы (глюконеогенез), а глутаминовая кислота дезаминируется и аммиак используется в синтезе мочевины.

Реакции глюкозо-аланинового цикла (выделен рамкой). Реакции, связанные с транспортными формами аммиака
Целевыми органами для транспорта аммиака являются печень, почки и кишечник.
В печени:
аспарагин и глутамин дезаминируются соответственно аспарагиназой и глутаминазой, образующийся аммиак используется для синтеза мочевины ,
аланин вступает в реакции трансаминирования с α-кетоглутаратом,
глутаминовая кислота подвергается окислительному дезаминированию.
В кишечнике часть глутамина дезаминируется глутаминазой. После этого образованный аммиак выделяется в просвет кишечника (не более 5%) или через кровь воротной вены уходит в печень, а глутамат вступает в трансаминирование с пируватом, в результате чего аминоазот переходит на аланин и с ним также поступает в печень,
В почках идет образование аммонийных солей с использованием глутамата, глутамина и аспарагина.
Синтез мочевины: схема реакций, суммарное уравнение. Взаимосвязь с ЦТК. Клиническое значение определения концентрации мочевины в крови и моче, причины повышения и понижения концентрации мочевины.
Синтез мочевины. Орнитиновый цикл. Функции орнитинового цикла
В печени выполняет две функции: превращение азота аминокислот в мочевину, которая выводится из организма, помогая избежать накопление токсичного аммиака; синтез аргинина, из которого образуется мочевина
Основным механизмом обезвреживания аммиака в организме является биосинтез мочевины. Последняя выводится с мочой в качестве главного конечного продукта белкового (соответственно аминокислотного) обмена. На долю мочевины приходится до 80-85% от всего азота мочи. Впервые Г. Кребс и К. Гензелейт в 1932 г. вывели уравнение реакции синтеза мочевины, которые представлены в виде цикла, получив в литературе название орнитинивого цикла мочевинообразоавния Кребса. Следует указать, что в биохимии эта была первая циклическая система метаболизма, описание которой почти на 5 лет опередило открытие Г. Кребсом другого метаболического процесса-цикла трикарбоновых кислот. Благодаря исследования Г. Коена, С. Ратнер и сотр. были уточнены промежуточные этапы и ферментные системы, катализирующие образование мочевины.
Весь цикл мочевинообразования может быть представлен следующим образом. На 1-м этапе синтезируется макроэргическое соединение карбомоилфосфат – это метаболически активная форма аммиака, используемая в качестве исходного продукта для синтеза пиримидиновых нуклеотидов. Фермент – аммиакзависимая карбамоилфосфатсинтетаза:
пиримидин←карбамоилфосфат→аргинин→мочевина ↓ ↓ ↓ ДНК РНК белки
Реакция требует затрату 2 АТФ, происходит в митохондриях клеток печени. В качестве активного стимулирующего аллостерического эффектора действует N-ацетилглутамат.
На 2-м этапе цикла мочевинообразования происходит кондесанция карбамоилфосфата и орнитина с образованием цитруллина; реакцию катализирует орнитин-карабамоилфосфатрансфераза.
На 3-м этапе цитруллин превращается в аргинин в результате двух последовательно протекающих реакций. Первая из них– это энергозависимая конденсация цитуллина и аспарагиновой кислоты с образованием аргининосукцината (эту реакцию катализирует аргининосукцинатсинтетаза). Вторая из них – аргининсукцинат распадается на аргинин и фумарат при участии другого фермента – аргининсукцинатлиазы.
На 4-м этапе аргинин под действием аргиназы расщепляется на мочевину и орнитин, который вступает в новый оборот цикла, соединяясь с карбамоил-фосфатом, образуя цитруллин.
Необходимо подчеркнуть, что аргиназа содержится в печени тех животных, которые экскретируют с мочой мочевину как основной и конечный продукт азотистого обмена. В печени птиц, например, аргиназа отсутствует, поскольку птицы вместо мочевины выделяют мочевую кислоту.
Суммарная реакция синтеза мочевины без учета всех промежуточных продуктов может быть в следующем виде:
CO2+NH3+3АТФ+2H2O+аспартат→мочевина+2АДФ+АМФ+фумарат+
+2Н3РО4+Н4P2О7
Данная реакция сопровождается снижением свободной энергии (ΔG=-40кДж), поэтому процесс всегда протекает в направлении синтеза мочевины. Следует указать, что синтез мочевины энергетически дорого обходится организму. На синтез одной молекулы мочевины затрачивается четыре высокоэнергетических фосфатных группы: две молекулы АТФ расходуются на синтез карабамоилфосфата и одна – на образование аргининоянтарной кислоты, при этом АТФ расщепляется на АМФ и который при гидролизе также образует две молекулы Н3РО4.

Орнитиновый цикл синтеза мочевины в печени (цикл Гензелейта)
Связь орнитинового цикла с ЦТК.
Источникоми аспартата для орнитинового цикла является фумарат, который последовательно в реакциях ЦТК превращающается сначала в малат (фермент - фумараза), а затем в ОАА (фермент – малат-ДГ) с последующим трансаминированием в аспартат.
В процессе эволюции живые организмы выработали различные типы азотистого обмена. Это аммонителический тип, при котором главным конечным продуктом азотистого обмена является аммиак; он свойствен преимущественно рыбам. При уретелическом типе обмена основным конечным продуктом обмена белков является мочевина; такой тип характерен для человека и животных. Урикотетический тип характерен для птиц рептилий; главным конечным продуктом данного типа обмена является мочевая кислота.
В норме концентрация мочевины в крови равна 20-40 мг/100 мл. За сутки с мочой у здоровых людей выделяется 20-35 г мочевины.
Количество азота мочевины в крови в норме колеблется в пределах 9-14 мг/100
мл. Цифры содержания азота мочевина в 2,14 раза меньше числа, выражающего концентрацию мочевины.
Большой интерес для практики представляет экспресс-методы определения концентрации мочевины, в частности с помощью прибора «Уреатест».
Клиническое значение определения мочевины.
При патологии сдвиги в уровне мочевины крови зависят от соотношения процессов мочевинообразования и её выделения. При острой почечной недостаточности концентрация мочевины в крови нередко достигает 300-500 мг/100 мл. При этом резко снижается выделение мочевины с мочой. Нарастание содержания мочевины в крови до 100-200 мг/100 мл (в расчёте на азот мочевины) является признаком нарушения функции почек средней тяжести, до 200 мг/100 мл – тяжёлым и свыше 300 мг/100 мл – очень тяжёлым нарушением с неблагоприятным прогнозом.
Иногда определяют отношение азота мочевины крови к остаточному азоту крови, выраженное в процентах:
Синтез креатина, креатинфосфата, креатинина. Функции этих соединений в организме.
Синтез креатина
Креатин необходим для образования в мышцах макроэрга - креатинфосфата.Синтез креатина протекает в 2 стадии с участием 3 аминокислот: аргинина, глицина и метионина. В почках из глицина и аргинина образуется гуанидинацетат при действииглицингуанидинтрансферазы.(ГАТ)
NH2 NH2

C=NH NH2 C=HN

ГАТ
NH + H2N—CH2—COOH (CH2)3 NH
глицин
(CH2)3 H2N—CH—COOH CH2
орнитин
NH2CH—COOH СООН
Аргинин гуанидинацетат
Затем, гуанидинацетат транспортируется в печень, где происходит реакция его метилирования с образованием креатина.

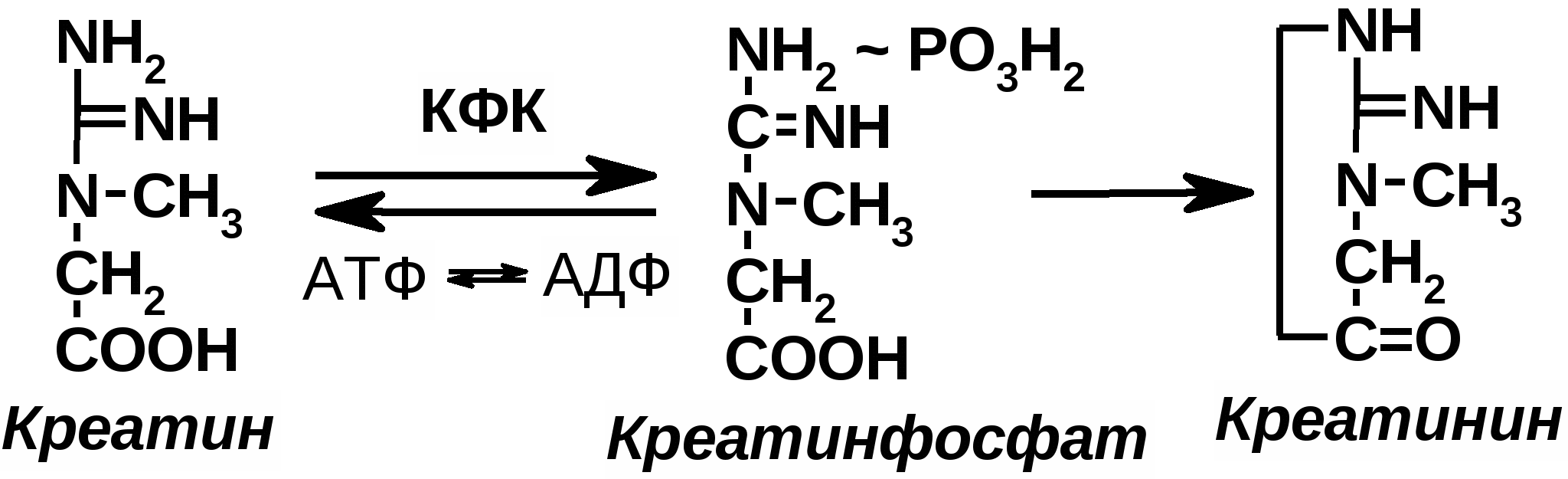
Креатин с кровотоком переносится в мышцы и клетки мозга, где из него образуется макроэрг-креатинфософат

Эта реакция легко обратима и катализируется ферментом креатинкиназой.(КФК)
Ферментативный гидролиз креатинфосфата – механизм ресинтеза АТФ в работающей мышце, поэтому креатинфосфат обеспечивает энергией процессы мышечного сокращения.
В результате неферментативного дефосфолирирования 2% креатинфосфата превращается в креатинин, выводимый с мочой.
В мозге, миокарде, мышцах
Фосфатидилхолины - 1) главные фосфолипиды биологических мембран клеток, входят в состав липопротеинов (транспортных форм липидов в кровотоке), 3) сурфактанта – комплекса, выстилающего внутреннюю поверхность альвеол, предотвращающего спадение альвеол на выдохе и их перерастяжение при вдохе.
Креатинфосфат содержится преимущественно в возбудимых тканях (мышечная и нервная ткани) и его биологической функцией является поддержание постоянной концентрации АТФ за счёт обратимой реакции перефосфорилирования: креатинфосфат + АДФ ⇔ креатин + АТФ
Креатин — важный компонент мышц, мозга. В форме креатин-фосфата он служит высокоэнергетическим фосфатом. Это единственный резервный макроэрг.
Креатинин участвует в энергетическом обмене мышечной и других тканей. Из организма креатинин выводится почками с мочой, поэтому креатинин (его количество в крови) — важный показатель деятельности почек.
Катаболизм пуриновых нуклеотидов. Содержание мочевой кислоты в сыворотке крови в норме и причины его повышения. Подагра.
Ко нечный
продукт катаболизма пурина у человека
- мочевая кислота. У других млекопитающих
имеется фермент уратоксидаза которая
превращает мочевую кислоту в более
растворимый аллантоин. У человека нет
такого фермента, и мочевая кислота,
которая образуется преимущественно в
печени, выделяется почками как конечный
продукт обмена пуриновых нуклеотидов.
Превращение мочевой кислоты в аллантоин
может протекать неферментативно. Эта
реакция рассматривается как один из
механизмов антиоксидантной защиты
клетки у организмов, утративших
способность синтезировать аскорбиновую
кислоту, а мочевая кислота как важный
антиоксидант, заменивший аскорбиновую
кислоту. У некоторых животных аллантоин
может распадаться далее до мочевины
или аммиака.
нечный
продукт катаболизма пурина у человека
- мочевая кислота. У других млекопитающих
имеется фермент уратоксидаза которая
превращает мочевую кислоту в более
растворимый аллантоин. У человека нет
такого фермента, и мочевая кислота,
которая образуется преимущественно в
печени, выделяется почками как конечный
продукт обмена пуриновых нуклеотидов.
Превращение мочевой кислоты в аллантоин
может протекать неферментативно. Эта
реакция рассматривается как один из
механизмов антиоксидантной защиты
клетки у организмов, утративших
способность синтезировать аскорбиновую
кислоту, а мочевая кислота как важный
антиоксидант, заменивший аскорбиновую
кислоту. У некоторых животных аллантоин
может распадаться далее до мочевины
или аммиака.
Норма содержания мочевой кислоты:
У детей - 120-330 (оптимально 120-280).
У взрослых-200-300 мкмоль/л уженщин ;250-360 мкмоль/л у мужчин.
Повышение МК в крови носит название гиперурикемия.
Заболевания суставов (подагра).
Мочекаменная болезнь и хроническая почечная недостаточность.
Гипертоническая болезнь
Ишемическая болезнь сердца.
Атеросклероз сосудов.
Цереброваскулярная болезнь.
Повышение МК часто связано с сахарным диабетом 2 типа.
Лейкоз, токсикоз, псориаз, гемолитическая анемия
Подагра. Причиной болезни является повышенное содержание мочевой кислоты в крови (первичная гиперурикемия). В свою очередь первичная гиперурикемия передается генами.
Подагра с воспалением в месте отложения кристаллов моноурата натрия у людей с гиперурикемией (повышение мочевой кислоты в крови), обусловленной внешнесредовыми и/или генетическими факторами
Известно, что пуриновые основания в организме человека расщепляются до мочевой кислоты, далее выводятся почками. При превышении концентрации мочевой кислоты в крови, происходит откладывание ее кристаллов в виде моноурата натрия в суставах, почках, мягких тканях. В результате возникает артрит, появляются образования на сгибательных поверхностях суставов, ушных раковинах (тофусы), развивается поражение почек в виде уратной нефропатии, а также в почках образуются камни.
Обмен метионина и его роль в обмене веществ.
Биологическое значение метионина
Таким образом, метионин, участвуя в процессах ДНК, синтезе полиаминов, образовании фосфолипидов биологических мембран, обеспечивает процессы пролиферации в частности регенерации клеток печени.
Участвуя в метилировании токсических продуктов и лекарственных препаратов, метионин обеспечивает детоксикационную функцию печени
Обеспечивая синтез фосфолипидов липопротеидов, метионин предотвращает накопление жиров в клетках печени.
То есть метионин является и гепатопротектором и гепатостимулятором. Поэтому при заболеваниях печени больным рекомендована диета с высоким содержанием метионина (творог)
Биологическое значение небелковых азотсодержащих веществ достаточно широко имеет клиническое значение, содержащие к ним относятся продукты обмена аминокислоты – креатинин, креатин, креатинфосфат, мочевина, мочевая кислота, аммиак серотонин, сукцинил SкоА.
Обмен метионина
Метионин - серосодержащая незаменимая аминокислота, поступающая в наш организм в составе продуктов животного происхождения. Особенно много этой аминокислоты содержится в твороге.


5 1
2
4 3 2
Так как метионин является α-аминокислотой, он включается в синтез белков и пептидов. Метильная группа радикала – мобильный одноуглеродный фрагмент, используемый для синтеза ряда соединений. Перенос метильной группы называется реакцией трансметилирования. Метионин участвует в синтезе полиаминов – активаторов клеточного деления. Наличие в радикале серы обуславливает то, что метионин является источником атома серы для синтеза цистеина. Метионил-тРНК участвует в инициации процесса трансляции.
Активация метионина
Активной формой метионина является - SAM – S-аденозинметионин, эта форма нестабильна и легко отщепляется (активный метионин), т. е. S-AM – это универсальный донор метильных групп для реакций трансметилирования. При отщеплении метильной группы S-AM превращается в S-аденозилгомоцистеин (S-АГ).
Но в систему трансметилирования входит не только метионин. Еще необходимы и два витамина - фолиевая кислота и витамин В12 (кобаламин).
Значение трансметилирования.
Метилирование ДНК- повышение клеточной активности пролиферации
Синтез креатина, карнитина, адреналина, фосфатидилхолина
Обезвреживание токсинов и лекарственных препаратов
метионин S-AM
CH3 CH3
Метилирование трасметилирование
гомоцистеин S-AГ

 фф.АДФ
Метилкобаламин Фолиевая
кислота
фф.АДФ
Метилкобаламин Фолиевая
кислота
CH3фолат-редуктаза


 АТФ Вит В12 H4-фолат
АТФ Вит В12 H4-фолат
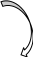
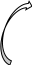
СН3
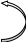

 метил-H4-фолат
метилен-H4-фолат
метил-H4-фолат
метилен-H4-фолат
 Гомоцистин Вит
В12
Гомоцистин Вит
В12
кобаломин
Функции метильного радикала:
CH4 обезвреживание токсинов
синтез карнитина
синтез креатина
метилирование синтез адреналина синтез фосфотидилхолина
