
- •Аминокислоталар, пептидлар, оқсиллар
- •Оқсилларнинг аминокислота таркибини аниқлаш
- •Оқсилларнинг тузилиши
- •Оқсил ва пептидларнинг кимёвий синтези
- •Оқсиллар ва пептидларнинг кимёвий модификацияси
- •40000 Марта катталаштирилган
- •Ферментлар
- •Ферментларнинг каталитик фаоллиги сабаблари
- •Ҳимоя оқсиллари
- •2. Антитаналарнинг изотиплари. Улар константа қисмининг типи орқали аниқланади. Баъзи изотиплар бириктирувчи занжир ёрдамида димерларни (IgA), ёки пентамерларни (IgM) ҳосил қилади.
- •Иммун жавоб медиаторлари - цитокинлар
- •Яллиғланиш медиаторларининг классификацияси
- •Тўқима лизокиназалари, стрептокиназа
- •Плазминоген (фибринолизиноген, профибринолизин)
- •Оқсил ва пептид гормонлар
- •Оқсил ва пептид гормонлар биосинтези
- •Нейропептидлар
- •Қилувчи гипоталамус гормонлари
- •Гастроинтестинал пептид-гормонлар ва уларнинг биологик функциялари
- •Пептид токсинлар
- •Предмет кўрсаткичи
- •Номлар кўрсаткичи
- •Фойдаланилган адабиётлар
- •Интернет ресурслари
- •Мундарижа
Оқсил ва пептидларнинг кимёвий синтези
Оқсил ва пептидларнинг кимёвий синтези (пептид боғ ҳосил қилиш усуллари),
ферментатив синтез, циклопептидлар, гетеропептидлар синтези, депсипептидлар.
Кириш. Пептидлар биринчи марта оқсилларнинг ферментатив гидролизатларидан ажратиб олинган. «Пептид» термини Эмиль Фишер тарафидан таклиф этилган. Биринчи синтетик пептидни 1881 йилда Т.Курциус синтез қилган. 1905 йилда Фишер пептид синтезининг умумий усулини ишлаб чиқди ва бир қатор олигопептидларни синтез қилди.
-
Пептидларнинг классификацияси. Барча пептидлар гомомер ва гетеромер пептидларга ажратилади. Гомомер пептидлар гидролиз натижасида фақат аминокислоталарни беради. Гетеромер пептидлар аминокислоталар билан бир қаторда бошқа синф моддаларни ҳам ҳосил қилади. Аминокислота бўлмаган компонентининг тузилишига қараб гетеромер пептидлар глико-, липо-, нуклео-, фосфопептидлар ва бошқаларга бўлинади. Гомомер ва гетеромер пептидлар чизиқли ва циклик тузилишга эга бўлиши мумкин. Аминокислота қолдиқлари ўзаро фақат пептид боғлар билан боғланган бўлиши мумкин (гомодет пептидлар), ёки пептид боғларидан ташқари мураккаб эфир, дисульфид ва бошқа боғлар билан ҳам боғланган бўлиши мумкиин (гетеродет пептидлар).
Гидроксиаминокислоталар занжирга кирган гетеродет пептидлар – пептолидлар деб аталади. Фақат бир хил аминокислота қолдиғидан тузилган пептидларга гомо-полиаминокислоталар дейилади, бир ёки бир нечта аминокислота қолдиғидан иборат участкалари қайтариладиган пептидларга регуляр пептидлар дейилади. Гетеромер гетеродет пептидларнинг алоҳида группасини депсипептидлар ташкил этади.
-
Оқсил ва пептидларнинг кимёвий синтези. Пептид синтези – кимёвий усуллар ёрдамида аминокислоталарни бир-бирига бириктириб, пептид занжирини ҳосил қилишдир. Одатда 40-45 аминокислоталардан иборат пептидлар, кичик оқсиллар синтез қилинади. Фойдаланилаётган услубий йўл ва синтез қилинаётган охирги маҳсулот характерига қараб қуйидаги тур пептид синтезлари ажратиб кўрсатилади:
-
Эритмада пептидларнинг классик синтези (босқичма-босқич- С-охирги аминокислотадан бошлаб N-охирги аминокислотага қадар аминокислоталарнинг бирикиши ва блокли – синтезланган фрагментлар асосида пептид занжирини ҳосил қилиш):
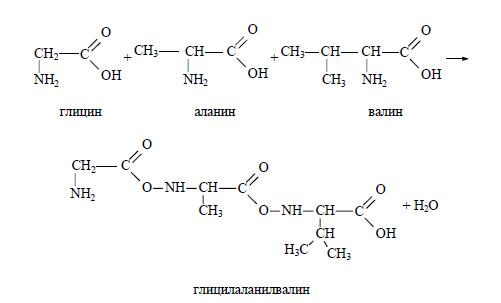
-
Пептидларни полимер ташувчида синтезлаш (ўсаётган полипептид занжири эрувчан ёки эримайдиган полимерга ковалент боғланган бўлади, қаттиқ фазада ёки суюқ фазада олиб борилади):
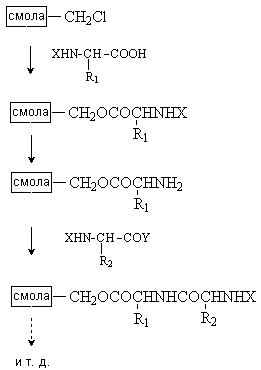
-
Гомо- ва гетерополиаминокислоталар бир ёки иккита аминокислота қолдиғи асосида қайтарилувчан синтезланади:
HOOC —CH2 —NH —H + HOOC —CH2 —NH2 →
HOOC —CH2 —NH —CO —CH2 —NH2 + H2O
-
Пептидларнинг ферментатив синтези. Баъзи пептид боғларини гидролизловчи ферментлар, маълум шароитларда тескари реакцияни катализ қилишга мойил бўлиб қолади, яъни аминокислоталар орасида пептид боғини ҳосил қилишга. Каталитик реакция мувозанатини ўзгартиришнинг усулларидан бири уни органик эритувчида озроқ сув иштирокида олиб боришдир.
-
Пептидларнинг полусинтези, семисинтези (табиий пептид ёки оқсил молекуласидан кичикроқ фрагмент ажратилади, ва кейин янги аминокислоталар кетма-кетлиги киритилади).
-
Циклик пептидлар синтези.
-
Гетеродет пептидлар синтези (нафақат амид боғлар, балки мураккаб эфир, дисульфид ва бошқа боғлар иштирокида).
Пептидларнинг синтези қуйидаги кетма-кет келадиган босқичлардан иборат:
-
Аминокомпонента карбоксигруппасининг ҳимояси
-
Карбоксикомпонента амин группасининг ҳимояси
-
Ён занжир карбокси- ва амин группаларининг ҳимояси
-
Карбоксикомпонента карбоксигруппасининг активацияси
-
Пептид боғ ҳосил қилиб синтез олиб бориш
-
Ҳимоя группаларидан озод бўлиш
-
Пептидни ажратиб олиш
-
Полиаминокислоталар синтези. Молекуласи таркибида фақат битта аминокислота қолдиғини сақлаган пептидларга гомополиаминокислоталар дейилади, бир хил қайтарилувчан (битта ёки бир нечта аминокислота қолдиқларидан) участкаларни сақлаган пептидлар эса регуляр пептидлар деб аталади. Полиаминокислоталарнинг N-карбоксиаминокислоталар ангидридларидан синтез қилиш қуйидаги схемага кўра амалга ошади:
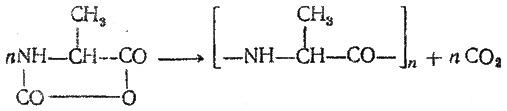
4. Пептид боғ ҳосил қилиш усуллари. Пептид боғ ҳосил қилиш усуллари сув элементларининг ажралиши билан боғлиқ. Бу жараённинг юқори тезлигини ва тўлиқ ўтишини таъминлаш учун карбоксил группани активациялаш зарур, яъни, карбонил группасидаги углерод атомининг электрофиллигини ошириш керак Сδ+.
Хлорангидрид усули. Ациламинокислоталарнинг тегишли хлорангидридларга айланиши карбоксил группани активлаштиришнинг энг эски усулларидан биридир (Э.Фишер). Масалан, карбобензоксиглицин хлорангидриди ишқорий муҳитда глицин билан осон реакцияга киришади ва карбобензоксиглицил-глицинни ҳосил қилади:
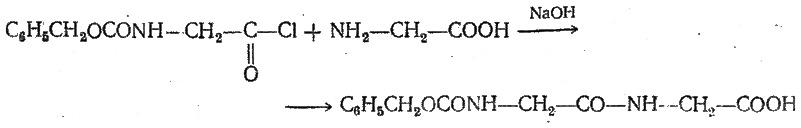
Азид усули (1902). Т.Курциуснинг бу усули пептидлар синтезида кенг қўлланилади. Гидразидлар ҳимояланган аминокислоталар ёки пептидлар эфирларининг тўғридан-тўғри гидразинолизи натижасида олинади, ёки ҳимояланган гидразидлардан (–СО–NH–NH–Z–, –СО–NH–NH–кайт.) олинади. Азидларни олиш учун кислотали муҳитда 5°С да натрий нитрити таъсир эттириб, ёки изоамилнитрит ёки учламчи бутилнитрит билан 20°Сда органик эритувчида таъсир эттириб олиб борилади Хонцль ва Рудингер модификацияси, 1961). Азидларни бевосита НООС-ҳосилалардан конденсацияловчи агент сифатида қўлланиладиган дифенилфосфорилазид N3PO(OC6H5)2 таъсир эттириб олиш мумкин:
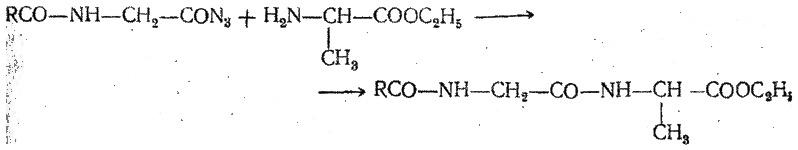
Аралаш ангидридлар усули. Хлоркўмир кислотаси эфирларининг N-алмашинган аминокислоталарга таъсири натижасида аминокислота ва кўмир кислотаси эфирининг аралаш ангидридлари ҳосил бўлади:
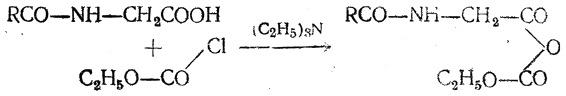
Аралаш
ангидридлар беқарорлиги туфайли ажратиб
олинмайди, аминокислота билан реакцияга
бевосита ҳосил бўлиши биланоқ қўшилади.
Улар жуда реакцион актив ва
аминокислоталарнинг эфирлари билан
ўзаро таъсирлашганда N-алмашинган
пептидларнинг эфирларини ҳосил қилади: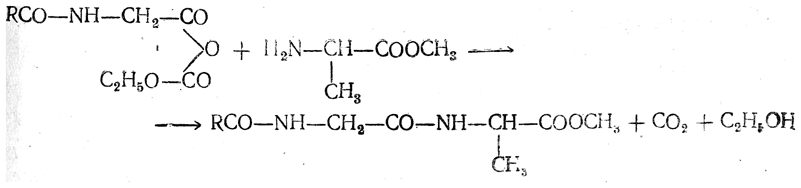
Аралаш ангидридлар олиш учун хлоркўмир кислотасининг эфирларидан ташқари бошқа органик кислоталарнинг хлорангидридларидан ҳам фойдаланиш мумкин.
Активлаштирилган эфирлар усули. Аминокислоталарнинг эфирлари бир-бири билан пептид боғ ҳосил қилиб ва спирт молекуласини ажратиб таъсирлашадилар. Бунда реакция одатда дипептид ҳосил бўлиши билан тўхтаб қолмайди, балки узун полипептид занжирларининг ҳосил бўлишига олиб келади. Охирги вақтларда эфир қолдиғига электроноакцептор группировкаларни киритиш аминокислотанинг реакцион қобилиятини ошириши аниқланган (масалан, цианметил, п-нитрфенил, 2,4-динитрофенил эфирлари).
Ациламинокислотага асос иштирокида хлорацетонитрил билан таъсир этиб, ациламинокислотанинг цианметил эфири олинади, у алмашинмаган аминокислота эфири билан осон таъсирлашади.
:
Активлаштирилган эфирлар, айниқса п-нитрофенил эфирлар пептид синтезида кенг қўлланилади.
Карбодиимид усули. 1955 йилда пенициллинни синтез қилишда Дж. Шиэн ва Г. Хесс тарафидан дициклогексилкарбодиимид таклиф этилган. Реакциянинг биринчи босқичида карбоксил компонентасини активлаштириш натижасида реакцион қобилияти юқори бўлган О-ацилизомочевинанинг ҳосиласи олинади. О-ацилизомочевинанинг ҳосиласи бевосита, ёки тегишли симметрик ангидрид орқали пептидга айланади. Бу ерда асосий қўшимча жараён О → N-ацил силжиши бўлиб, унинг натижасида реакцияга қобилияти бўлмаган N-ацилизомочевиналар ҳосил бўлади.
Бу
усул билан пептид синтези учун одатда
дициклогексилмочевинани п-толуолсульфохлорид
билан дегидратацияга учратиш натижасида
олинадиган дициклогексилкарбодиимид
ишлатилади: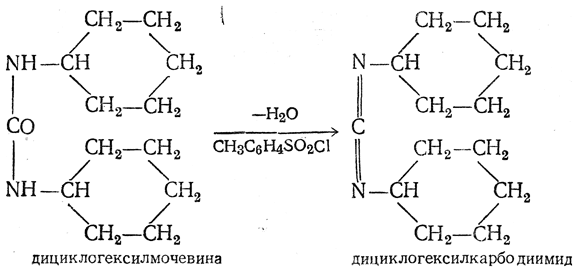
Дициклогексилкарбодиимид N-алмашинган аминокислота билан (ёки пептид билан) таъсирлашганда аввал О-ацилланган дициклогексилизомочевина ҳосил бўлади:
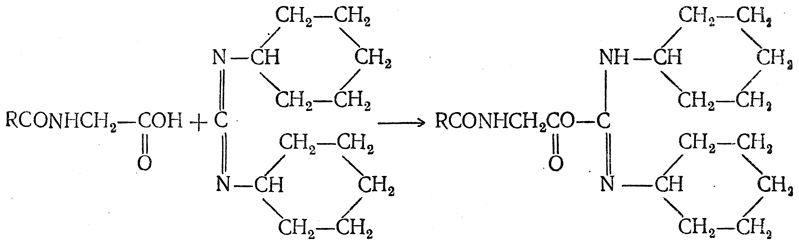
Дициклогексилизомочевина
аминокислота (пептид) эфири билан осон
таъсирлашади:
Дициклогексилкарбодиимид пировардида қийин эрувчан дициклогексилмочевинага айланади, уни пептиддан ажратиб олиш қийин эмас. Карбодиимид усули турли узунликдаги пептидларни синтез қилишда муваффақият билан қўлланилмоқда. Бу усулнинг афзал тарафларидан бири реакцияни сувли ва спиртли эритмаларда олиб бориш мумкинлигидир.
Карбоксиангидрид
усули. Этоксиацетиленни қўллаш. 1966
йилда Р.Хиршман сувли муҳитда пептидларни
йўналтирилган синтези учун
N-карбоксиангидридлардан
(NCA, Лейкс ангидридлари, оксазолидиндионлар)
фойдаланишни таклиф этди. N-алмашинган
аминокислоталар юмшоқ шароитларда
этоксиацетилен билан таъсирлашадилар: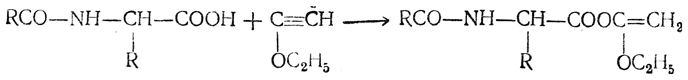
Ҳосил
бўлаётган активлашган эфир, амин
компонентаси билан таъсирлашиб
(аминокислота ёки пептиднинг эфири)
тегишли пептидни ҳосил қилади:
Бу реакцияда ягона қўшимча маҳсулот сифатида сиркаэтилэфири ҳосил бўлади, шунинг учун асосий маҳсулотни тозалаш ҳам осон кечади.
Бу усулни қўллаб Хиршман рибонуклеаза молекуласининг S-оқсили ўзун пептид фрагментларини синтез қилган. Пептид синтезида асосий қўшимча реакция – рацемизация бўлиб, бу нарса ҳимоя группаларини ва конденсация усулларини танлашда қаттиқ чекловлар қўяди.
Юқорида келтирилган пептид синтезининг кимёвий усуллари асосида карбоксил группасини активлаштириш ётади. Аминогруппани активлаштиришга асоосланган усуллар ҳам мавжуд, бироқ, улар бу қадар кенг тарқалиб кетмаган.
5. Полимер ташувчида пептидлар синтези. Классик вариантдаги пептид синтези жуда кўп вақт ва меҳнат талаб қилади. Ўз вақтида гормон табиатига эга бўлган 8 та аминокислота қолдиғидан иборат бўлган пептид – окситоцин синтези (1953, Винсент дю Виньо, 1955 йил Нобель мукофоти) жуда катта муваффақият тарзида кўрилган эди:
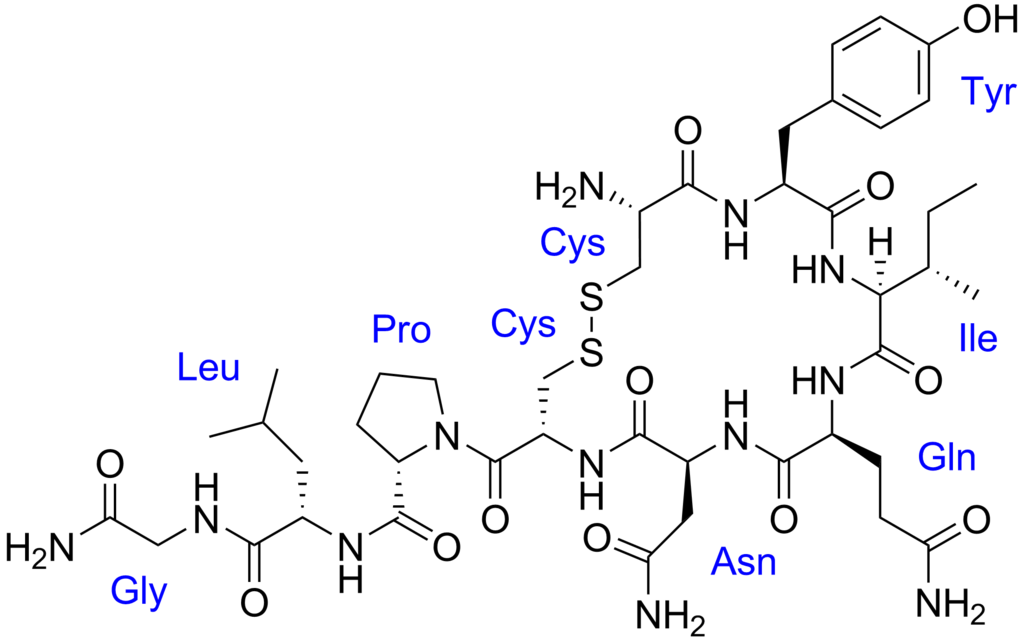
Окситоцин
Самарали методологияни яратиш мақсадида 1963 йилда Р.Меррифилд пептидларни қаттиқ фазада синтез қилиш усулини таклиф этди. Ўсаётган полипептид занжири эримайдиган полимер ташувчига ўтказилиши бу усулнинг моҳиятини ташкил этади.
Биринчи босқичда аминогруппа бўйича ҳимояланган С-охирги аминокислота қаттиқ фазага (–CH2Cl группаси киритилган полистирол) жойлаштирилади. Ҳимоя группаси олиб ташлангандан сўнг, қаттиқ фазага жойлаштирилган аминокислотанинг аминогруппасини, активлашган СООН группасини ва ҳимояланган аминогруппани тутган бошқа аминокислота билан ацилланади. Ҳимоя олиб ташлангач, ациллашнинг кейинги босқичига ўтилади ва иш шу тариқа давом эттирилади. Реакция маҳсулотини қаттиқ фаза – полимер ташувчининг ўзида қўшимча маҳсулотлардан тозалаш учун ювилади, ва синтез тугатилгач полипептид полимер ташувчидан, унга HBrO3 кислотаси таъсир эттириб, ажратиб олинади. Қаттиқ фазада пептид синтези автоматлаштирилган ва автоматик синтезаторлар ёрдамида ўтказилади. Бунда ҳимоя группаларининг танланиши рацемизация содир бўлишига йўл қўймаслиги керак. Қаттиқ фазада пептид синтези учун юқори даражада тозаланган реагент ва эритувчилар талаб этилади. Брадикинин гормонининг қаттиқ фазада синтезини биринчи бўлиб Р. Меррифилд амалга оширган, 70% унум билан. Полимер ташувчи сифатида кўпинча органик эритувчиларда яхши бўкувчи, кимёвий ва механиқ мустаҳкамликка эга бўлган хлорметилланган стирол ва дивинилбензолнинг сополимери ишлатилади.
Лаборатория шароитида пептидлар турли усуллар ёрдамида олиниши мумкин. Бу усулларнинг умумий тарафи – реакцияга киришаётган аминокислоталардан бирининг амин группасини, иккинчисининг эса карбоксил группасини ҳимоя қилиниши шартидир. Шунда аминокислоталар ўз таркибида эркин қолган (ёки кимёвий реагент билан боғланиб активлаштирилган) СООН группаси ёки амин группаси бўйича конденсация реакциясига киришади.
Бу борада Р.Меррифилд таклиф этган пептидларнинг қаттиқ фазадаги синтези тез маълум бўлиб кетди. Бу усулга кўра дастлабки аминокислотанинг СООН группасини полимерга боғлаб ҳимоя қилинади, боғланаётган иккинчи аминокислотанинг NH2-группасини эса учламчи изобутилоксикарбонил (БОК) радикали билан ҳимоя қилинади. Бу усулни автоматлаштириш мумкин, унинг асосида автоматик синтезатор яратилган, ва ундан фойдаланиб пептидларнигина эмас оқсилларни ҳам синтез қилиш мумкин.
Меррифилд брадикинин пептидини синтез қилган. Брадикинин 9 та аминокислота қолдиғидан иборат бўлган пептид. У трипсин протеолитик ферментининг қон плазмасининг глобулин фракциясига таъсир этганда ҳосил бўлади, ва жуда кам миқдорларда ҳам қон босимининг пасайишига олиб келади (гипотензив эффект). Брадикининнинг таркиби: Apг-Про-Про-Гли-Фен-Сер-Про-Фен-Apг.
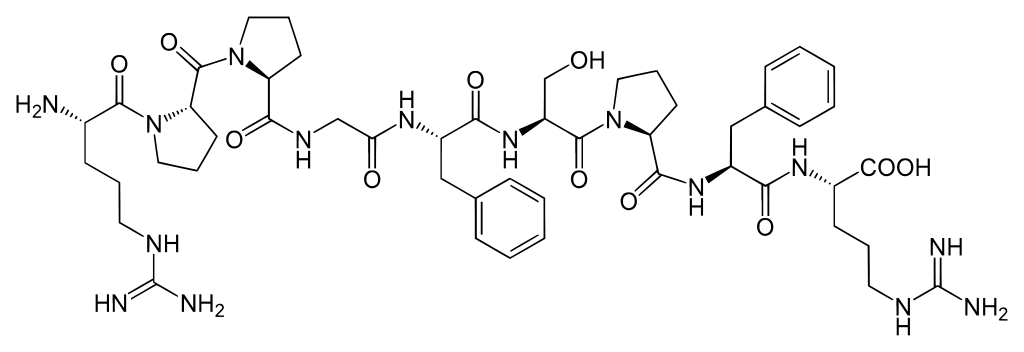
Брадикинин
Қаттиқ фазада пептидлар синтези техникаси вақт ва меҳнатни иқтисод қилиш имкониятини берар эди. Масалан, Хиршман ўзининг 22 та ҳамкасблари билан бирга суюқ фазадаги классик усул ёрдамида жуда катта меҳнатлар ҳисобига 124 та аминокислота қолдиғидан иборат рибонуклеаза ферментининг синтезини амалга оширган. Бир вақтнинг ўзида шу оқсил автоматлаштирилган қаттиқ фаза усулида синтез қилинган. 369 та кимёвий реакция ва 11931 кимёвий операцияни ўз ичига олган бу иккинчи йўлни 2 та кимёгар (Гатте ва Меррифилд) бир неча ой ичида амалга ошира олганлар (ўсаётган полипептид занжирига бир кунда 6 тагача аминокислота қолдиғи бирикиб борган). Кейинчалик бу усулни такомиллаштириш натижасида тўлиқ автоматик синтезаторни қуриш имконияти пайдо бўлган.
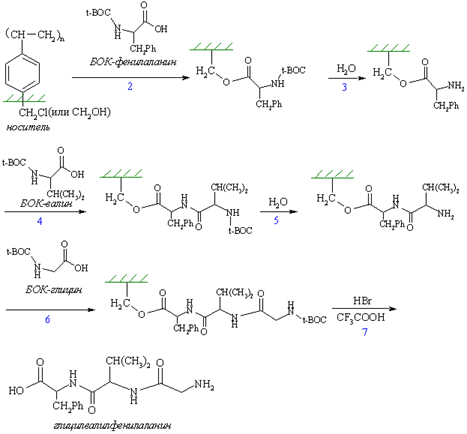
Қаттиқ фазада пептидлар синтезининг схемаси
Меррифилд усули органик синтезда янги йўналиш – комбинатор кимёнинг асоси бўлиб хизмат қилди. Баъзан комбинатор экспериментлар эритмаларда олиб борилса ҳам, улар қаттиқ фаза техникаси ёрдамида ўтказилади, яъни реакциялар полимер смолаларининг сферик гранулалари ҳолида бўлган қаттиқ фазани (подложка) қўллаб ўтказилади. Бу усулнинг қатор фойдали тарафлари бор:
-
Турли дастлабки моддалар алоҳида гранулалар билан боғланиб қолади. Сўнгра бу гранулалар аралаштирилади, ва шундай қилиб барча дастлабки моддалар реагент билан бир экспериментда таъсирлаша олади. Натижада реакция маҳсулотлари алоҳида гранулаларда ҳосил бўлади. Кўпчилик ҳолларда дастлабки моддаларни суюқ фазада аралаштириш полимеризация, смола ҳосил бўлиб қолиши каби керак бўлмаган ҳолатларни берар эди. Қаттиқ фазадаги экспериментлар мана шундай эффектларга йўл қўймайди.
-
Дастлабки моддалар ва ҳосил бўлган маҳсулотлар қаттиқ фаза билан боғланган экан, уларнинг подложка билан боғланмаган ортиқча миқдорини осонликча ювиб олиш мумкин.
-
Реагентларни катта ортиқча миқдорда ишлатиб реакцияни охиригача (99% унум билан) етказиш мумкин, чунки бу ортиқча миқдорларни осонликча ажратиб олиш мумкин.
-
Дастлабки моддалар кичик ҳажмда (1 гр подложкага 0,8ммоль дан кам) олинганда керак бўлмаган қўшимча реакциялардан қутулиш мумкин.
-
Интермедиатлар гранулалар билан боғланган бўлгани учун уларни тозалаш талаб этилмайди.
-
Полимернинг индивидуал гранулалари эксперимент охирида ажратилиши мумкин, ва натижада индивидуал маҳсулотлар ажратиб олинади.
-
Полимер подложка, парчалаш усуллари ва тегишли якорь группалари – линкерлар танланганда, регенерация қилиниши мумкин.
-
Қаттиқ фазадаги синтезни автоматлаштириш мумкин. Қаттиқ фазадаги синтез ўтказишнинг, реакцион шароитларда инерт бўла оладиган ва эримайдиган полимер подложканинг мавжудлигидан ташқари, зарурий шартлари қуйидагилардир:
-
Киритилаётган модданинг подложка билан боғланишини таъминлаб берувчи кимёвий функция – якорь ёки линкернинг бўлиши. У смола (полимер) билан ковалент боғланган бўлиши керак. Субстрат якорь билан ўзаро таъсирлаша олиши учун у ҳам реакцион қобилиятли функционал группа бўлиши керак.
-
Субстрат ва линкер орасида ҳосил бўлаётган боғ реакция шароитларида барқарор бўлиши шарт.
-
Маҳсулот ёки интермедиатнинг линкер билан ҳосил қилган боғланишини узиш усуллари бўлиши керак.
6. Пептидларнинг ярим синтези (полусинтез). Полусинтез (семисинтез, қисман синтез) – табиий пептид, оқсилларнинг ёки уларнинг фрагментларини тўлиқ синтезланган ёки модификация қилинган оқсил ёки пептидлар, ёки уларнинг фрагментлари билан комбинациялашга асосланган усул. Ярим синтезни табиий бирикмаларни модификация қилишга асосланган методик усул (приём) деб қараш мумкин. Оқсилларнинг структуравий кимёсида маълум бўлган пептид боғларини ферментатив ва кимёвий парчалаш усуллари ва ҳосил бўлган фрагментларни хроматография техникаси орқали ажратиб олиш усули гомоген пептид блокларини олиш имконини беради. Турли усуллар ёрдамида керакли фрагментни максадга йўналтирилган ҳолда ўзгартириш (қисқартириш, узайтириш, янги қолдиқларни киритиш ва ҳ-зо), ва ҳосил бўлган блоклардан янгиларини йигиш, ўзгартирилган кетма-кетликлар ҳосил қилиш мумкин. Ярим синтезда ҳимоя группалари шундай танланадики, улар киритилганда ҳосил бўлган ҳосилалар сувда ва сувли-органик эритувчиларда яхши эрисин. Тайёрланган пептид блокларидан керакли кетма-кетлик йиғилаётганда кўпинча DCC/HOBt, DCC/HOSu, азид усули ва активлаштирилган эфирлар усули қўлланилади (DCC – дициклогексилкарбодиимид). Бунда рацемизация муаммосига алоҳида эътибор бериш зарур.
7. Циклопептидлар синтези. Полипептидлар циклик тузилишга ҳам эга бўлиши мумкин. Айниқса 2 та аминокислота қолдиғидан тузилган циклопептидлар осон ҳосил бўлади. Пиперазиннинг ҳосилалари деб қараш мумкин бўлган бу бирикмалар 2,5-дикетопиперазинлар номини олган. Дикетопиперазинлар синтезининг қуйидаги усуллари мавжуд:
Аминокислоталарни
қиздириш.
Кўпчилик аминокислоталар, масалан,
лейцин, уларнинг глицериндаги ёки
этиленгликольдаги эритмаларини
қиздирганда дикетопиперазинларни
ҳосил қилади: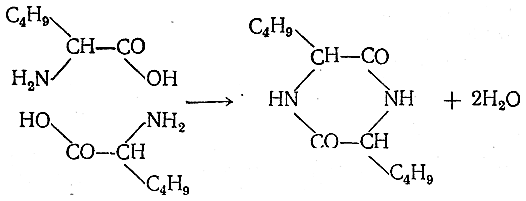
Дикетопиперазиннинг ҳосил бўлиши
Аминокислота
эфирларидан олиш.
Аминокислота эфирларини қиздирилганда
дикетопиперазинлар ундан ҳам осон
ҳосил бўлади: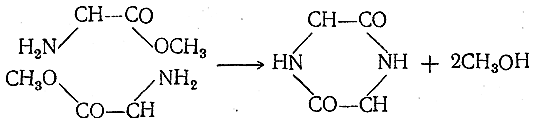
Дипептидларнинг
эфирларидан олиш.
Дипептидларнинг эфирлари ҳам қиздирилганда
осонликча дикетопиперазинлар ҳалқасини
ҳосил қилади. Бу усул билан 2 хил
аминокислота қолдиқларидан иборат
бўлган дикетопиперазинларни олиш
мумкин: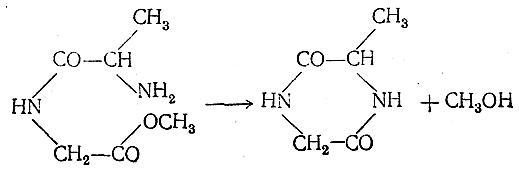
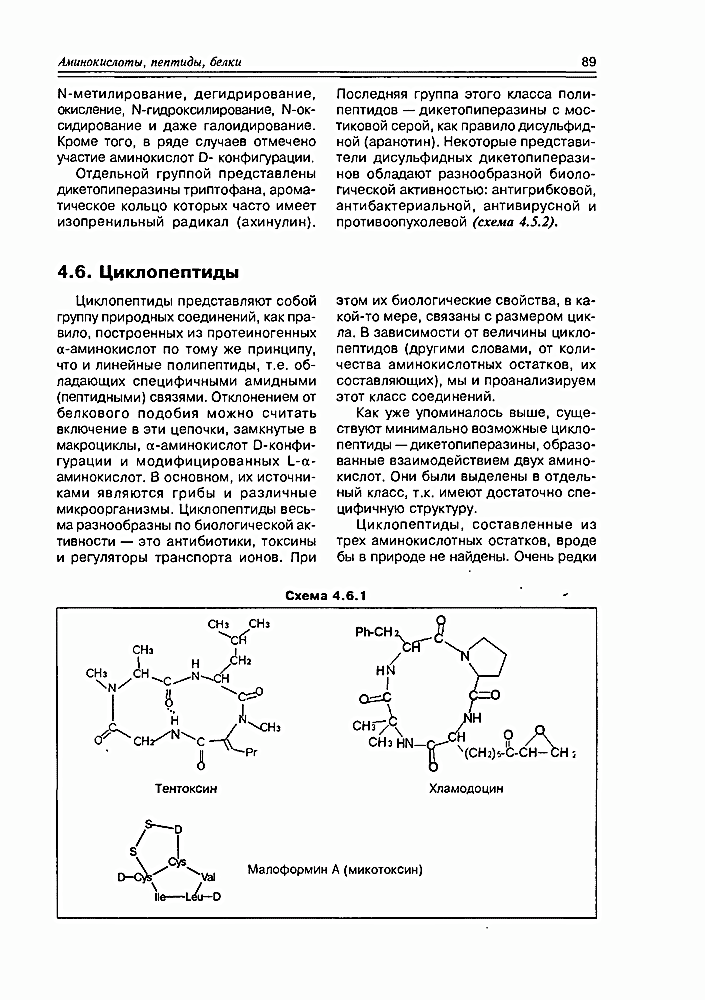
Циклопептидлар табиий бирикмалр группасини ташкил этган моддалардир. Одатда улар протеиноген α-аминокислоталар қолдиғидан чизиқли полипептидларнинг тузилиш принципи бўйича тузилган бўлади, яъни ўзига хос амид (пептид) боғларга эга. Оқсилларга ўхшашликдан истисно сифатида макроциклларга бирлашган ушбу занжирларга D-конфигурациядаги α-аминокислоталарнинг ва модификацияланган L-α-аминокислоталарнинг кириб қолишини келтириш мумкин. Уларнинг манбаъи, асосан, замбуруғлар ва турли микроорганизмлардир.
Биологик активлиги бўйича циклопептидлар хилма-хилликни намоён қилади, улар - антибиотиклар, токсинлар ва ионларни транспорт қилиш регулятор пептидларидир. Уларнинг биологик активлиги циклнинг ўлчамига боғлиқ. Циклопептидлар кичик молекулалардир, асосан 6 – 12 та аминокислота қолдиғидан тузилган бўлади. Циклик структурага эга бўлгани учун, фазовий ҳаракатланиши ҳам чекланган.
Циклопептидларга мисол тариқасида замбуруғлардан олинган микотоксин – тентоксинни, хламодоцинни келтириш мумкин – булар циклик тетрапептидлардир.
Циклик пентапептидларга малоформинлар оиласи, виомицин, туберактиномицин ва капреомицин киради. Ушбу қаторнинг баъзи вакиллари сил касаллигини даволашда ишлатилади.
Циклик гексапептидлар қаторида сидерохромлар (сидерофорлар) синфига кирувчи темир сақлаган метаболитлар кўпроқ ўрганилган. Феррихром пептиди мисолида микроорганизмлар ўсишининг фактори эканлиги кўрсатилган. Ушбу циклопептиднинг молекуласида 5-аминогруппа бўйича ацилланган ва гидроксилланган орнитиннинг 3 та қолдиғи бор. Айнан мана шу функционализацияланган қолдиқлар уч валентли темир иони билан комплекс боғ ҳосил қилади.
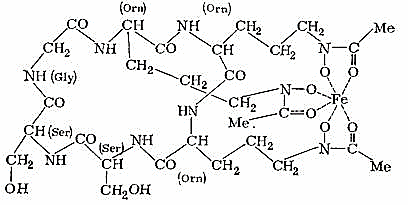
Fe (III) сақлаган феррихром циклопептидининг тузилиши
Орнитин
–
диаминвалериан кислотаси,
NH2CH2CH2CH2CH(NH2)СООН
– одамнинг овқатланишида алмаштириб
бўладиган аминокислота, оқсиллар
таркибига кирмайди, мочевина биосинтезида
муҳим роль ўйнайди. Орнитин аргинин
синтезида муҳим оралиқ маҳсулот
ҳисобланади: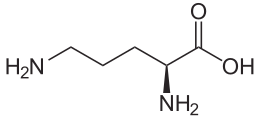
Орнитин
8. Сидерохромлар (сидерофорлар) – микроорганизмлар ишлаб чиқарадиган махсус пептидлар бўлиб, атроф-муҳитдан темир ионларини боғлаб олиш хусусиятига эга. Уларни микроорганизмларнинг темир транспортловчи агентлари деб қараш мумкин.
9. Депсипептидлар. Депсипептидлар молекуласи таркибида амид боғларидан ташқари, бир ёки бир нечта мураккаб эфир боғларини ҳам сақлайди. Кўпчилик табиий депсипептидлар тузилишининг ўзига хослиги – уларнинг молекуласида гетерокомпонентларнинг – α-аминокислоталарнинг қолдиқлари бўлмаган фрагментларнинг сақланишидир.
Депсипептидларнинг кимёвий ва физик хоссалари бошқа пептидларнинг хоссаларига ўхшаш. Улар эфир, хлороформ, диоксанда яхши эрийди, сувда ёмон эрийди. Табиий депсипептидларни асосан бактериялар ишлаб чиқаради. Уларнинг классификацияси продуцентнинг номига боғлиқ (кимёвий табиатига эмас). Таркибида гидроксиаминокислота, меркаптоаминокислота ёки гетероциклик карбон кислота қолдиқларини тутган циклик депсипептидлар пептидлактонлар деб аталади. Масалан, цистеиннинг S-пептидлари, треонин ва сериннинг О-пептидлари, актиномицин антибиотиклари, этамицин, А ва В микамицинлар ва бошқаларни келтириш мумкин.
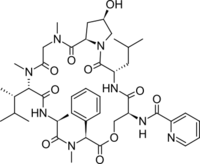
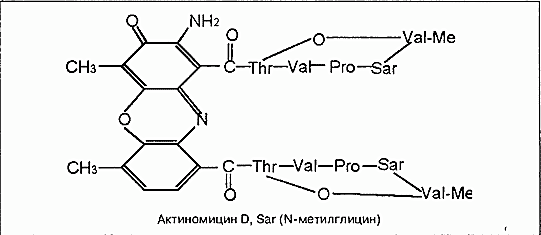
Актиномицин Этамицин
Актиномицинлар группаси норегуляр депсипептидлар туркумига киради, уларнинг молекуласи феноксазин фрагменти билан боғланган 2 та циклопептид циклидан иборат. Оксикислота сифатида треонин молекулси ўзининг спирт группаси ёрдамида N-метилвалиннинг карбоксил группаси билан боғланган.
Актиномицинлар ДНК га боғлиқ РНК синтезининг ингибиторларидир, уларнинг бу хоссасидан баъзи ўсмаларни даволашда клиникада фойдаланилади. Депсипептидлар кенг спектрдаги биологик таъсирни намоён қилади – улар антибиотик, ўсмаларга қарши, инсектицид ва бошқа активликларни намоён қилади.
Таркибига гидроксикислоталар қолдиқлари кирган депсипептидлар пептолидлар деб аталади. Уларнинг қаторига валиномицин, А ва В энниатинлар, В ва С анголидлар (III) киритилади, 23-расм.
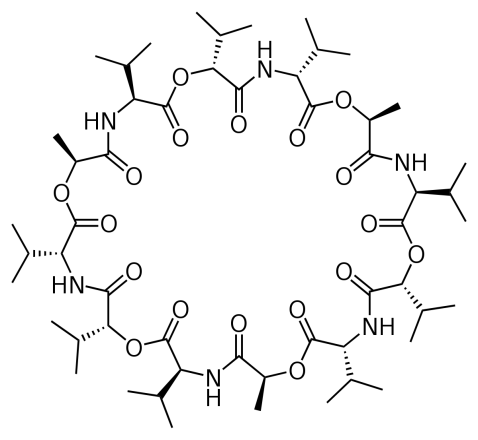

23-расм. Валиномицин: D – D-валин, L – L-валин, рангсиз доира - L-сут кислотаси
Циклик депсипептидларнинг антибиотик активлиги уларнинг эритмаларда ишқорий ва ишқорий-ер металларининг катионларини боғлай олиш хоссаси билан боғлиқ, бунда металл катионлари депсипептид молекуласининг ички бўш қисмида қутбли амид ва мураккаб эфир боғлари ёрдамида «ушланиб» жойлашиб қолади, мисол тариқасида валиномицинни келтириш мумкин, бундай моддаларга молекуляр контейнерлар ҳам дейилади
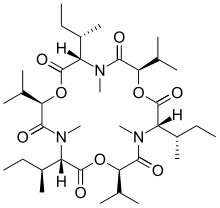
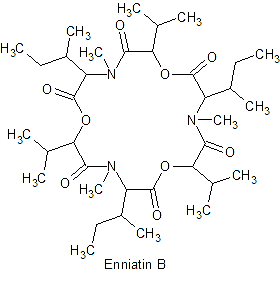
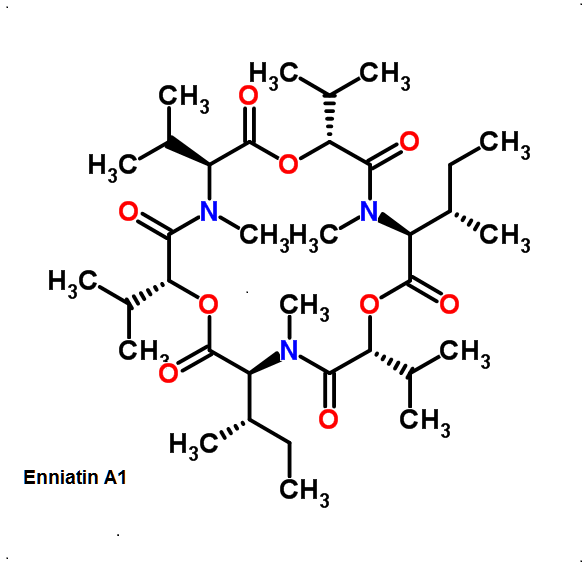
Энниатин А Энниатин В Энниатин А1
Fusarium замбуруғидан олинган депсипептидлар, ОИТС га қарши актив
Мавзуни қайтариш учун саволлар
-
Пептидларнинг классификацияси хақида маълумот беринг.
-
Гомодет пептидлар ва гетеродет пептидлар хақида маълумот беринг.
-
Фойдаланилаётган услубий йўл ва синтез қилинаётган охирги маҳсулот характерига қараб қандай тур пептид синтезлари ажратиб кўрсатилади?
-
Пептидларни полимер ташувчида синтезлашда ўсаётган полипептид занжири эрувчан ёки эримайдиган полимерга қандай боғ орқали боғланган бўлади?
-
Пептидларнинг синтези қайси босқичлардан иборат?
-
Полиаминокислоталарни N-карбоксиаминокислоталар ангидридларидан синтез қилиш қандай амалга ошади?
-
Пептид боғ ҳосил қилишнинг қандай усуллари мавжуд?
-
Аралаш ангидридлар усули қўлланилганда хлоркўмир кислотаси эфирларининг N-алмашинган аминокислоталарга таъсири натижасида қандай маҳсулотлар ҳосил бўлади?
-
Карбодиимид усулининг моҳияти нимадан иборат?
-
Карбоксиангидрид усулининг моҳияти нимадан иборат?
-
Р.Меррифилд пептидларни синтез қилишнинг қайси усулини таклиф этган? Бу усулнинг моҳияти нимада?
-
Қаттиқ фазада пептидлар синтези техникаси қандай имкониятларни беради?
-
Табиий бирикмалар группасини ташкил этган циклопептидларнинг тузилиш принципи қандай?
-
Сидерохромлар (сидерофорлар) қандай пептидлар? Уларнинг асосий хусусияти нимадан иборат?
-
Циклик депсипептидларнинг антибиотик активлиги уларнинг қайси хоссаси билан боғлиқ?
-
Таркибига гидроксикислоталар қолдиқлари кирган депсипептидлар қандай номланади?
-
Циклик депсипептидларнинг антибиотик активлиги уларнинг қайси хоссаси билан боғлиқ?
