- •Часть вторая Циклические соединения
- •Глава 10
- •Алициклические соединения
- •10.1. Способы получения
- •10.2. Химические свойства
- •10.3. Кислородсодержащие производные
- •10.4. Пяти- и шестичленные циклы
- •10.4.1. Способы получения
- •10.5. Циклопентан и его производные
- •10.5. Циклогексан и его производные
- •10.3. Взаимопревращения циклов
- •10.2.4. Полициклические алифатические соединения
- •Способы получения
- •10.2.6. Средние циклы и макроциклы
- •10.2.6.1. Производные циклогептана
- •10.2.6.2. Производное циклооктана
- •10.2.6.3. Макроциклы
- •10.2.6.4. Каркасные алициклы
- •10.2.6.5. Терпеноиды
- •Ароматический ряд
- •Глава 11 Арены
- •11.1. Строение бензола
- •11.2. Ароматичность
- •11.3. Изомерия и номенклатура
- •11.4. Способы получения
- •11.5. Химические свойства
- •Реакции замещения
- •Реакции присоединения
- •Реакции боковой цепи
- •11.5.10. Закономерности реакций электрофильного замещения
- •-Nh2, -nhr, -nr2, -oh, -nhcor, -or, -c6h5, , алкилы, галогены
- •11.5.10.1. Теория резонанса
- •11.5.10.2. Механизм электрофильного замещения в ароматическом ряду
- •11.5.10.2.1. Генерирование электрофильных частиц
- •11.5.10.2.2. Общий механизм электрофильного замещения
- •11.5.10.2.3. Влияние заместителей на скорость замещения
- •11.5.10.2.4. Влияние заместителей на ориентацию
- •11.5.10.2.5. Передача электронных эффектов при замещении
- •Глава 12 арилгалогениды
- •12.1. Методы получения
- •12.2. Химические свойства
- •12.3. Механизмы замещения ароматически связанного галогена
- •Глава 13 Сульфокислоты
- •13.1. Методы получения
- •13.2. Химические свойства
- •13.2.1. Реакции бензольного кольца
- •13.2.2. Реакции сульфогруппы
- •13.2.3. Замещение сульфогруппы
- •Ароматические соединения кислорода
- •Глава 14 Фенолы
- •14.1. Одноатомные фенолы
- •14.1.1. Методы получения
- •14.1.2. Химические свойства
- •Реакции с участием гидроксильной группы
- •Реакции с участием бензольного кольца
- •14.2. Многоатомные фенолы
- •14.2.2. Химические свойства
- •14.3. Хиноны
- •14.4. Ароматические спирты
- •Глава 15 Ароматические альдегиды и кетоны
- •15.1. Альдегиды
- •15.1.1. Методы получения
- •15.1.2. Химические свойства
- •15.2. Кетоны
- •15.2.1. Способы получения
- •15.2.2. Химические свойства
- •15.3.4. Карбоновые кислоты
- •15.3.1. Методы получения
- •15.3.2. Химические свойства
- •Ароматические азотсодержащие соединения
- •Глава 16 Нитросоединения
- •16.1. Получение нитросоединений нитрованием
- •16.2. Химические свойства
- •Глава 17 Амины
- •17.1. Методы получения
- •17.2. Химические свойства
- •Реакции по аминогруппе
- •17.2.1. Основность
- •Реакции с участием бензольного кольца
- •17.3. Соли диазония
- •17.3.1. Методы получения
- •17.3.2. Химические свойства
- •Реакции с выделением азота
- •Глава 18 Полициклические ароматические соединения
- •18.1. Ароматические соединения с изолированными бензольными кольцами
- •18.1.1. Группа дифенила
- •18.1.2. Полифенилалканы
- •18.2. Ароматические соединения с конденсированными бензольными ядрами
- •18.2.1. Нафталин
- •18.2.2. Антрацен и фенантрен
- •Глава 11 Гетероциклические соединения
- •11.2. Гетероциклические ароматические соединения
- •11.2.1. Фуран
- •Реакции электрофильного замещения
- •Реакции присоединения
- •Обмен гетероатома
- •Раскрытие кольца
- •Превращения функциональных производных
- •11.2.2. Пиррол
- •Реакции замещения
- •Реакции присоединения
- •Кислотно-основные свойства
- •Реакции окисления и восстановления
- •Биологически активные соединения на основе пиррола
- •11.2.3. Индол
- •11.4. Тиофен
- •Реакции присоединения
- •11.5. Пиридин
- •Реакции электрофильного замещения
- •Реакции нуклеофильного замещения
- •Пиридин как основание
- •Окисление, восстановление и раскрытие кольца пиридина
- •Оглавление
- •Глава 1. Общие положения органической химии………..
- •Глава 2. Углеводороды
- •Глава 3. Галогенпроизводные углеводородов………………..
- •Глава 4. Спирты и простые эфиры……………………………………
- •Глава 5. Альдегиды и кетоны………….
- •Глава 6. Карбоновые кислоты….
- •Глава 7. Азотсодержащие органические соединения
- •Глава 8. Углеводы….
- •Глава 9. Аминокислоты и белки…
- •Глава 10…
- •Глава 11..
- •Глава 12
- •Глава 13
- •Глава 14
- •Глава 15
- •Глава 16
- •Глава 17
- •Глава 18
- •Глава 19
14.3. Хиноны
Хиноны относятся к сопряженным циклическим дикетонам. У них с фенолами тесные взаимоотношения: фенолы и хиноны легко превращаются друг в друга.
Простейший и наиболее распространенный хинон был получен Воскресенским (1838 г.) окислением хинной кислоты (1,3,4,5-тетраоксигексагидробензойная кислота) двуокисью марганца в серной кислоте
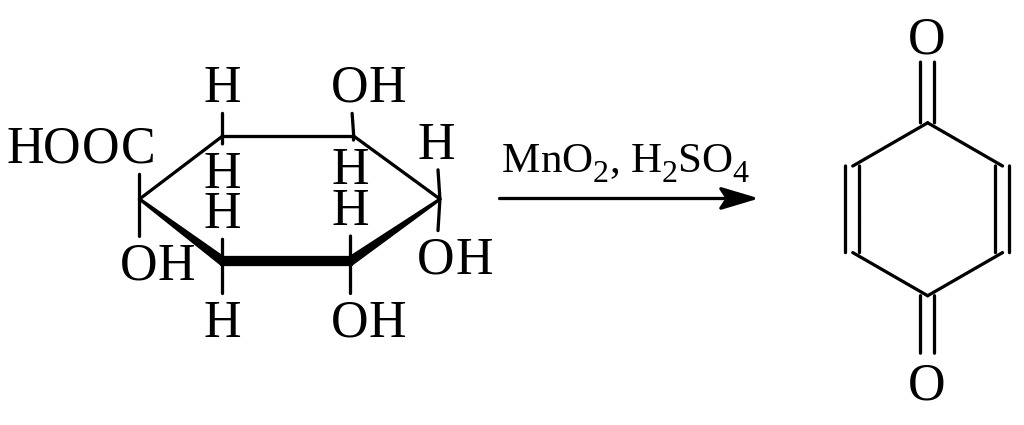
Свое название хинон получил от названия хинной кислоты.
Хиноны подразделяются на 1,2- и 1,4-хиноны или о- и п-хиноны. Как уже отмечалось, 1,3-хиноны не могут существовать по структурным соображениям. Интересно, хиноны различимы по цвету кристаллов: п-хиноны в большинстве случаев бывают желтыми, а о-хиноны – оранжевыми или красными.
Основные методы получения хинонов уже рассматривались – это окисление двухатомных фенолов и окисление анилина хромовой кислотой.
Хиноны обладают высокой реакционной способностью. Направления их превращений предсказуемы: они реагируют как кетоны и одновременно по карбонильной группе и двойным связям. Для них характерны реакции 1,4- и 1,6-присоединения

Хинон как кетон вступает в реакцию с гидроксиламином с образованием моно- и диоксима
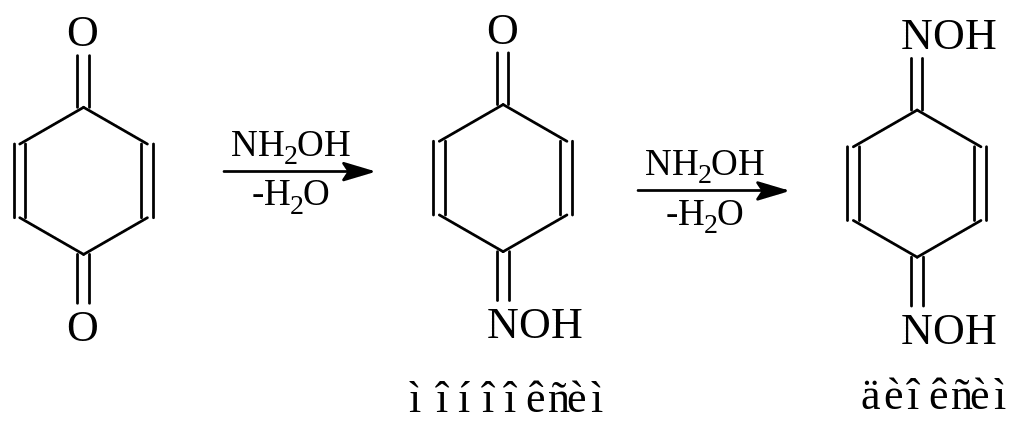
Хиноны вступают в многочисленные реакции присоединения.
Присоединение брома происходит по 3,4-положению п-хинона. Образующийся при этом дибромид легко отщепляет молекулу бромистого водорода и дает замещенный хинон
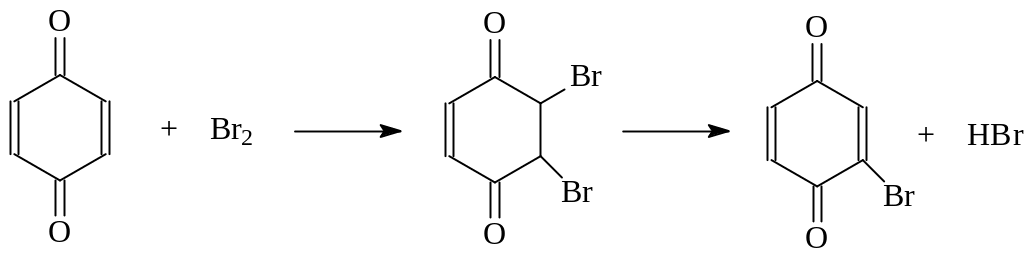
Аналогично протекает присоединение диенов. В реакции Дильса-Альдера хиноны выступают как диенофилы
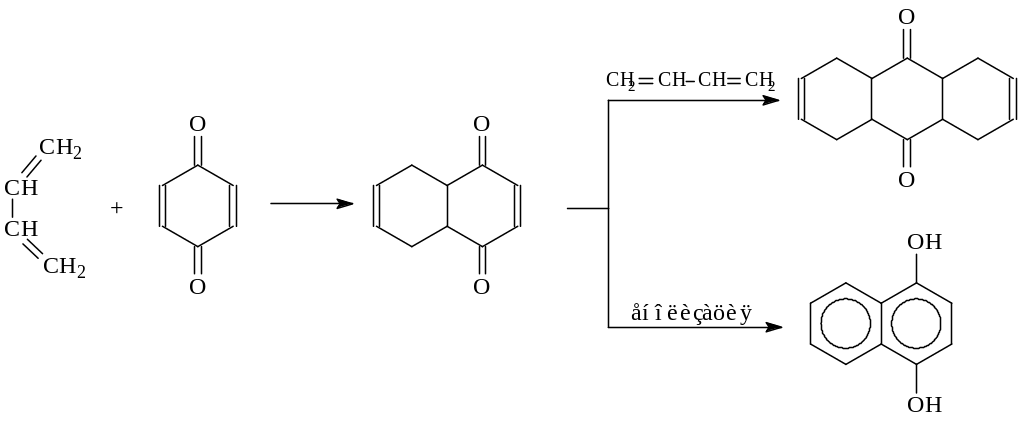
Однако хиноны и сами могут реагировать по 1,3-положению подобно диенам с сопряженными двойными связями. Примером такой реакции является присоединение к хинонам галогенводородных кислот
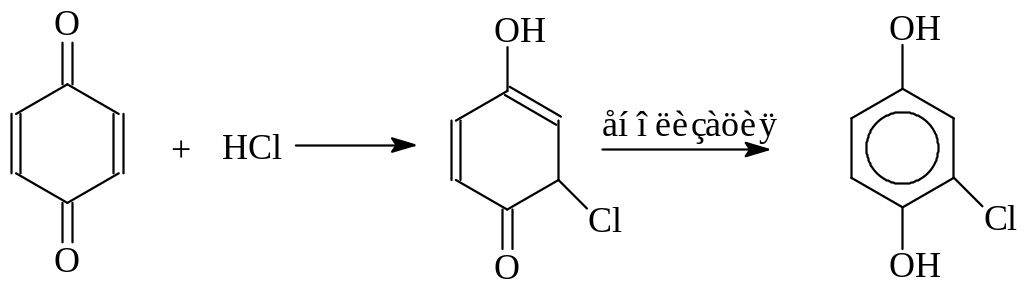
Аналогично присоединяется к хинону и уксусный ангидрид.
Примером реакции 1,6-присоединения является присоединение водорода с образованием двухатомных фенолов
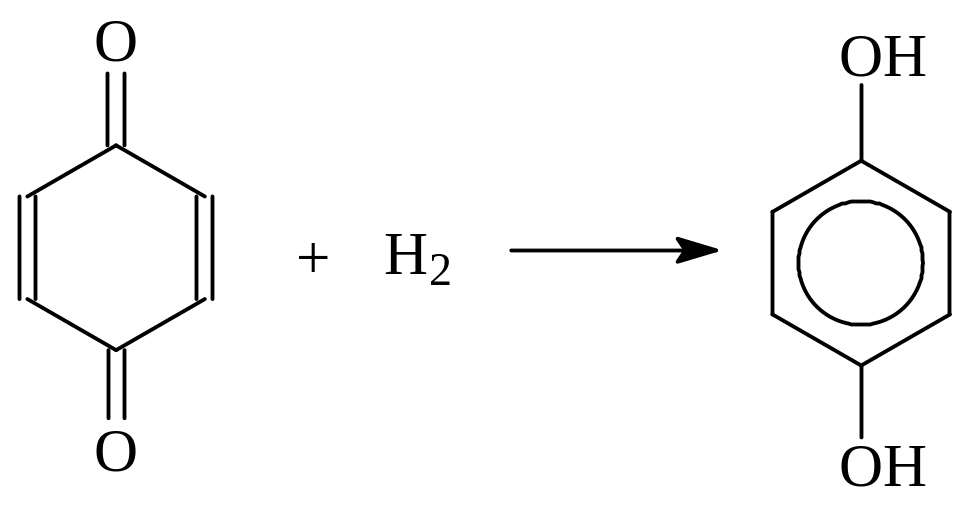
14.4. Ароматические спирты
Ароматические спирты классифицируются в зависимости от взаимного расположения гидроксила и бензольного кольца.
Спирты с α-положением гидроксила содержат гидроксил у углерода боковой цепи, связанного с бензольным кольцом. Их получают с использованием уже известных методов синтеза спиртов.
Галогенпроизводные с α-положением атома галогена легко могут быть получены галогенированием алкилбензолов при освещении ультрафиолетом. Такие галогенпроизводные легко гидролизуются даже при кратковременном нагревании с раствором соды

Другой часто используемый метод – восстановление ароматических альдегидов
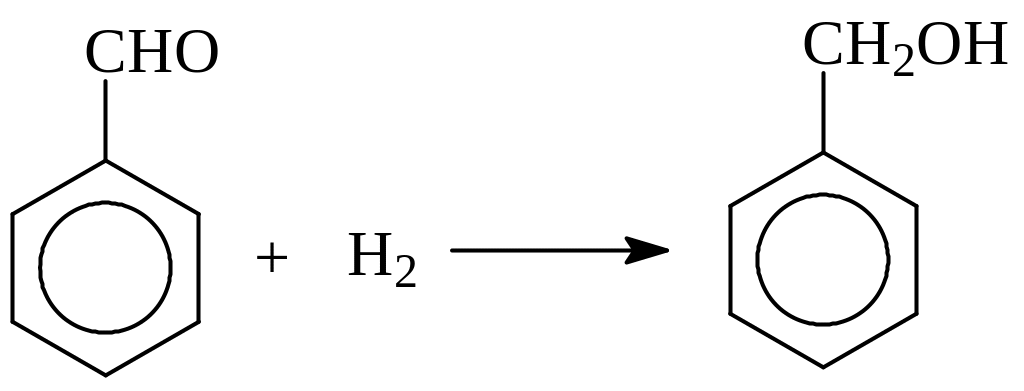
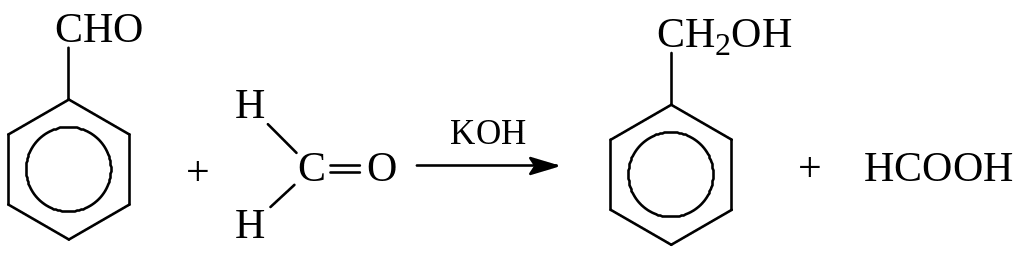
Восстановление альдегидов можно вести и путем вовлечения их в перекрестную реакцию Канницаро когда одним из альдегидов выступает формальдегид. При этом из двух альдегидов формальдегид неизменно окисляется, а ароматический альдегид – восстанавливается
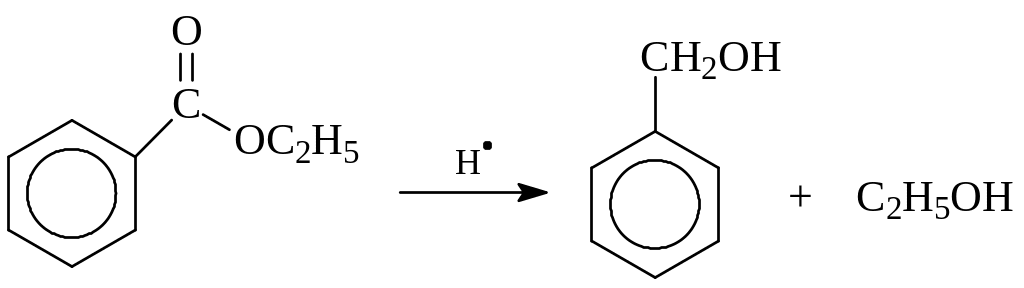
Нередко для получения ароматических спиртов с α-расположением гидроксила исходят из соответствующих сложных эфиров, легко восстанавливающихся атомарным водородом по Буво и Блану (металлический натрий и спирт)
Спирты с β-расположением гидроксила не могут быть получены из соответствующих галогенпроизводных, которые легче подвергаются дегидрогалогенированию, чем гидролизу. Между тем, β-фенилэтиловый спирт широко применяется в парфюмерии («розовое масло»). Поэтому были разработаны эффективные методы его синтеза реакцией фенилмагнийбромида с окисью этилена
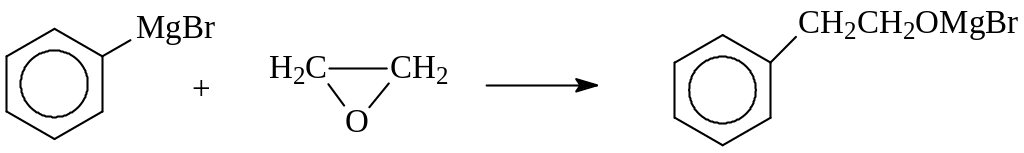
В последующем оказалось, что реакцию можно существенно упростить, сведя ее к реакции Фриделя-Крафтса
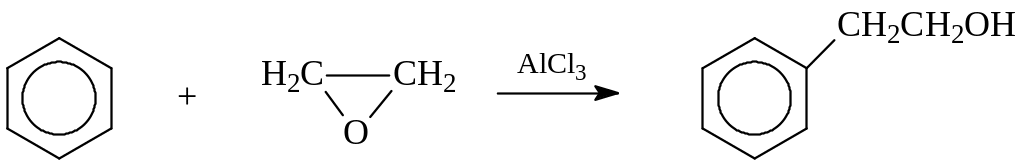
Представитель ароматических спиртов с γ-положением гидроксила - γ-фенилпропиловый спирт – легче всего синтезировать восстановлением коричной кислоты
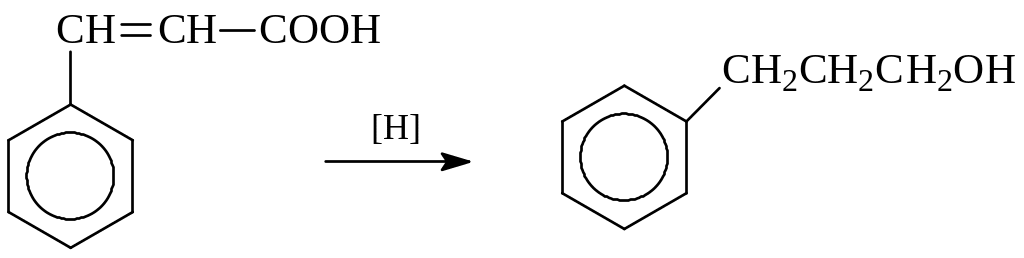
Сама кислота получается из бензальдегида и уксусного ангидрида при их конденсации по Перкину.
γ-Фенилпропиловый спирт обладает запахом гиацинтов и применяется в парфюмерии.
Ароматические спирты по своим свойствам повторяют свойства спиртов алифатического ряда.
К особенностям ароматических спиртов можно отнести ту легкость, с которой происходит замещение гидроксила на галоген у спиртов типа бензилового спирта (SN1).

Это объясняется стабильностью бензилового карбкатиона с участием бензольного кольца.
Спирты с β-расположением гидроксильной группы легко дегидратируются в арилолефины