
Современные проблемы и методы биотехнологии
.pdf
ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
нее токсична для насекомых, которые не являются мишенью ее токсического воздействия у растений, синтезирующих инсектициды.
Для генома хлоропластов характерен высокий уровень полиплоидии – 10–100 копий на хлоропласт. Учитывая большое число самих хлоропластов на клетку, каждая отдельная клетка с трансформированными хлоропластами содержит тысячи копий трансгена, что позволяет получать очень высокий уровень экспрессии соответствующих рекомбинантных белков (до 25 % от суммарного растворимого клеточного белка).
Транзиентная «временная» экспрессия в растениях – это еще один путь для синтеза чужеродных целевых белков. Преимущество транзиентной экспрессии заключается в том, что этот метод не приводит к возникновению трансгенного растения с его экологическими и другими ограничения для ГМО. Чаще всего для этого используются векторы на основе различных фитовирусов, например, вируса табачной мозаики (ВТМ), вируса мозаики коровьего гороха (ВМКГ). Заражение растительных тканей производят рекомбинантными вирусами, несущими в своем составе гены целевых белков. Скорость мультипликации вирусной РНК в растениях чрезвычайно высока, за счет чего достигается высокая копийность транскриптов чужеродных генов в цитоплазме зараженных клеток. Поэтому продуктивность вирусной системы экспрессии в среднем на 2 порядка выше по сравнению со стабильной трансформацией растений. Иногда такую технологию применяют для масштабного коммерческого производства.
Для транзиентной продукции в растениях также используют векторы Ti-системы. При инфицировании целого растения или его части (листья) рекомбинантной Agrobacterium, содержащей целевой ген в составе бинарного вектора, уровень продукции чужеродного белка может достигать 10–30 % от общего растворимого белка растения в короткое время (5–10 дней). Такой способ также используется, когда требуется проверить сконструированную экспрессионную кассету перед получением стабильных трансформантов или разово наработать небольшое количество (порядка миллиграмма) рекомбинантного белка, например, для оценки его качества или доклинических испытаний.
2.3.2.Преимуществаипроблемыбиопродукции
врастительнойсистеме
Биопродукция чужеродных белков в растительных клетках имеет ряд особенностей и преимуществ. Прежде всего, в клетках высших растений происходят гликозилирование и фолдинг белков, сходные с таковым в клетках млекопитающих, но получение трансгенных растений намного проще по сравнению с животными. Культивирование растений не требует дорогостоя-
Современные проблемы и методы биотехнологии. Учеб. пособие |
91 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
щего оборудования (ферментеры), культуральных сред и системы стерильности, стоимость выращивания растений несравнимо ниже стоимости культивирования клеток бактерий, дрожжей, насекомых или животных. Сельскохозяйственные масштабы продукции позволяют получать рекомбинантные белки и метаболиты в достаточных количествах. В отличие от животных, растительные клетки не содержат в своем составе патогенные для человека вирусы, а также прионы и, таким образом, могут служить безопасным источником рекомбинантных препаратов медицинского назначения. Хотя стоимость выделения и очистки целевого белка из растений-продуцентов может быть сопоставима с таковой для других систем, наработка сырого материала обходится значительно дешевле. В ряде случаев, например, при использовании трансгенных растений в качестве «съедобных вакцин» выделение белка в чистом виде не требуется.
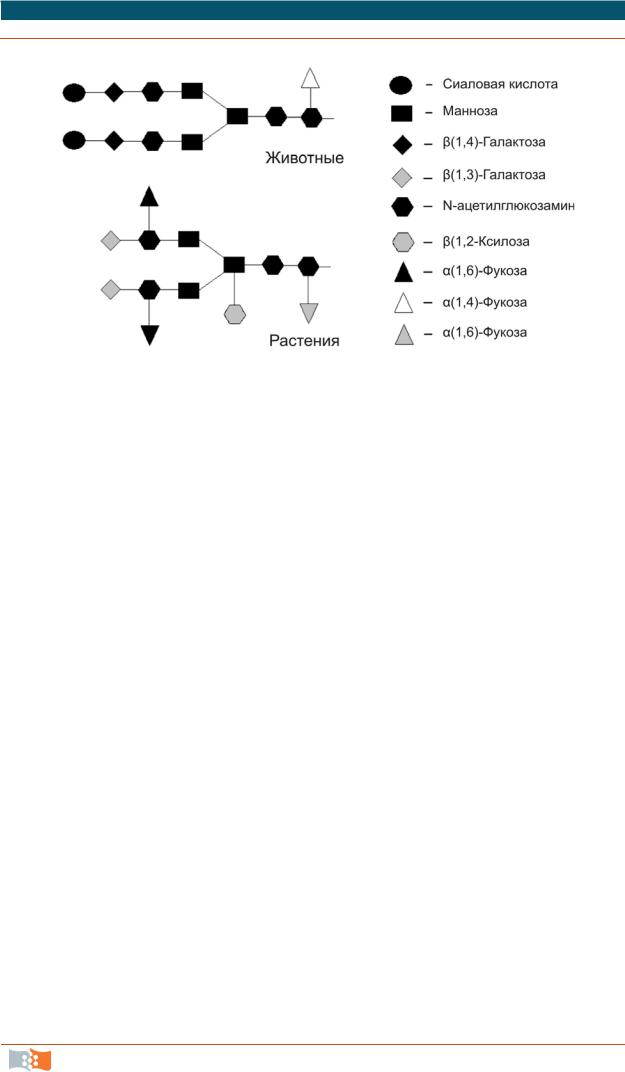
Гликозилирование в клетках высших растений сходно с клетками млекопитающих, но имеются и отличия, которые могут повлиять на биологическую активность синтезируемых рекомбинантных белков в растительной системе. У растений гликопротеины имеют два углеводных остатка, не встречающихся у млекопитающих – β(1,2)-ксилозу и α(1,3)-фукозу (рис. 2.14). Эти олигосахаридные остатки могут стать аллергенами для человека, поскольку в некоторых экспериментах в крови подопытных животных обнаруживались специфические иммуноглобулины IgE против растительных углеводных детерминант. Различия в гликозилировании у растений и животных могут быть особенно важны при использовании в медицине антител, синтезированных в растениях.
В животных клетках ключевым ферментом, превращающим N-гликаны растений в N-гликаны млекопитающих, является β(1,4)-галактозилтрансфераза. Если ввести этот ген в растения, можно получить гликозилирование белков по типу клеток млекопитающих. Было проведено скрещивание трансгенных растений табака, синтезирующих этот фермент, с растениями-продуцентами тяжелой и легкой цепей антител. У полученного потомства, содержащего все три белка, до 30 % иммуноглобулинов имели галактозилированные N-гликаны. Таким образом, существует возможность изменить тип гликозилирования белков человека в трансгенных растениях. Вероятно, эта проблема будет решена тем или иным путем и антитела, синтезированные в растениях, будут широко использоваться в медицине.
Современные проблемы и методы биотехнологии. Учеб. пособие |
92 |
ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
Рис. 2.14. Общая схема гликозилирования белков в клетках животных и растений
Уровень синтеза рекомбинантных белков в растительной клетке.
Хотя идея внедрения экзогенной ДНК в растительный геном для наработки соответствующих продуктов в растении представляется весьма перспективной, этот подход не лишен и некоторых недостатков. Среди них необходимо отметить частый низкий уровень экспрессии перенесенных генов, даже при использовании очень сильных промоторов. Например, первые эксперименты по экспрессии различных человеческих белков в трансгенном табаке дали очень низкий выход – содержание сывороточного альбумина человека составило приблизительно 0,02 %, эритропоэтина – 0,003 % и b -интерферона – 0,001 % от суммарного белка листьев. Одной из причин этого, по-видимому, является увеличение скорости деградации мРНК чужеродного гена, когда ее уровень достигает порогового значения. Этот механизм, возможно, служит одним из способов защиты растения от РНК-содержащих вирусов. Повысить продукцию чужеродных белков в растениях в некоторых случаях удалось введением трансгена в геном хлоропластов, например, в этом случае человеческий сывороточный альбумин составил более 11 % от растворимого белка клеток, человеческий гормона роста – до 7 %.
Второй причиной низкого уровня продукции является протеолиз чужеродных белков в цитоплазме растительной клетки. Введение в полипептидную цепь целевого белка сигнальных последовательностей, направляющих его накопление в эндоплазматической сети или секрецию в апопласт, где частота протеолиза значительно ниже, позволяет достичь повышения продуктивности трансгенных растений в 100 раз. Экспрессия целевых белков в запасной ткани семян, где уровень биодеградации ниже, чем в обводненных тканях (листья, плоды), способствует повышению продуктивности на 2-3 порядка. Так, например, уровень синтеза гирудина, слитого с олеозином (белком из масляных телец), в семенах трансгенного рапса достигал 0,3 %. Уро-
Современные проблемы и методы биотехнологии. Учеб. пособие |
93 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
вень синтеза под глютелиновым промотором энкефалина человека, направленного в компартменты накопления запасных белков сигнальной последовательностью глютелина (запасной белок риса), составил 2,9 % от тотального белка в семенах арабидопсиса.
Очевидно, что многие проблемы в получении высокоэффективных стабильных трансгенных растений для хозяйственных целей в настоящее время обусловлены недостатком фундаментальных знаний о функционировании генома высших растений. В частности, пока нет ясного понимания того, каким образом происходит включение и выключение генов в ДНК растений.
Сайленсинг генов (gene silencing) – явление «замолкания» генов в последующих поколениях – было обнаружено уже через несколько лет после создания первых трансгенных растений. Было выявлено, что у достаточно заметной доли трансгенных растений интродуцированный ген через какое-то время теряет свою активность – «замолкает», хотя физически сохраняется в геноме. Таким образом, было установлено, что растение обладает способностью активно противостоять экспрессии чужеродной ДНК. Как правило, перенесенные гены наследуются согласно законам Менделя, однако к настоящему времени накоплено достаточно много примеров отклонений от менделевского наследования, обусловленных инактивированием трансгенов. Несмотря на интенсивные исследования этого явления во многих ведущих биотехнологических центрах мира, причины и молекулярно-генетические механизмы все еще остаются до конца не выясненными.
Проблема замолкания генов имеет большое практическое значение, так как у генетически трансформированных сельскохозяйственных культур трансгены должны функционировать стабильно. За последние годы удалось выяснить механизмы и некоторые условия, способствующие замолканию генов при интеграции в ядерный геном растений. Один из основных факторов – число идентичных копий гена, встроенных в геном: чем больше таких копий и чем они протяженнее, тем больше вероятность замолкания генов. Откуда следуют практические рекомендации генным инженерам: трансгенные культуры должны содержать не более одного встроенного гена на гаплоидный геном; сигнальные части и регуляторные части чужеродной ДНК (промоторы, терминаторы и др.) не должны иметь длинных гомологий (более 100–300 нп) с участками хозяйского генома; фрагменты векторной плазмидной или вирусной ДНК должны быть по возможности полностью удалены из конструкции перед встраиванием рекомбинантной ДНК в растительные клетки.
2.3.3. Областиприменениягеннойинженериирастений
Метаболическая инженерия растений направлена на проведение трансгенной клеткой новых биохимических реакций путем введения чужеродных генов или модификацией генов клетки-хозяина. Растения представляют один из наиболее привлекательных объектов для метаболической инженерии. Имея одинаковые пути синтеза основных биологических соедине-
Современные проблемы и методы биотехнологии. Учеб. пособие |
94 |
ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
ний, растения отличаются поразительным разнообразием своих конечных продуктов: сахаров, ароматических соединений, жирных кислот, стероидных соединений и других биологически активных веществ. Растения дают человечеству десятки тысяч природных продуктов, многие из которых представляют большую ценность для фармакологии и промышленности.
Иногда такими продуцентами важных лекарственных веществ являются уникальные тропические и эндемические растения, недоступные для их агротехнического производства в умеренных климатических зонах большинства развитых стран мира. Выделение из таких растений генов, определяющих направленный синтез специфических органических соединений, и их перенос в подобранные соответствующие растения превращают их в новые продуценты важных биологически активных веществ.
Многие растения содержат
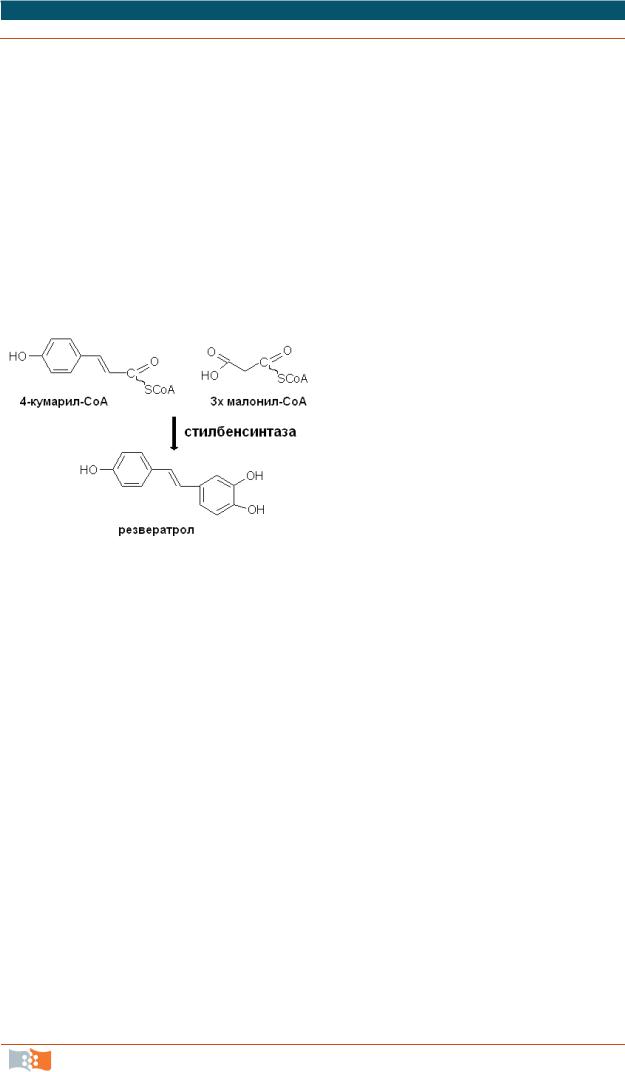
предшественников биосинтеза ценных биологических соединений, однако они не имеют ферментов для их превращений в эти соединения. Часто для метаболической инженерии достаточно переноса в клетку только одного гена. Примером такого типа метаболической инженерии является получение новых растенийпродуцентов резвератрола, ценного лекарственного препарата широкого спектра действия, замедляющего старение. Резвератрол был обнаружен в винограде, где фермент стилбенсинтаза катализирует реакцию синтеза резвератрола из трех
молекул малонил-СоА и одной молекулы 4-кумарил-СоА (рис. 2.15). Переносом гена стилбенсинтазы были получены другие растения, синтезирующие резвератрол.
Создание растений с улучшенными лечебно-диетическими свойст-
вами поможет улучшить пищевую ценность растений. Ранее было практически невозможно с помощью селекции вывести растения с повышенным содержанием витаминов. Однако с развитием биохимии растений стало более ясным, какие метаболические пути являются критическими для биосинтеза витаминов. Например, для синтезаβ -каротина (провитамина А) в растениях необходима фитоен-синтетаза. Этот фермент участвует в конденсации двух молекул геранил-геранил дифосфата. Ген фитоен-синтетазы из нарцисса был введен в рис и экспрессирован в эндосперме риса. Таким образом, получен «золотой рис», который может помочь 2 млрд чел., страдающих от дефицита витамина А, для них рис – основная пища. Получены трансгенные растения рапса, экспрессирующие ген фитоен-синтетазы, в семенах которых значи-
Современные проблемы и методы биотехнологии. Учеб. пособие |
95 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
тельно повысилось содержание каротиноидов. Показана экспрессия этого же фермента в клубнях картофеля, что приводило к повышенному синтезу каротиноидов и лютеина.
Недавно получены трансгенные растения земляники с повышенным синтезом L-аскорбиновой кислоты. Эти растения отличались суперэкспрессией гена НАДФ-зависимой Д-галактуронат-редуктазы (GalUR). Созданы растения сои с повышенным в пять раз содержанием витамина Е в семенах. Получены растения арабидопсиса с повышенным содержанием фолатов за счет экспрессии в них бактериального гена ГТФ-циклогидролазы-1 (EcGCH). Уже существует салат с увеличенным содержанием железа, обогащенная лизином кукуруза. Ждет своего запуска в практику сорт сои с повышенным содержанием ненасыщенных жирных кислот (омега-3, омега-6 НЖК и др.), которые не синтезируются в организме человека, а попадают по пищевым цепям в основном через морепродукты из водорослей. Гены, встраиваемые в геном соевых бобов, были выделены из клеток водорослей (разработчик – компания Monsanto).
Разработаны в лабораториях и другие разнообразные трансгенные формы растений с улучшенными лечебно-диетическими свойствами.
Самый первый коммерческий успех получили растения, устойчивые к гербицидам, поскольку позволили очень успешно бороться с сорняками. Самыми распространенными являются трансгенные растения, устойчивые к глифосату (Раундап) – самому популярному гербициду, разлагающемуся в почве на нетоксичные составляющие и потому безопасному для окружающей среды. Ген был выделен из глифосат-устойчивого штамма E. coli.
Выведение растений, устойчивых к вредителям и болезням, помо-
жет резко сократить применение химических средств защиты растений и уменьшить стоимость культивирования. Одними из первых в широкую практику вошли инсектицидные хлопок и кукуруза – так называемые Bt-сорта, которые были получены введением в них гена дельта-эндотоксина из Bacillus. thuringiensis (Bt или Cry-белок). Bt-белок высокотоксичен для насекомых, но безопасен для других видов животных и человека. Он является протоксином, который расщепляется в кишечнике личинок насекомых, образуя активированный токсин. Активированный токсин, в свою очередь, специфично связывается с рецепторами в средней кишке насекомых, что приводит к лизису клеток кишечного эпителия. Данный энтомотоксин – смертельный яд для ряда насекомых (в том числе и колорадского жука), но в то же время вполне безопасен для человека и животных, поскольку в организме млекопитающих нет ферментов для его расщепления и усвоения. Взаимодействие Bt-токсина с рецепторами насекомых строго специфично. В природе найдено большое количество штаммов B. thuringiensis, чьи токсины действуют на строго определенные виды насекомых.
Современные проблемы и методы биотехнологии. Учеб. пособие |
96 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
Ранее препараты бактерий B. thuringiensis, содержащие Bt-белок, с успехом применяли для борьбы с насекомыми-вредителями, хотя использование таких препаратов достаточно дорого и не всегда эффективно. Введение гена протоксина в растения привело к тому, что Bt-растения перестали поедаться насекомыми. Этим путем был получен трансгенный картофель, устойчивый к колорадскому жуку.
Устойчивость к вирусам может обладать исключительной важностью для повышения сельскохозяйственной продуктивности. В настоящее время в различных странах мира проводят полевые испытания устойчивых к вирусам сортов батата (вирус SPFMV, sweet potato feathery mottle virus), кукурузы
(MSV, maize streak virus) и африканской маниоки (мозаичный вирус). Возможно, эти культуры будут коммерциализованы в течение ближайших 3–5 лет. Из-за сложности генома пшеницы, работа над созданием сортов, устойчивых к вирусу желтой карликовости ячменя (barley yellow-dwarf virus), продвигается очень медленно и до сих пор находится на стадии лабораторных экспериментов. Разработан также устойчивый к нематодам (корневым червям) ГМ-картофель.
Генно-инженерная биотехнология растений для фармакологии делает свои первые успешные практические шаги. Растения являются удобной, безопасной и экономически выгодной альтернативой для получения различных белков, вакцин и антител по сравнению с системами экспрессии на основе микроорганизмов, культур животных клеток или трансгенных животных. За последние 20 лет множество ценных белков эффективно экпрессировано в растениях. Это белки человеческой сыворотки, регуляторы роста, антитела, вакцины, промышленные ферменты, биополимеры и реагенты для молекулярной биологии. Следует отметить перспективность получения ГМ-растений, синтезирующих новые формы антимикробных пептидов.
Растительные системы имеют все перспективы успешного использования для производства рекомбинантных белков в промышленном масштабе. Некоторые белки, синтезируемые трансгенными растениями, уже производятся западными компаниями или будут выпущены на рынок в ближайшие годы. Например, авидин, трипсин иβ -глюкуронидаза, выделяемые из трансгенной кукурузы, производятся фирмой Sigma-Aldrich (США). В скором времени должны быть подготовлены к промышленному производству коллаген, липаза, лактоферрин, лизоцим, синтезируемые трансгенными растениями.
Синтез субъединичных вакцин в трансгенных растениях. Выявлен-
но, что при экспрессии различных антигенов в растениях сохраняется их структурная идентичность и иммуногенность. Антигены, синтезируемые растениями, вызывали иммунный ответ при введении, например, HBs-антиген, синтезируемый растениями картофеля, вызывал у мышей более сильный иммунный ответ, чем дрожжевой. В настоящее время более пятидесяти различных антигенов были экспрессированы в ГМ-растениях, для некоторых из них
Современные проблемы и методы биотехнологии. Учеб. пособие |
97 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
показана иммуногенность при оральном введении. Интенсивно разрабатывается концепция «съедобных вакцин» на основе трансгенных растений, чьи плоды, листья и семена годятся в пищу. В случае успеха исчезнет потребность в дорогостоящей очистке антигенов, которая необходима при создании вакцин для парентерального введения. Антигены, экспрессируемые в растениях, защищены растительными клеточными стенками от протеолиза при прохождении пищеварительного тракта и могут быть легко доставлены к клеткам слизистой оболочки кишечника, ответственным за мукозную систему иммунитета.
Таким образом, непрерывно разрабатываются все новые виды пищевых и технических растений с измененными свойствами – с улучшенным составом жиров, повышенным содержанием белков и витаминов, сладкие без сахара и накапливающие меньше вредных для здоровья нитратов, с повышенными декоративными свойствами. Опытные испытания проходят сотни пород деревьев, у которых часть ненужного человеку лигнина заменена полезной целлюлозой. При этом растут ГМ-деревья вдвое быстрее обычных. Трансгенные растения вырабатывают вакцины и лекарства, очищают почву от химического и радиоактивного загрязнения, синтезируют биодеградируемые полимеры для производства упаковки и белок паутины, из которого можно делать колготки и бронежилеты повышенной прочности.
2.3.4.Коммерциализациятрансгенныхрастений
ибиобезопасность
Смомента публикации в 1983 г. первых работ по получению трансгенных растений табака прошло не очень много времени, но существующее сейчас количество самых разнообразных трансгенных растений уже не поддается учету. И, несмотря на то, что путь от лабораторного получения трансгенного растения до его коммерческого применения довольно долог, в настоящее время в сельскохозяйственном производстве общие площади биотехнологических культур достигли уже 114,3 млн га (рис. 2.16, табл. 2.2). Разрешения на коммерческое использование дожидаются сотни сортов десятков видов пищевых растений и технических растений с самыми разнообразными новыми свойствами. Новые культуры проходят длительную всестороннюю тщательную проверку в отношении биобезопасности.
Самыми распространенными из трансгенных сельскохозяйственных растений является соя (51 %), за ней следуют быстро набирающая объемы культивирования кукуруза (31 %), хлопок (13 %) и рапс (5 %). Необходимо отметить, что некоторые генно-модифицированные культуры (например, ГМ-соя) уже обогнали позахваченной площади свои «традиционные» аналоги.
Современные проблемы и методы биотехнологии. Учеб. пособие |
98 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
Рис. 2.16. Рост общих площадей под посевами биотехнологических культур в 1996–2007 гг. (по данным ISAAA). В 2007 г. по сравнению с 2006 г. произошло увеличение площадей на 12 % или 12,3 млн га (разрешено к публикации www.isaaa.com)
По рейтингу свойств коммерциализированных трансгенных растений, составленному Международной службой по использованию агробиотехнологии (ISAAA), на протяжении всего периодакультивирования с 1996 по 2007 гг. первое место занимают гербицидоустойчивые культуры, затем следуют Bt-культуры, устойчивые к насекомым-вредителям, за ними – комбинированные культуры (оба этих признака), в последние годы появились культуры, совмещающие три признака. В 2007 г. все устойчивые к гербицидам культуры (соя, кукуруза, рапс, хлопок, люцерна и др.) суммарно занимали 63 %; Bt-культуры –18 %; комбинированные культуры с двумя или тремя признаками –19 %. В 2007 г. по сравнению с 2006 г. быстрее всего увеличивались площади посевов комбинированных культур (с двумя и тремя признаками) – на 66 %; затем идут Bt -культуры – 7 % роста и устойчивые к гербицидам культуры – 3 % роста.
Начинает увеличиваться доля культивируемых трансгенных растений, устойчивых к вирусам, грибкам, нематодам и другим вредителям, холоду, жаре, засухе или долго не портящихся при хранении. Новые сорта способны не только расти, но и приносить хороший урожай там, где старые сорта просто не могли выжить (слишком холодно или тепло, или сухо). Например, Северная Дакота, ранее считавшаяся совершенно не пригодной для выращивания соевых бобов, в настоящее время уже стала одним из главных поставщиков этой культуры в США.
Современные проблемы и методы биотехнологии. Учеб. пособие |
99 |

ГЛАВА 2. СОВРЕМЕННЫЕ УСПЕХИ ГЕНОМИКИ: ТРАНСГЕННЫЕ ОРГАНИЗМЫ
2.3. Трансгенные растения и животные как биореакторы
Таблица 2.2
Посевные площади, занятые трансгенными растениями в 2007 г. (разрешено к публикации www.isaaa.com)
№ |
Страна |
Площадь, |
ГМ-растения |
|
|
млн га |
|||||
|
|
|
|
||
1* |
США |
57,7 |
Соя, кукуруза, хлопок, рапс, папайя, бахчевые, люцерна |
|
|
2* |
Аргентина |
19,1 |
Соя, кукуруза, хлопок |
|
|
3* |
Бразилия |
15,0 |
Соя, хлопок |
|
|
4* |
Канада |
7,0 |
Соя, кукуруза, рапс |
|
|
5* |
Индия |
3,2 |
Хлопок |
|
|
6* |
Китай |
6,8 |
Хлопок, томаты, сладкий перец, папайя, тополь, петуния |
|
|
7* |
Парагвай |
2,6 |
Соя |
|
|
8* |
Южная Африка |
1,8 |
Соя, кукуруза, хлопок |
|
|
9* |
Уругвай |
0,5 |
Соя, кукуруза |
|
|
10* |
Филиппины |
0,3 |
Кукуруза |
|
|
11* |
Австралия |
0,1 |
Хлопок |
|
|
12* |
Испания |
0,1 |
Кукуруза |
|
|
13* |
Мексика |
0,1 |
Соя, хлопок |
|
|
14 |
Колумбия |
<0,1 |
Хлопок, гвоздика |
|
|
15 |
Чили |
<0,1 |
Соя, кукуруза, рапс |
|
|
16 |
Франция |
<0,1 |
Кукуруза |
|
|
17 |
Гондурас |
<0,1 |
Кукуруза |
|
|
18 |
Чехия |
<0,1 |
Кукуруза |
|
|
19 |
Португалия |
<0,1 |
Кукуруза |
|
|
20 |
Германия |
<0,1 |
Кукуруза |
|
|
21 |
Словакия |
<0,1 |
Кукуруза |
|
|
22 |
Румыния |
<0,1 |
Кукуруза |
|
|
23 |
Польша |
<0,1 |
Кукуруза |
|
|
|
* Наиболее |
биотехнологически развитые страны выращивают более 50 тыс. га |
|||
трансгенных растений (13 стран). |
|
|
|||
Широкое распространение сельскохозяйственных трансгенных растений объясняется тем, что их культивирование позволило фермерам резко повысить урожаи, при этом снизить закупки гербицидов (средств борьбы с сорняками) и закупки инсектицидов. Например, проведенные в Индии и Китае в 2007 г. исследования показали, что использование Bt-хлопка дало возможность увеличить урожайность до 50 и 10 % соответственно и сократить использование инсектицидов в обеих странах до 50 % и более. Выращивание гербицидоустойчивых растений требует в 2–4 раза меньше гербицидных обработок полей. Не случайно за годы использования трансгенных растений продажи химических средств защиты растений неуклонно снижаются.
Трансгенные посадки продолжают разрастаться по всему миру. В среднем за год они увеличиваются на 10–15 %. Хотя несомненным лидером в культивировании трансгенных растений по-прежнему остаются США (табл. 2.2), их доля неуклонно уменьшается, поскольку все больше стран начинают использовать ГМ сорта в сельском хозяйстве.
Современные проблемы и методы биотехнологии. Учеб. пособие |
100 |
