
- •Раздел 1. Техническая термодинамика
- •Изучение конструкций приборов для измерения параметров состояния рабочих тел
- •Краткие теоретические сведения
- •Типы измерительных приборов
- •Манометрические термометры.
- •Сильфоны.
- •Термоэлектрические термометры – термопары.
- •Жидкостные манометры.
- •Деформационные манометры.
- •Максиметры.
- •Грузопоршневые манометры.
- •Мерные устройства (штихпроберы).
- •Счетчики с крыльчатыми вертушками (радиальные).
- •Счетчики с винтовыми вертушками (осевые).
- •Дросселирование газа диафрагмой (дроссельной шайбой) .
- •Контрольные вопросы
- •Определение газовой постоянной
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок выполнения работы
- •Обработка результатов опыта
- •Контрольные вопросы
- •Определение удельной объемной изобарной теплоемкости воздуха
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок проведения опыта
- •Обработка результатов опыта
- •Контрольные вопросы
- •Определение показателя адиабаты для воздуха
- •Краткие теоретические сведения
- •Методика проведения работы
- •Описание установки
- •Порядок проведения опыта
- •Обработка результатов опыта
- •Контрольные вопросы
- •Исследование изохорного процесса
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок выполнения опыта
- •Обработка результатов опыта
- •Оценка погрешности
- •Контрольные вопросы
- •Исследование политропного процеса при истечении газа
- •Краткие теоретические сведения
- •Описание установки
- •Порядок выполнения работы
- •Обработка результатов исследования
- •Оценка погрешности
- •Контрольные вопросы
- •Определение термодинамических свойств воды и водяного пара
- •Краткие теоретические сведения
- •Описание экспериментальной установки
- •Порядок проведения эксперимента
- •Раздел 2. Теория теплообмена
- •Исследование теплообмена при кипении
- •Краткие теоретические сведения.
- •Теплоотдача при пузырьковом кипении жидкости в условиях свободного движения
- •Эмпирические формулы.
- •Описание установки
- •Формулы используемые при выполнении л.Р.
- •Контрольные вопросы
- •Дополнительные вопросы.
- •Примеры выполнения лабораторной работы.
- •Опеределение коэффициента теплопроводности теплоизоляционного материала методом трубы
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок выполнения работы
- •Обработка результатов опыта
- •Оценка погрешности
- •Контрольные вопросы
- •Исследование теплоотдачи от металлического стержня
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок выполнения работы
- •Обработка результатов
- •Контрольные вопросы
- •Определение коэффициента теплоотдачи от вертикального цилиндра при свободной конвекции
- •Краткие теоретические сведения
- •Методика выполнения работы
- •Описание установки
- •Порядок выполнения работы
- •Обработка результатов
- •Оценка погрешности
- •Контрольные вопросы
- •Исследование теплопередачи в водяном теплообменнике
- •Краткие теоретические сведения
- •Описание экспериментальной установки
- •Порядок выполнения работы
- •Обработка результатов опыта
- •Оценка погрешности
- •Контрольные вопросы
Методика выполнения работы
В основу экспериментального определения газовой постоянной положено выражение (2), из которого получаем
R
=
![]()
При изменении давления газа в сосуде на величину δр и его массы на δm газовая постоянная находится из выражения
R
=
![]() (5)
(5)
Давление газа δр, температуру t и массу m измеряют с помощью приборов.
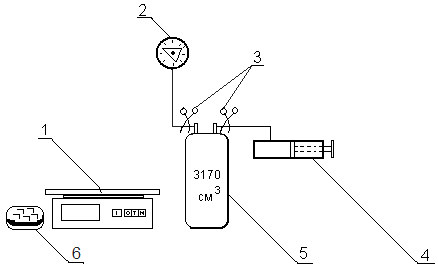
Описание установки
Тонкостенный металлический сосуд 5 объемом V,см3 с помощью резиновых трубок присоединяется к насосу 4 и манометру 2. Масса сосуда измеряется с помощью электронных весов 1, а температура – с помощью жидкостного термометра.
Порядок выполнения работы
Устанавливают
электронные весы 1 на нулевое деление.
Взвешивают массу m1
сосуда 5 вместе с зажимами 3 с точностью
до 0,1 г, используя довесы 6 массой 0,1 г
каждый. Подсоединяют сосуд 5 к насосу 4
(н) и манометру 2 установки, создают
насосом избыточное давление в сосуде
1-1,5 кг/см2.
Сразу после установления соответствующего
давления пережимают зажимом 3 трубку
от сосуда к насосу и отсоединяют трубку
насоса. Давление в сосуде измеряют через
8-10 мин., когда оно перестанет уменьшаться.
Записывают давление
![]() Пережимают
зажимом 3 трубку сосуда на участке до
соединения ее с трубкой манометра,
Взвешивают сосуд с зажимами и определяют
массу сосуда с воздухом m2.
Измеряют температуру воздуха t,0С
по имеющемуся в лаборатории термометру.
Пережимают
зажимом 3 трубку сосуда на участке до
соединения ее с трубкой манометра,
Взвешивают сосуд с зажимами и определяют
массу сосуда с воздухом m2.
Измеряют температуру воздуха t,0С
по имеющемуся в лаборатории термометру.
Полученные данные заносят в таблицу.
№ опыта |
|
m1, кг |
m2, кг |
t, 0С |
V, см3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Обработка результатов опыта
Размерность
всех параметров приводят к системным
единицам. Определяют массу
![]() воздуха
в сосуде как разность m2
-
m1
и
по
уравнению (5) определяют газовую
постоянную. Найденное значение газовой
постоянной сравнивают с ее табличным
значением R=287
Дж/кг град.
воздуха
в сосуде как разность m2
-
m1
и
по
уравнению (5) определяют газовую
постоянную. Найденное значение газовой
постоянной сравнивают с ее табличным
значением R=287
Дж/кг град.
Контрольные вопросы
Что называется идеальным газом? Каким закономерностям он подчиняется?
В каком случае реальный газ может считаться идеальным?
Какие величины называются параметрами состояния? Назовите основные термодинамические параметры состояния, дайте их определение. укажите размерность.
Сформулируйте законы Бойля-Мариотта, Гей-Люссака и объединенный закон Клапейрона.
Напишите уравнение состояния идеального газа для 1 кг и m кг, для 1 моля и m молей.
Что называется молярной массой и молярным объемом?
Напишите уравнение Менделеева-Клапейрона. Чему равны величины, входящие в это уравнение? Чему равна универсальная газовая постоянная и как она определяется?
Каковы физический смысл и размерность удельной и универсальной газовых постоянных? Какова связь между ними?
Сформулируйте закон Авогадро и напишите его уравнение. Укажите следствия из закона Авогадро.
Напишите соотношение плотностей газов и их молярных масс при одинаковых р и Т, а из него выведите соотношение и µ.
Как определяется значение удельной газовой постоянной для конкретных газов? От чего она зависит?
Напишите уравнение Ван-дер-Ваальса. Поясните его значение.
ЛАБОРАТОРНАЯ РАБОТА 3
