
- •Государственное образовательное учреждение высшего профессионального образования Санкт-Петербургский государственный горный институт им. Г.В. Плеханова (технический университет)
- •Конспект практических занятий физическая химия
- •Применение первого начала термодинамики к процессам в идеальных газах
- •Расчет теплоемкости Вычисление средней теплоемкости
- •Расчет теплоемкости по Нейману и Коппу
- •Расчет теплоемкости твердого вещества по Эйнштейну-Дебаю
- •Расчет теплоемкости газа по квантово-статистической теории
- •Расчет количества теплоты для нагревания/охлаждения вещества
- •Вычисление теплового эффекта химической реакции Вычисление теплового эффекта химической реакции через систему термохимических уравнений
- •Вычисление теплового эффекта химической реакции при обычных условиях
- •Вычисление теплового эффекта реакций в водных растворах по стандартным энтальпиям образования гидратированных ионов
- •Вычисление теплового эффекта при заданной температуре
- •Вычисление теплового баланса процесса
- •Вычисление изменения энтропии химической реакции Вычисление изменения энтропии химической реакции при обычных условиях
- •Вычисление изменения энтропии химической реакции при заданной температуре
- •Вычисление энергии Гиббса химической реакции и определение направления протекания процесса Вычисление энергии Гиббса для реакций, протекающих при обычных условиях
- •Вычисление изобарно-изотермического потенциала реакций в водных растворах по стандартным энергиям Гиббса образования гидратированых ионов
- •Вычисление энергии Гиббса химической реакции при заданной температуре
- •Использование закона действующих масс для расчета состава равновесной газовой смеси
- •Уравнение изотермы химической реакции (влияние состава на равновесие)
- •Расчет энергии Гиббса и константы равновесия при заданной температуре
- •6. Вычислить изменение энтропии реакции при 850 k:
- •8. Вычислить константу равновесия данной реакции по уравнению:
- •Метод Темкина-Шварцмана
- •Метод приведенных энергий Гиббса
- •Уравнение изобары химической реакции
- •1) Константу равновесия при данной температуре,;
- •2) Тепловой эффект реакции.
Расчет теплоемкости газа по квантово-статистической теории
![]() ;
;
![]() ;
;
![]() для
линейных молекул;
для
линейных молекул;
![]() для
нелинейных молекул
для
нелинейных молекул
Пример: определить изобарную теплоемкость аммиака при 500 и 1000 K.
Решение: из таблицы 110 «Краткого справочника физико-химических величин» взять значения характеристических температур для молекулы NH3 (молекула нелинейная, симметричная пирамида):
Ө |
4800 |
4968 |
1368 |
2341 |
Степень вырождения |
1 |
2 |
1 |
2 |
Ө/500 |
9,6 |
9,94 |
2,74 |
4,68 |
СЕ(500) |
0,05 |
0,039 |
4,604 |
1,723 |
Ө/1000 |
4,8 |
4,97 |
1,37 |
2,34 |
СЕ(1000) |
1,602 |
1,421 |
7,131 |
5,39 |
![]()
Т=500
![]()
Т=1000
![]()
Расчет количества теплоты для нагревания/охлаждения вещества
Нагревание вещества от обычной температуры до заданной без фазового превращения:
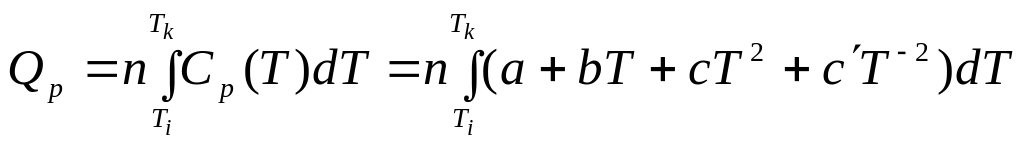
Нагревание вещества от обычной температуры до заданной с фазовым превращением:
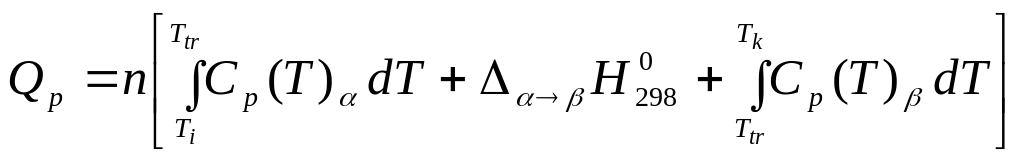
Пример 1. Определить количество теплоты, необходимое для нагревания 10 кг галенита (сульфид свинца (II)) от 25 до 1000°С.
Решение.
1. По таблице 44 «Термодинамические
свойства простых веществ…» определить
для сульфида свинца (II)
коэффициенты уравнения Келли:
![]() .
.
2. Проинтегрировать уравнение Кирхгофа:
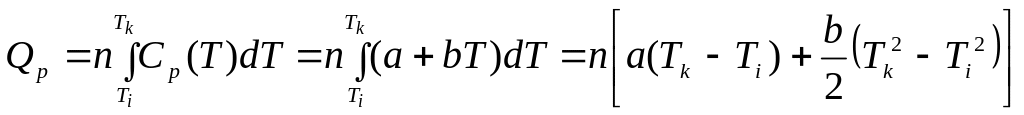 .
.
3. Определить количество вещества галенита:
![]()
4. Вычислить количество теплоты
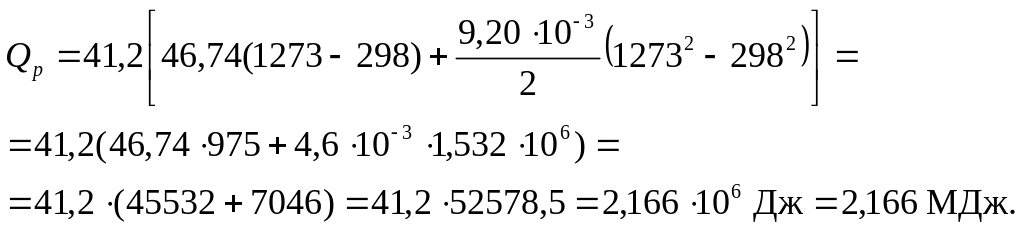
Пример
2. Вычислить
количество теплоты, выделившейся при
охлаждении 1 кг свинца от 1000 до 298 K
при изобарном процессе. Температура
плавления (кристаллизации) свинца
![]() 601 K,
изменение энтальпии плавления
601 K,
изменение энтальпии плавления
![]() 4,77 кДж/моль.
4,77 кДж/моль.
Решение. 1. По таблице 44 «Термодинамические свойства простых веществ…» определить для твердого и жидкого свинца коэффициенты уравнения Келли:
-
Pb(l)
Pb(s)
a
32,49
24,23
b∙103
‒3,09
8,71
2. Вычислить количество вещества свинца:
![]()
3. Процесс охлаждения состоит из трех стадий: охлаждение до точки плавления, кристаллизация, охлаждение до комнатной температуры твердого свинца.
4. Вычислить количество теплоты на каждой из стадий процесса:
а) охлаждение жидкого свинца от начальной температуры до температуры плавления;
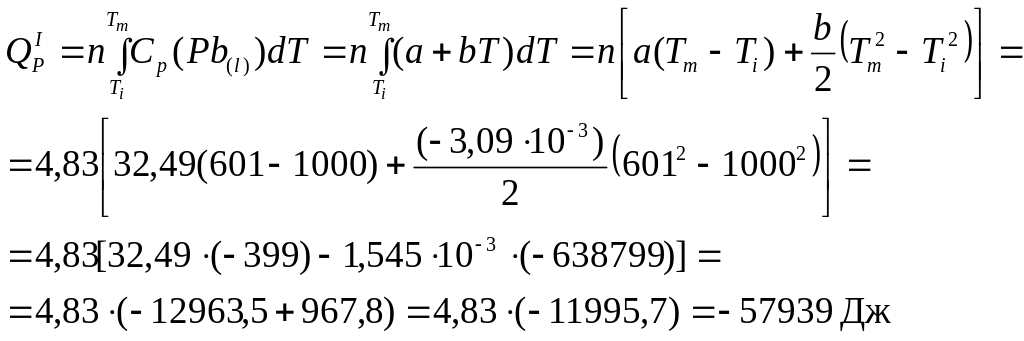
б)
кристаллизация жидкого свинца:
![]()
в) охлаждение твердого свинца от точки плавления до конечной температуры:
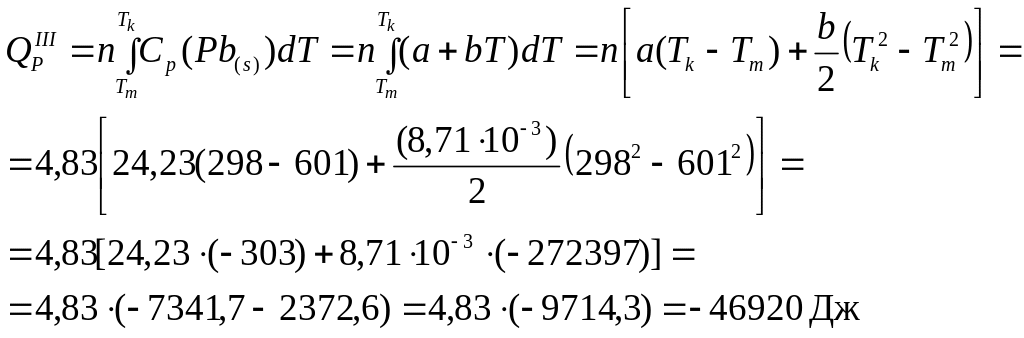
4. Суммировать количество теплоты по трем стадиям:
![]() .
.
Вычисление теплового эффекта химической реакции Вычисление теплового эффекта химической реакции через систему термохимических уравнений
Термохимическими называют уравнения реакций, в которых около символов химических соединений указываются агрегатные состояния этих соединений (s – твердое вещество, l – жидкость, g – газ, aq – водный раствор) или кристаллическая модификация и в правой части уравнения указываются численные значения тепловых эффектов. Согласно закону Гесса, с термохимическими уравнениями можно оперировать так же, как и с математическими.
Пример. Тепловые эффекты реакций при 0°С и давлении 1 атм:
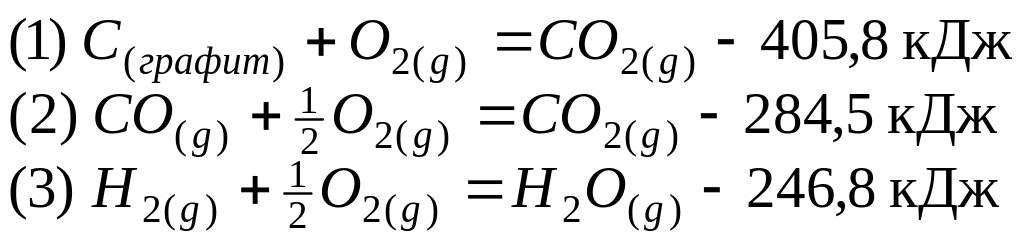
Вычислить при тех же условиях тепловой эффект реакции
![]()
Решение. Чтобы получить уравнение с неизвестным тепловым эффектом нужно
из уравнения (1) вычесть уравнение (2):
![]()
и из полученного результата вычесть уравнение (3):
![]()
получим
![]()
